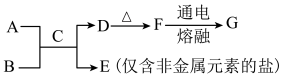
根据元素周期表和元素周期律判断,下列叙述不正确 的是
| A.氢元素与其他元素既可形成共价化合物也可形成离子化合物 |
| B.气态氢化物的稳定性:H2O > NH3 > SiH4 |
C.用中文“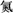 ”(ào)命名的第118号元素在周期表中位于第七周期0族 ”(ào)命名的第118号元素在周期表中位于第七周期0族 |
D.下图所示实验可证明元素的非金属性:Cl > C > Si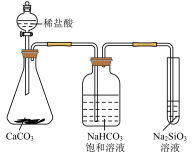 |
19-20高一下·山东济南·期中 查看更多[6]
辽宁省朝阳市建平县实验中学2021-2022学年高一下学期第一次月考化学试题安徽省蚌埠田家炳中学2020-2021学年高一4月月考化学试题黑龙江省大庆铁人中学2020-2021学年高一下学期开学考试化学试题(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)第16单元 物质的结构与性质(选考)(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷山东省济南市山东师范大学附属中学2019-2020学年高一下学期5月学业水平检测化学试题
更新时间:2020-11-03 17:06:09
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关元素周期律的说法正确的是
| A.离子半径:K+>Ca2+>Al3+ | B.元素原子得电子能力:P>S>Cl |
| C.碱性:Be(OH)2>Ca(OH)2 | D.热稳定性:CH4>NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关性质的比较,能用元素周期律解释的是
A.酸性: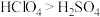 | B.沸点:H2S |
C.溶解性: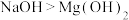 | D.热稳定性: |
您最近一年使用:0次
【推荐1】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 取两支试管,分别加入等体积等浓度的双氧水,然后试管①中加入0.01mol/LFeCl3溶液2mL,向试管②中加入0.01mol/LcuCl2溶液2mL,试管①产生气泡快 | 加入 时,双氧水分解反应的活化能较大 时,双氧水分解反应的活化能较大 |
| B | 将0.1mol/LAgNO3溶液和0.1mol/LNaCl溶液等体积混合,得到悬浊液后过滤,向滤液和白色沉淀中分别滴加0.1mol/LKI溶液,滤液出现浑浊,沉淀变为黄色 |  |
| C | 充分加热铁粉和硫粉的混合物,冷却后取少量固体于试管中,加入足量稀硫酸,再滴入K3[Fe(CN)6]溶液,产生蓝色沉淀 | 铁被硫氧化至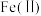 |
| D | 用pH试纸测定1mol/L的Na2S和NaCl溶液的pH,前者的试纸颜色比后者深 | 非金属性: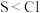 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】2022年9月9日,中国科学家首次在月球上发现一种磷酸盐矿物,命名为“嫦娥石”。该物质除了含钙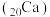 、铁
、铁 、钇
、钇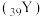 三种长周期元素外,还含有X、R、Z、W四种原子序数依次增大的短周期主族元素.仅X、W为非金属元素,R、Z相邻,且R是短周期原子半径最大的主族元素。下列叙述正确的是
三种长周期元素外,还含有X、R、Z、W四种原子序数依次增大的短周期主族元素.仅X、W为非金属元素,R、Z相邻,且R是短周期原子半径最大的主族元素。下列叙述正确的是
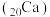 、铁
、铁 、钇
、钇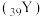 三种长周期元素外,还含有X、R、Z、W四种原子序数依次增大的短周期主族元素.仅X、W为非金属元素,R、Z相邻,且R是短周期原子半径最大的主族元素。下列叙述正确的是
三种长周期元素外,还含有X、R、Z、W四种原子序数依次增大的短周期主族元素.仅X、W为非金属元素,R、Z相邻,且R是短周期原子半径最大的主族元素。下列叙述正确的是A.铁 是第四周期ⅡB族元素 是第四周期ⅡB族元素 | B.原子半径: |
C.元素的金属性: | D.简单氢化物稳定性: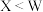 |
您最近一年使用:0次
单选题
|
适中
(0.65)
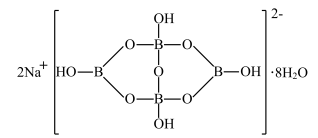
【推荐1】 俗称硼砂(硼砂在水溶液中存在水解平衡),其结构如下图所示。下列说法不正确的是
俗称硼砂(硼砂在水溶液中存在水解平衡),其结构如下图所示。下列说法不正确的是
 俗称硼砂(硼砂在水溶液中存在水解平衡),其结构如下图所示。下列说法不正确的是
俗称硼砂(硼砂在水溶液中存在水解平衡),其结构如下图所示。下列说法不正确的是
| A.硼砂的水溶液显碱性 |
B.硼原子的杂化方式为 、 、 |
| C.硼砂阴离子间可结合成链状结构,则阴离子间以氢键结合 |
| D.硼砂中存在的化学键类型有离子键、极性键、配位键、氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】Fe、Co、Ni均为第族元素,它们的化合物在生产、生活中有着广泛的应用,下列说法错误的是
| A.基态Fe原子中,电子填充的能量最高的能层符号为N |
B.铁氰化钾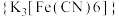 溶液是检验Fe2+常用的试剂。lmol 溶液是检验Fe2+常用的试剂。lmol 含 含 键的数目为12NA(NA为阿伏伽德罗常数的值) 键的数目为12NA(NA为阿伏伽德罗常数的值) |
| C.从电子排布的角度分析,在空气中FeO稳定性大于Fe2O3 |
D.Co3+的一种配离子 中,Co3+对的配位数是6 中,Co3+对的配位数是6 |
您最近一年使用:0次