①我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为___________ 价。
②海水中镁的总储量约为2×1015t,目前世界上生产的镁有60%来自海水,海水中的镁元素处于___________ (填“游离态”或“化合态”),从海水中提取氯化镁___________ (填“属于”或“不属于”)氧化还原反应。
②海水中镁的总储量约为2×1015t,目前世界上生产的镁有60%来自海水,海水中的镁元素处于
更新时间:2020-11-06 07:39:04
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】下表是某城市场销售的一种“加碘食盐”包装袋上的部分文字说明。
(1)碘酸钾属于__________(填“氧化物”、“酸”或“盐”),其中碘元素的化合价为__________;
(2)根据“加碘食盐”的食用方法,可推测碘酸钾在受热时__________________。
| 配料 | 氯化钠、碘酸钾(KIO3) |
| 含碘量 | 20-40mg·kg-1 |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
(1)碘酸钾属于__________(填“氧化物”、“酸”或“盐”),其中碘元素的化合价为__________;
(2)根据“加碘食盐”的食用方法,可推测碘酸钾在受热时__________________。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】维生素和微量元素是生命基础的重要物质。如中学生每天需要补充维生素C约60 mg,微量元素碘约150 μg。
(1)维生素C又称抗坏血酸,其水溶液显酸性。向维生素C的溶液中滴加紫色石蕊溶液,溶液变_______ 色。某同学欲探究维生素C的还原性,可选择的试剂是_______ (填序号)。
①氨水、淀粉 ②KI溶液 ③酸性KMnO4溶液
(2)加碘盐可预防碘缺乏症,其中加入的含碘物质是碘酸钾。碘酸钾的化学式为_______ (填序号)。
①I2 ②KI ③KIO3
已知在酸性条件下,碘化钾与碘酸钾反应可生成碘单质。若用盐酸酸化的碘化钾淀粉溶液检验加碘盐中的碘酸钾,可观察到的现象是_______ 。
(1)维生素C又称抗坏血酸,其水溶液显酸性。向维生素C的溶液中滴加紫色石蕊溶液,溶液变
①氨水、淀粉 ②KI溶液 ③酸性KMnO4溶液
(2)加碘盐可预防碘缺乏症,其中加入的含碘物质是碘酸钾。碘酸钾的化学式为
①I2 ②KI ③KIO3
已知在酸性条件下,碘化钾与碘酸钾反应可生成碘单质。若用盐酸酸化的碘化钾淀粉溶液检验加碘盐中的碘酸钾,可观察到的现象是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】为提高人体素质,避免人体缺碘影响正常的生命活动,我国早已采取食盐加碘措施。据报道,人从食物中摄取碘后碘便在甲状腺中积存下来,通过一系列化学反应可形成甲状腺素。甲状腺素的结构如下图,回答下列问题:

(1)甲状腺素由________ 种元素组成;
(2)“加碘食盐”中的碘元素以碘酸钾(KIO3)的形式存在, KIO3中碘的化合价是____ ,我们用稀盐酸和淀粉KI试纸可以检验食盐中碘酸钾的存在,实验现象是__________________ 。
(3)在“加碘食盐”包装袋上有“烹调时,待食品熟后加入碘盐”文字说明,由此可推测碘酸钾在受热时容易_____________ 。

(1)甲状腺素由
(2)“加碘食盐”中的碘元素以碘酸钾(KIO3)的形式存在, KIO3中碘的化合价是
(3)在“加碘食盐”包装袋上有“烹调时,待食品熟后加入碘盐”文字说明,由此可推测碘酸钾在受热时容易
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】化学与资源利用、材料研制、环境保护等密切相关。
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015t,海水里镁的存在形式主要是________ (填“游离态”或“化合态”)。
②下列物质不经过化学变化就能从海水中获得的是_________ (填字母)。
A.单质钠 B.单质钾 C.氯化钠
(2)保持洁净安全的生存环境已成为全人类的共识
①pH<_________ 的雨水称为酸雨。
②下列物质中,会破坏臭氧层的是_________ (填字母)。
A.氮气 B.一氧化碳 C.氟氯烃
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015t,海水里镁的存在形式主要是
②下列物质不经过化学变化就能从海水中获得的是
A.单质钠 B.单质钾 C.氯化钠
(2)保持洁净安全的生存环境已成为全人类的共识
①pH<
②下列物质中,会破坏臭氧层的是
A.氮气 B.一氧化碳 C.氟氯烃
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】为除去粗盐中的Ca2+、Mg2+、Fe3+、SO 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):

(1)第⑤步实验操作需要烧杯、___ 等玻璃仪器。
(2)步骤⑦中蒸发结晶时会用到下列仪器中的___ (填仪器名称)。
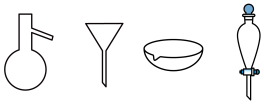
(3)除杂试剂Na2CO3、NaOH、BaCl2加入的顺序还可以是___ (任写一种合理顺序即可)
 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
(1)第⑤步实验操作需要烧杯、
(2)步骤⑦中蒸发结晶时会用到下列仪器中的

(3)除杂试剂Na2CO3、NaOH、BaCl2加入的顺序还可以是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(1)从海水中提取镁的流程如图所示:
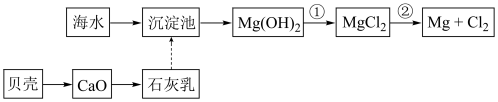
反应①的离子方程式为__ ;
反应②的化学方程式为__ ;
(2)海水提取溴流程:
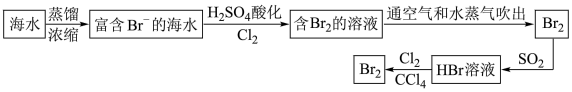
①该流程中涉及发生反应的离子方程式:__ ; ___ ;
②该流程中溴元素被氧化又被还原又被氧化的目的是:___ ;
③从最终溴的四氯化碳溶液中得到液溴,应采取的操作是__ 。
(1)从海水中提取镁的流程如图所示:

反应①的离子方程式为
反应②的化学方程式为
(2)海水提取溴流程:
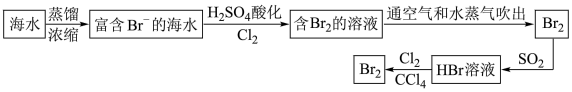
①该流程中涉及发生反应的离子方程式:
②该流程中溴元素被氧化又被还原又被氧化的目的是:
③从最终溴的四氯化碳溶液中得到液溴,应采取的操作是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】镁及其合金是一种用途很广的金属材料,目前世界上 的镁是从海水中提取的。主要步骤如下:
的镁是从海水中提取的。主要步骤如下:
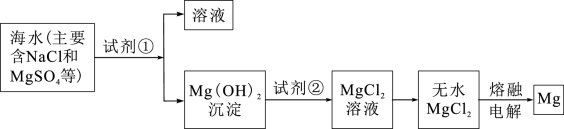
(1)为了使 转化为
转化为 ,试剂①可以选用
,试剂①可以选用_______ (填化学式)。
(2)加入试剂①后,能够分离得到 沉淀的方法是
沉淀的方法是_______ 。
(3)试剂②可以选用_______ (填化学式)。
(4) 的电子式为
的电子式为_______ ,无水 在熔融状态下,通电后会产生
在熔融状态下,通电后会产生 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
 的镁是从海水中提取的。主要步骤如下:
的镁是从海水中提取的。主要步骤如下:
(1)为了使
 转化为
转化为 ,试剂①可以选用
,试剂①可以选用(2)加入试剂①后,能够分离得到
 沉淀的方法是
沉淀的方法是(3)试剂②可以选用
(4)
 的电子式为
的电子式为 在熔融状态下,通电后会产生
在熔融状态下,通电后会产生 和
和 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】化学是一门以实验为基础的自然科学。根据题意回答下列问题:
(1)硅元素在自然界形成了多种含氧化合物,光导纤维的主要成分是_______ (填化学式);
(2)检验某溶液中是否含SO ,先加盐酸酸化,再加
,先加盐酸酸化,再加_______ 。(填“BaCl2”或“NaCl”)溶液;
(3)海水提镁的重要步骤之一是加沉淀剂将海水中的Mg2+转化为_______ 沉淀(填化学式);
(4)以下含氮物质中,遇到HCl会产生白烟的是_______ (用字母填空);在实验室制氨气的实验中,与氢氧化钙加热发生反应产生刺激性气味气体的是_______ (用字母填空)。
A、氮气 B、氨气 C、硝酸钠 D、氯化铵
(1)硅元素在自然界形成了多种含氧化合物,光导纤维的主要成分是
(2)检验某溶液中是否含SO
 ,先加盐酸酸化,再加
,先加盐酸酸化,再加(3)海水提镁的重要步骤之一是加沉淀剂将海水中的Mg2+转化为
(4)以下含氮物质中,遇到HCl会产生白烟的是
A、氮气 B、氨气 C、硝酸钠 D、氯化铵
您最近一年使用:0次



