(1)用50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和热。回答下列问题:
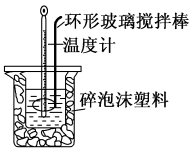
①烧杯间填满碎泡沫塑料的作用是____________ 。
②若大烧杯上改用薄铁板,求得的反应热将_____ (填“偏大”“偏小”或“无影响”)。
③若通过测定计算出产生的热量为1.42 kJ,请写出该反应的热化学方程式:_________________________________________ 。
(2)①已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为___________________________________ 。
②一定条件下,在水溶液中所含离子Cl-、ClO-、ClO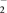 、ClO
、ClO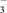 、ClO
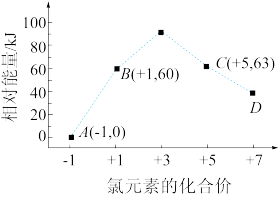
、ClO 各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO
各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO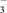 (aq)+2Cl-(aq)的ΔH=
(aq)+2Cl-(aq)的ΔH=____________ kJ·mol-1。

①烧杯间填满碎泡沫塑料的作用是
②若大烧杯上改用薄铁板,求得的反应热将
③若通过测定计算出产生的热量为1.42 kJ,请写出该反应的热化学方程式:
(2)①已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
②一定条件下,在水溶液中所含离子Cl-、ClO-、ClO
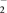 、ClO
、ClO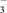 、ClO
、ClO 各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO
各1 mol,其相对能量(kJ)的大小如图所示(各离子在图中用氯元素的相应化合价表示),则反应3ClO-(aq)===ClO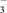 (aq)+2Cl-(aq)的ΔH=
(aq)+2Cl-(aq)的ΔH=
更新时间:2020-10-12 20:08:51
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理:

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为___________ 、_________________ ,制得等量H2所需能量较少的是________ 。
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
由此计算△H1=________ kJ/mol;已知△H2=-58kJ/mol,则△H3=_______ kJ/mol。

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为
(2)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3回答下列问题:
已知反应①中相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1=
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】汽车尾气中的主要污染物是NOx和CO,它们是现代化城市中的重要大气污染物。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是_______ ,图1中对应反应的热化学方程式为_______ 。 △H。有关化学反应的能量变化过程如图2所示。
△H。有关化学反应的能量变化过程如图2所示。_______ ,该反应的△H=_______ ;
②在反应体系中加入Pt2O+作为该反应的催化剂,则△H_______ (填“增大”“减小”或“不变”)。
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:
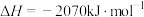 。若有15 g NO被还原,则释放的热量为
。若有15 g NO被还原,则释放的热量为_______ kJ。
(4)“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。已知25℃和101 kPa下:
①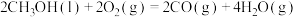 △H =-a kJ/mol
△H =-a kJ/mol
② △H =-b kJ/mol
△H =-b kJ/mol
③H2O(g)=H2O(l) △H =-c kJ/mol
则表示CH3OH(l)燃烧热的热化学方程式为_______ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是

 △H。有关化学反应的能量变化过程如图2所示。
△H。有关化学反应的能量变化过程如图2所示。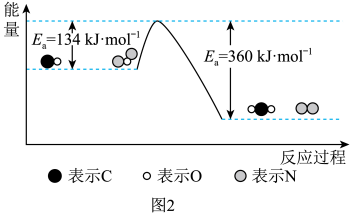
②在反应体系中加入Pt2O+作为该反应的催化剂,则△H
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:

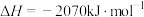 。若有15 g NO被还原,则释放的热量为
。若有15 g NO被还原,则释放的热量为(4)“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。已知25℃和101 kPa下:
①
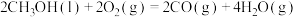 △H =-a kJ/mol
△H =-a kJ/mol②
 △H =-b kJ/mol
△H =-b kJ/mol ③H2O(g)=H2O(l) △H =-c kJ/mol
则表示CH3OH(l)燃烧热的热化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
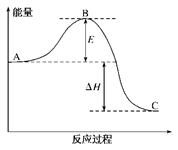
【推荐3】2SO2(g)+O2(g)==2SO3(g)反应过程中的能量变化如下图所示。
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示__________ 的能量、___________ 的能量;
(2)图中ΔH=______________________ ;
(3)已知单质硫的燃烧热为-296 kJ·mol-1,计算由S(s)生成3mol SO3(g)ΔH=___________ ;
(4)化学反应的焓变与反应物和生成物的键能有关。
已知:①H2(g)+Cl2(g)=2HCl(g) ΔH=-185 kJ·mol-1
②H—H键能为436kJ·mol-1,Cl—Cl键能为247kJ·mol-1。则H—Cl键能为____________________ 。
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示
(2)图中ΔH=
(3)已知单质硫的燃烧热为-296 kJ·mol-1,计算由S(s)生成3mol SO3(g)ΔH=
(4)化学反应的焓变与反应物和生成物的键能有关。
已知:①H2(g)+Cl2(g)=2HCl(g) ΔH=-185 kJ·mol-1
②H—H键能为436kJ·mol-1,Cl—Cl键能为247kJ·mol-1。则H—Cl键能为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)在200℃、101kPa时,0.5molH2(g)与足量I2(g)完全反应放出7.45kJ的热量,该反应的热化学方程式表示为____ 。
(2)根据键能数据估算
CH4(g)+4F2(g) =CF4(g)+4HF(g)的反应热ΔH为______ kJ/mol
(3) 已知:①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH1=-a kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-b kJ/mol
③2H2(g) + O2(g) = 2H2O(g) ΔH3 = -c kJ/mol
a、b、c均大于0 则:反应①中,ΔS______ (选填“>”、“<”或“=”)0;
2C(s)+4H2(g)+O2(g) = 2CH3OH(l) ΔH=_______ kJ/mol。
(1)在200℃、101kPa时,0.5molH2(g)与足量I2(g)完全反应放出7.45kJ的热量,该反应的热化学方程式表示为
(2)根据键能数据估算
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
CH4(g)+4F2(g) =CF4(g)+4HF(g)的反应热ΔH为
(3) 已知:①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH1=-a kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-b kJ/mol
③2H2(g) + O2(g) = 2H2O(g) ΔH3 = -c kJ/mol
a、b、c均大于0 则:反应①中,ΔS
2C(s)+4H2(g)+O2(g) = 2CH3OH(l) ΔH=
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学在能源开发与利用中起着十分关键的作用。
(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为_____ 。
(2)家用液化气中主要成分之一是丁烷。当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ。试写出丁烷燃烧的热化学方程式:____ 。
(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为
(2)家用液化气中主要成分之一是丁烷。当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ。试写出丁烷燃烧的热化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)某反应A(g)+B(g)=C(g)+D(g)过程中的能量变化如图所示,回答问题。
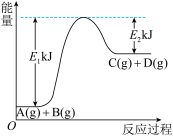
①该反应是_______ (填“吸热”或“放热”)反应,反应的ΔH=_______ kJ•mol-1(用含E1、E2的代数式表示)。
②该反应过程中,断裂旧化学键吸收的总能量_______ (填“>”“<”或“=”)形成新化学键释放的总能量。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:_______ 。
(3)有机物M经过太阳光光照可转化成N,转化过程如图: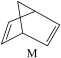
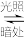
 △H=+88.6kJ•mol-1,则M、N相比,较稳定的是
△H=+88.6kJ•mol-1,则M、N相比,较稳定的是_______ 。
(4)已知CH3OH(l)的燃烧热为726.5kJ•mol-1,CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H=-akJ•mol-1,则a
O2(g)=CO2(g)+2H2(g) △H=-akJ•mol-1,则a_______ 726.5(填“>”、“<”或“=”)。
(1)某反应A(g)+B(g)=C(g)+D(g)过程中的能量变化如图所示,回答问题。

①该反应是
②该反应过程中,断裂旧化学键吸收的总能量
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(3)有机物M经过太阳光光照可转化成N,转化过程如图:

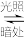
 △H=+88.6kJ•mol-1,则M、N相比,较稳定的是
△H=+88.6kJ•mol-1,则M、N相比,较稳定的是(4)已知CH3OH(l)的燃烧热为726.5kJ•mol-1,CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H=-akJ•mol-1,则a
O2(g)=CO2(g)+2H2(g) △H=-akJ•mol-1,则a
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)用括号内的字母代号填空:中和热测定实验时,使用的酸和碱最好是_______ (A.恰好完全反应;B.酸稍过量;C.碱稍过量),溶液混合的时候应_______ (A.一次性快速倒入;B.缓缓滴入),若用环形铜丝代替环形玻璃搅拌棒,会导致测定数据_______ (A.偏高;B.偏低)。
(2)保护环境已成为当前和未来的一项全球性重大课题。为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促进燃料循环使用的构想,如图所示:

过程I的能量转化形式为_______ 能转化为_______ 能。
(3)有机物M经过太阳光照射可转化成N,转化过程如下:
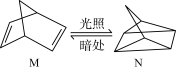 △H=+88.6 kJ·mol−1。
△H=+88.6 kJ·mol−1。
则M、N相比,较稳定的是_______ 。
(4)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。其过程如下所示:

反应I:2H2SO4(l) 2SO2(g)+2H2Og)+O2(g) △H1=+551 kJ·mol−1
2SO2(g)+2H2Og)+O2(g) △H1=+551 kJ·mol−1
反应Ⅲ:S(s)+O2(g)=SO2(g) △H2=-297 kJ·mol−1
写出反应Ⅱ的热化学方程式:_______ 。
(1)用括号内的字母代号填空:中和热测定实验时,使用的酸和碱最好是
(2)保护环境已成为当前和未来的一项全球性重大课题。为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促进燃料循环使用的构想,如图所示:

过程I的能量转化形式为
(3)有机物M经过太阳光照射可转化成N,转化过程如下:
 △H=+88.6 kJ·mol−1。
△H=+88.6 kJ·mol−1。则M、N相比,较稳定的是
(4)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。其过程如下所示:

反应I:2H2SO4(l)
 2SO2(g)+2H2Og)+O2(g) △H1=+551 kJ·mol−1
2SO2(g)+2H2Og)+O2(g) △H1=+551 kJ·mol−1反应Ⅲ:S(s)+O2(g)=SO2(g) △H2=-297 kJ·mol−1
写出反应Ⅱ的热化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液测定计算中和反应的反应热。
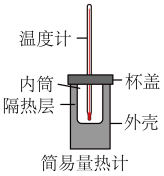
回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是_______ 。
②如改用0.0275molNaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将_______ (填“偏大”、“偏小”或“无影响”)。
(2)反应mA(g)+nB(g) pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
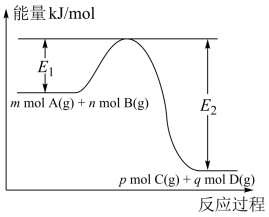
①该反应ΔH=_______ (用含E1、E2式子表示);
②在反应体系中加入催化剂,E1_______ (填“增大”、“减小”、“不变”),ΔH_______ (填“增大”、“减小”、“不变”)。
(3)依据事实,写出下列反应的热化学方程式:
①4g硫粉在O2中完全燃烧生成SO2气体,放出37kJ热量,写出表示硫燃烧热的热化学方程式为:_______ 。
②25℃101kPa时,氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水,放出2.444kJ的热量。请写出氢气和氧气反应生成1mol液态水时的热化方程式为:_______ 。
(4)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①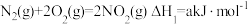
②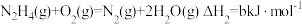
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:_______ 。
(1)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液测定计算中和反应的反应热。

回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是
②如改用0.0275molNaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将
(2)反应mA(g)+nB(g)
 pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
①该反应ΔH=
②在反应体系中加入催化剂,E1
(3)依据事实,写出下列反应的热化学方程式:
①4g硫粉在O2中完全燃烧生成SO2气体,放出37kJ热量,写出表示硫燃烧热的热化学方程式为:
②25℃101kPa时,氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水,放出2.444kJ的热量。请写出氢气和氧气反应生成1mol液态水时的热化方程式为:
(4)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①
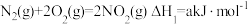
②
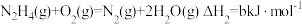
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮元素在工业应用上有重要地位,回答下列问题:
(1)理论研究表明,在 和
和 下,
下, 异构化反应的能量变化如图。
异构化反应的能量变化如图。
___________ 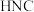 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②该异构化反应的
___________ 
(2)“长征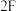 ”运载火箭使用
”运载火箭使用 和
和 (偏二甲册)作推进剂。
(偏二甲册)作推进剂。 液态
液态 在液态
在液态 中燃烧生成
中燃烧生成 、
、 、
、 三种气体,放出
三种气体,放出 热量。该反应的热化学方程式为
热量。该反应的热化学方程式为________ 。
(3)科学家用氮气和氢气制备肼,过程如下:

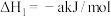

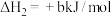
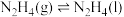
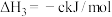
则

___________  (用含a、b、c的计算式表示)。
(用含a、b、c的计算式表示)。
(4)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式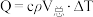 计算获得。
计算获得。
①热量的测定:取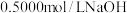 溶液和
溶液和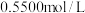 盐酸各
盐酸各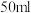 进行反应,测得反应前后体系的温度值(℃)分别为
进行反应,测得反应前后体系的温度值(℃)分别为 、
、 ,则该过程放出的热量为
,则该过程放出的热量为___________ J(c和 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
________  。
。
②下列操作会使所测得的焓变 偏小的是
偏小的是___________
a.用等物质的量浓度的醋酸代替盐酸实验
b.量热装置绝热效果欠佳
c. 溶液量多了
溶液量多了
(1)理论研究表明,在
 和
和 下,
下, 异构化反应的能量变化如图。
异构化反应的能量变化如图。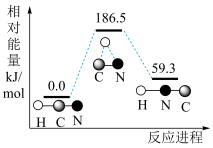

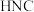 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②该异构化反应的


(2)“长征
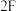 ”运载火箭使用
”运载火箭使用 和
和 (偏二甲册)作推进剂。
(偏二甲册)作推进剂。 液态
液态 在液态
在液态 中燃烧生成
中燃烧生成 、
、 、
、 三种气体,放出
三种气体,放出 热量。该反应的热化学方程式为
热量。该反应的热化学方程式为(3)科学家用氮气和氢气制备肼,过程如下:

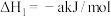

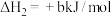
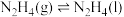
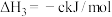
则


 (用含a、b、c的计算式表示)。
(用含a、b、c的计算式表示)。(4)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式
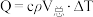 计算获得。
计算获得。①热量的测定:取
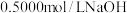 溶液和
溶液和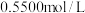 盐酸各
盐酸各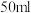 进行反应,测得反应前后体系的温度值(℃)分别为
进行反应,测得反应前后体系的温度值(℃)分别为 、
、 ,则该过程放出的热量为
,则该过程放出的热量为 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
 。
。②下列操作会使所测得的焓变
 偏小的是
偏小的是a.用等物质的量浓度的醋酸代替盐酸实验
b.量热装置绝热效果欠佳
c.
 溶液量多了
溶液量多了
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】SO2、NOx是主要的空气污染源,需经过处理才能排放。回答下列问题:
(1)二氧化硫在V2O5作用下的催化氧化是工业上产生硫酸的主要反应。催化反应的机理是:
第一步:SO2(g)+V2O5(s)=SO3(g)+V2O4(s) ΔH=+akJ•mol-1
第二步:V2O4(s) +O2(g)+2SO2(g)=2VOSO4(s) ΔH=-bkJ•mol-1
第三步:4VOSO4(s)+O2(g)=2V2O5(s)+4SO3(g) ΔH=-ckJ•mol-1
请写出二氧化硫催化氧化的热化学方程式___________ 。
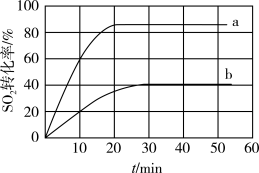
(2)一定条件下,用Fe2O3作催化剂对燃煤烟气进行回收。反应为2CO(g)+SO2(g) 2CO2(g)+S(l) ΔH<0.80℃时,在容积恒为1L的密闭容器中投入总物质的量为2mol的气体,按n(CO):n(SO2)为1:1或3:1投料时SO2转化率的变化情况如图。则图中表示n(CO):n(SO2)=1:1的变化曲线为
2CO2(g)+S(l) ΔH<0.80℃时,在容积恒为1L的密闭容器中投入总物质的量为2mol的气体,按n(CO):n(SO2)为1:1或3:1投料时SO2转化率的变化情况如图。则图中表示n(CO):n(SO2)=1:1的变化曲线为___________ (填字母),若曲线bSO2的平衡转化率是42%,用SO2表示30min内的平均反应速率是___________ 。CO2和SO2的中心原子杂化方式分别为______ ,_____ 。
(3)一定温度下,在容积恒为1L的密闭容器中,充入0.3molNO与过量的金属Al,发生的反应存在如下平衡:Al(s)+2NO(g N2(g)+Al2O3(s) ΔH<0.已知在此条件下NO与N2的消耗速率与各自的浓度有如下关系(k1、k2为速率常数):v(NO)=k1•c2(NO),v(N2)=k2•c(N2)。
N2(g)+Al2O3(s) ΔH<0.已知在此条件下NO与N2的消耗速率与各自的浓度有如下关系(k1、k2为速率常数):v(NO)=k1•c2(NO),v(N2)=k2•c(N2)。
①在T1温度下,k1=0.004L•mol•min-1,k2=0.002min-1,该温度下反应的平衡常数的值为______ 。
②T2温度下,NO的物质的量随时间的变化如图,其平衡常数的值为___________ ;温度T1___________ T2(填“小于”“等于”或“大于”),判断理由是___________ 。

(1)二氧化硫在V2O5作用下的催化氧化是工业上产生硫酸的主要反应。催化反应的机理是:
第一步:SO2(g)+V2O5(s)=SO3(g)+V2O4(s) ΔH=+akJ•mol-1
第二步:V2O4(s) +O2(g)+2SO2(g)=2VOSO4(s) ΔH=-bkJ•mol-1
第三步:4VOSO4(s)+O2(g)=2V2O5(s)+4SO3(g) ΔH=-ckJ•mol-1
请写出二氧化硫催化氧化的热化学方程式
(2)一定条件下,用Fe2O3作催化剂对燃煤烟气进行回收。反应为2CO(g)+SO2(g)
 2CO2(g)+S(l) ΔH<0.80℃时,在容积恒为1L的密闭容器中投入总物质的量为2mol的气体,按n(CO):n(SO2)为1:1或3:1投料时SO2转化率的变化情况如图。则图中表示n(CO):n(SO2)=1:1的变化曲线为
2CO2(g)+S(l) ΔH<0.80℃时,在容积恒为1L的密闭容器中投入总物质的量为2mol的气体,按n(CO):n(SO2)为1:1或3:1投料时SO2转化率的变化情况如图。则图中表示n(CO):n(SO2)=1:1的变化曲线为
(3)一定温度下,在容积恒为1L的密闭容器中,充入0.3molNO与过量的金属Al,发生的反应存在如下平衡:Al(s)+2NO(g
 N2(g)+Al2O3(s) ΔH<0.已知在此条件下NO与N2的消耗速率与各自的浓度有如下关系(k1、k2为速率常数):v(NO)=k1•c2(NO),v(N2)=k2•c(N2)。
N2(g)+Al2O3(s) ΔH<0.已知在此条件下NO与N2的消耗速率与各自的浓度有如下关系(k1、k2为速率常数):v(NO)=k1•c2(NO),v(N2)=k2•c(N2)。①在T1温度下,k1=0.004L•mol•min-1,k2=0.002min-1,该温度下反应的平衡常数的值为
②T2温度下,NO的物质的量随时间的变化如图,其平衡常数的值为

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1) 焙烧产生的
焙烧产生的 可用于制硫酸。
可用于制硫酸。
已知:25℃、101kPa时,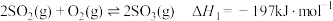 ;
;
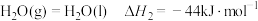 ;
;
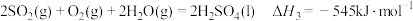 ;
;
则 与
与 反应生成
反应生成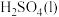 的热化学方程式是
的热化学方程式是___________ 。
(2)某实验小组用 的NaOH溶液和
的NaOH溶液和 的
的 溶液进行中和反应的反应热测定。
溶液进行中和反应的反应热测定。
①测定稀硫酸和氢氧化钠稀溶液反应的反应热的实验装置如图所示。则仪器A的名称为___________ 。

②碎泡沫塑料的作用是___________ 。
(3)取 溶液和
溶液和 溶液进行实验,实验数据如下表。
溶液进行实验,实验数据如下表。
①温度差的平均值为___________ ℃。(保留两位有效数字)
②近似认为 的NaOH溶液和
的NaOH溶液和 的
的 溶液的密度都是
溶液的密度都是 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容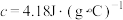 。则测得生成
。则测得生成 时中和反应的反应热
时中和反应的反应热
___________ (取小数点后一位)。
(1)
 焙烧产生的
焙烧产生的 可用于制硫酸。
可用于制硫酸。已知:25℃、101kPa时,
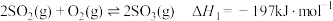 ;
;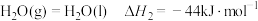 ;
;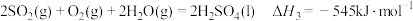 ;
;则
 与
与 反应生成
反应生成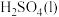 的热化学方程式是
的热化学方程式是(2)某实验小组用
 的NaOH溶液和
的NaOH溶液和 的
的 溶液进行中和反应的反应热测定。
溶液进行中和反应的反应热测定。①测定稀硫酸和氢氧化钠稀溶液反应的反应热的实验装置如图所示。则仪器A的名称为

②碎泡沫塑料的作用是
(3)取
 溶液和
溶液和 溶液进行实验,实验数据如下表。
溶液进行实验,实验数据如下表。| 实验次数 | 反应物温度/℃ | 反应前体系的温度 /℃ /℃ | 反应后体系的温度 /℃ /℃ | |
 | NaOH | |||
| 1 | 26.6 | 26.6 | 26.6 | 29.1 |
| 2 | 27.0 | 27.0 | 27.0 | 31.0 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
②近似认为
 的NaOH溶液和
的NaOH溶液和 的
的 溶液的密度都是
溶液的密度都是 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容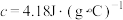 。则测得生成
。则测得生成 时中和反应的反应热
时中和反应的反应热
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】能量是人类生存基础,因此化学反应与能量关系一直是研究热点,贯穿于生活和生产各个领域 .
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为_______
(2)化学反应中放出的热能(焓变),△H与反应物和生成物的键能E有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=-185kJ/mol, E(H-H)=436kJ/mol,E(Cl-Cl)=243kJ/mol。
则E(H-Cl)=___________
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,已知:
2Cu(s)+ O2(g)=CuO(s) △H=-169kJ.mol-1.
O2(g)=CuO(s) △H=-169kJ.mol-1.
C(s)+ O2(g)=CO(g) △H=-110.5kJ.mol-1
O2(g)=CO(g) △H=-110.5kJ.mol-1
2Cu(s)+O2(g)=2CuO(s) △H=-314kJ.mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu和CO的热化学方程__________
(4)如图是N2和H2反应生成2molNH3过程中能量变化示意图
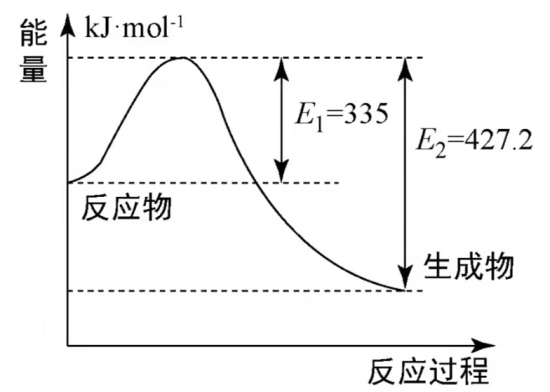
①请计算每生成1moNH3放出热量为___________
②若起始时向容器内放入1moN2和3molH2达平衡后N2的反应体积分数为20%,则反应放出的热量为Q1kJ,则Q1的数值为___________
(5)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是_______
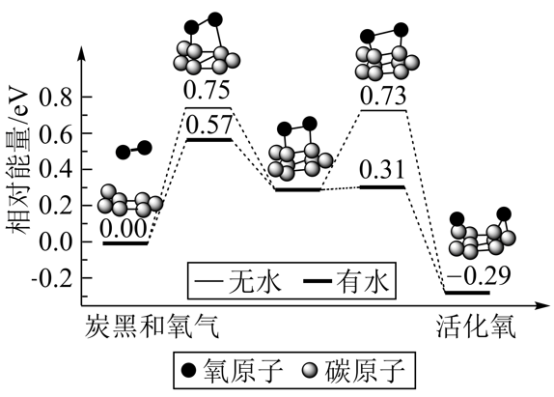
A.氧分子的活化包括O-O键的断裂与C-O键的生成
B.每活化一个氧分子放出0.29eV的能量
C.水可使氧分子活化反应的活化能降低0.42eV
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为
(2)化学反应中放出的热能(焓变),△H与反应物和生成物的键能E有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=-185kJ/mol, E(H-H)=436kJ/mol,E(Cl-Cl)=243kJ/mol。
则E(H-Cl)=
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,已知:
2Cu(s)+
 O2(g)=CuO(s) △H=-169kJ.mol-1.
O2(g)=CuO(s) △H=-169kJ.mol-1.C(s)+
 O2(g)=CO(g) △H=-110.5kJ.mol-1
O2(g)=CO(g) △H=-110.5kJ.mol-12Cu(s)+O2(g)=2CuO(s) △H=-314kJ.mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu和CO的热化学方程
(4)如图是N2和H2反应生成2molNH3过程中能量变化示意图

①请计算每生成1moNH3放出热量为
②若起始时向容器内放入1moN2和3molH2达平衡后N2的反应体积分数为20%,则反应放出的热量为Q1kJ,则Q1的数值为
(5)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是

A.氧分子的活化包括O-O键的断裂与C-O键的生成
B.每活化一个氧分子放出0.29eV的能量
C.水可使氧分子活化反应的活化能降低0.42eV
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
您最近半年使用:0次



