金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制的工业方法,其反应原理:2NaCl(熔融) 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是____________ 。
A.放在棕色瓶中 B.放在细沙中 C.放在水中 D.放在煤油中
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,请写出发生反应的化学方程式:________ ,生成物的颜色为_______ 。
(3)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为_______________ (填化学式)。将少量金属钠投入硫酸铜溶液中写出发生的离子反应方程式___________ 。
(4)过氧化钠中阴阳离子个数比为________ ,过氧化钠常用于呼吸面具和潜水艇氧气的来源,其原理为:__________ ,______ (用化学反应方程式表示) 。
(5)已知CO2+2NaOH=Na2CO3+H2O,Na2CO3+H2O+CO2=2NaHCO3,Na2CO3+HCl= NaHCO3,NaHCO3+HCl=H2O+CO2。现将一定量的CO2通入NaOH溶液中,再向所得溶液中逐滴滴加盐酸,所得气体的体积与加入盐酸的物质的量关系如图所示:
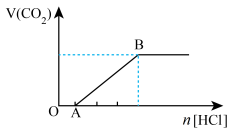
①其中OA段发生的离子反应方程式为____________ 。
②达到B点时所消耗盐酸为5mol,则原NaOH溶液中所含溶质的质量为_____ 。
 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:(1)下列各项中属于保存金属钠的正确方法是
A.放在棕色瓶中 B.放在细沙中 C.放在水中 D.放在煤油中
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,请写出发生反应的化学方程式:
(3)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为
(4)过氧化钠中阴阳离子个数比为
(5)已知CO2+2NaOH=Na2CO3+H2O,Na2CO3+H2O+CO2=2NaHCO3,Na2CO3+HCl= NaHCO3,NaHCO3+HCl=H2O+CO2。现将一定量的CO2通入NaOH溶液中,再向所得溶液中逐滴滴加盐酸,所得气体的体积与加入盐酸的物质的量关系如图所示:

①其中OA段发生的离子反应方程式为
②达到B点时所消耗盐酸为5mol,则原NaOH溶液中所含溶质的质量为
更新时间:2020-11-10 21:54:27
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】钠是活泼金属,受热后与氧气剧烈反应,发出黄色火焰,生成一种淡黄色固体——过氧化钠,由于空气中还有其它成分,因此可能还有一些同时发生的其它反应”。某校化学兴趣小组同学据此进行了有关探究。
【猜想】钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
【查阅资料】氮化钠与水反应能生成氢氧化钠和氨气。
【实验】①取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224L(折算成标准状态)气体和1000mL溶液;
③经检验,该气体为纯净的氧气;
④从1000mL溶液中取出25.00mL溶液,加入1.00mol·L-1HCl溶液至13.50mL时恰好完全反应。
【结论】
(1)通过计算确定钠的燃烧产物中是否含有氮化钠___________ 。
(2)计算钠在空气中燃烧产物中各成分的物质的量之比___________ 。
【猜想】钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
【查阅资料】氮化钠与水反应能生成氢氧化钠和氨气。
【实验】①取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224L(折算成标准状态)气体和1000mL溶液;
③经检验,该气体为纯净的氧气;
④从1000mL溶液中取出25.00mL溶液,加入1.00mol·L-1HCl溶液至13.50mL时恰好完全反应。
【结论】
(1)通过计算确定钠的燃烧产物中是否含有氮化钠
(2)计算钠在空气中燃烧产物中各成分的物质的量之比
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】有一块表面被氧化成Na2O的金属钠,质量4.91g,投入95.29g水中,完全反应后,收集到标准状况下的氢气体积为2.24L。
(1)其中含Na2O的质量为______________ 。
(2)反应后所得溶液的质量分数为_____________ 。
(3)若反应后所得溶液的密度为ρ g/cm3,则其溶质的物质的量浓度为______________ (用含ρ的代数式表示)。
(1)其中含Na2O的质量为
(2)反应后所得溶液的质量分数为
(3)若反应后所得溶液的密度为ρ g/cm3,则其溶质的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含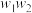 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为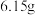 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为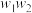 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
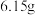 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式______ ,____ 。
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气体,则该漂白粉中所含有效成分的质量为_____________ (假设漂白粉中的其它成分不与硝酸反应)。
(2)将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:原混合物中Na2O的质量为______ g,所得溶液的物质的量浓度为______ mol·L-1。

①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气体,则该漂白粉中所含有效成分的质量为
(2)将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:原混合物中Na2O的质量为
您最近一年使用:0次
【推荐2】根据所学知识填写下列空白。
(1)在标准状况下,1.7g氨气与同条件下______ molH2S含有相同的氢原子数。
(2)在标准状况下,某气体的密度为2.86g•L-1,则其相对分子质量为______ (取整数值)。
(3)某气态氧化物化学式为R2O3,在标准状况下,1.52g该氧化物的体积是448mL,则R的摩尔质量为______ g•mol-1。
(4)将18.7gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体2.24L,所得溶液的体积为500mL,试计算:原混合物中Na2O的物质的量为______ mol。所得溶液中溶质的物质的量浓度为______ mol•L-1。
(5)现有含Na2SO4、MgSO4和NaNO3的混合溶液1L,已知其中c(Mg2+)=0.4mol•L-1,c(SO )=0.7mol•L-1, c(NO
)=0.7mol•L-1, c(NO )=0.2mol•L-1,则此溶液中c(Na+)为
)=0.2mol•L-1,则此溶液中c(Na+)为______ mol•L-1。
(1)在标准状况下,1.7g氨气与同条件下
(2)在标准状况下,某气体的密度为2.86g•L-1,则其相对分子质量为
(3)某气态氧化物化学式为R2O3,在标准状况下,1.52g该氧化物的体积是448mL,则R的摩尔质量为
(4)将18.7gNa2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体2.24L,所得溶液的体积为500mL,试计算:原混合物中Na2O的物质的量为
(5)现有含Na2SO4、MgSO4和NaNO3的混合溶液1L,已知其中c(Mg2+)=0.4mol•L-1,c(SO
 )=0.7mol•L-1, c(NO
)=0.7mol•L-1, c(NO )=0.2mol•L-1,则此溶液中c(Na+)为
)=0.2mol•L-1,则此溶液中c(Na+)为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】向
 和
和 的混合溶液中逐滴加入
的混合溶液中逐滴加入 的盐酸,产生
的盐酸,产生 气体的体积(标准状况下)与所加盐酸的体积关系如图所示。
气体的体积(标准状况下)与所加盐酸的体积关系如图所示。

请回答:
(1)OA段反应的离子方程式为____ 。
(2)混合溶液中 的物质的量浓度为
的物质的量浓度为____ 。
(3)最终产生 气体的体积(标准状况下)为多少mL
气体的体积(标准状况下)为多少mL____ ?(此小题需写出解题过程)。

 和
和 的混合溶液中逐滴加入
的混合溶液中逐滴加入 的盐酸,产生
的盐酸,产生 气体的体积(标准状况下)与所加盐酸的体积关系如图所示。
气体的体积(标准状况下)与所加盐酸的体积关系如图所示。
请回答:
(1)OA段反应的离子方程式为
(2)混合溶液中
 的物质的量浓度为
的物质的量浓度为(3)最终产生
 气体的体积(标准状况下)为多少mL
气体的体积(标准状况下)为多少mL
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将质量为44.4克含有少量NaCl的纯碱晶体(Na2CO3·nH2O)样品,平均分成A、B、C三份,进行如图实验,进行如图实验(Na2CO3受热不分).

(1)将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是______ .
(2)A样品中与BaCl2溶液反应的Na2CO3的质量是______ 克.
(3)B样品中含有结晶水的质量是______ 克.
(4)化学式Na2CO3·nH2O中n的数值是.______
(5)对C样品的操作结束后,所得NaCl溶液的溶质质量分数是______ (精确到0.01%)

(1)将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是
(2)A样品中与BaCl2溶液反应的Na2CO3的质量是
(3)B样品中含有结晶水的质量是
(4)化学式Na2CO3·nH2O中n的数值是.
(5)对C样品的操作结束后,所得NaCl溶液的溶质质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】取一定物质的量浓度的NaOH溶液100 mL,向其通入一定量的CO2气体,得到溶质为Na2CO3和NaHCO3的溶液A,向A中逐滴缓慢加入2mol·L-1的盐酸,产生CO2的体积与所加盐酸的体积之间关系如图所示。(假设产生的 CO2全部逸出)
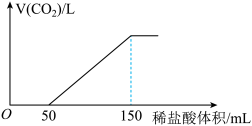
(1)加入盐酸0~50mL时发生的离子方程式为__________ 。
(2)Na2CO3与NaHCO3的物质的量之比是___________ 。
(3)通入的CO2的物质的量为___________ 。
(4)原NaOH溶液的物质的量浓度是___________ 。

(1)加入盐酸0~50mL时发生的离子方程式为
(2)Na2CO3与NaHCO3的物质的量之比是
(3)通入的CO2的物质的量为
(4)原NaOH溶液的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)向10mL lmol/L的NaOH溶液中加入10mL l mol/L的H2SO4溶液,加热、蒸干,得到固体A的化学式是_____________________ 。
(2)向40mL 1mol/L的NaOH溶液中通入过量的CO2,并将溶液分成两等份。
①一份加热、蒸干、灼烧,所得固体的化学式是_____________________ 。
②将(1)中所得固体A全部放入另一份溶液中,发生反应的离子方程式是____________ 。混合后的溶液充分搅拌后,加热、蒸干、灼烧,所得固体中两种阴离子的物质的量之比是________ 。
(2)向40mL 1mol/L的NaOH溶液中通入过量的CO2,并将溶液分成两等份。
①一份加热、蒸干、灼烧,所得固体的化学式是
②将(1)中所得固体A全部放入另一份溶液中,发生反应的离子方程式是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】100mL稀盐酸中加入混合均匀的NaHCO3和KHCO3固体粉末,充分反应后使气体全部逸出,下图是加入粉末的质量与产生CO2(该状况下,气体的密度为1.964g/L)体积的关系。请计算:

(1)该盐酸中HCl的质量为_____ g。
(2)若该盐酸为120mL时,加入粉末为58.5g,则产生CO2的体积为_______ 。
(3)若粉末的质量为xg,该盐酸的体积为140mL,产生的CO2体积为yL.请把粉末质量x(g)与产生CO2体积y(L)之间的关系填入下表(可不填满):___________

(1)该盐酸中HCl的质量为
(2)若该盐酸为120mL时,加入粉末为58.5g,则产生CO2的体积为
(3)若粉末的质量为xg,该盐酸的体积为140mL,产生的CO2体积为yL.请把粉末质量x(g)与产生CO2体积y(L)之间的关系填入下表(可不填满):
| 粉末质量x(g)的取值范围 | CO2体积y(L) |
| ___________ | ______________ |
| _____________ | ______________ |
| _______________ | ______________ |
| ____________________ | ___________ |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(1)研究性学习小组的同学,为测定某纯碱样品(含少量的氯化钠)中碳酸钠的质量分数,设计下列两种不同实验方案进行探究。
①方案1:取mg纯碱样品,溶于水加入过量的氯化钙溶液,过滤、用蒸馏水洗涤、烘干、称重得ag固体,计算出纯碱样品纯度。写出方案1发生反应的离子方程式___________ ;如何洗涤沉淀,方法是______________________ 。
②方案2:取mg纯碱样品,加入过量的盐酸,充分反应后,蒸发,灼烧,称重得bg固体,计算出纯碱样品纯度为___________________ 。
(2)将CO2通入NaOH和KOH的混合溶液中,恰好得到等物质的量混合的NaHCO3和 KHCO3的混合物ag,再将其与100mL 盐酸反应。(题中涉及的气体体积以标准状况计,填空时可以用带字母的数学式表示,不必化简)。
①该混合物中NaHCO3和KHCO3的质量比为_________________ 。
②如果反应后盐酸不足量,要计算生成CO2的体积,还需知道_________ 。
③若该混合物与盐酸恰好完全反应,则盐酸的物质的量浓度为_________ 。
④若NaHCO3和KHCO3不是以等物质的量混合,则ag固体混合物与足量的盐酸完全反应时,生成CO2的体积的取值范围是_____________ 。
①方案1:取mg纯碱样品,溶于水加入过量的氯化钙溶液,过滤、用蒸馏水洗涤、烘干、称重得ag固体,计算出纯碱样品纯度。写出方案1发生反应的离子方程式
②方案2:取mg纯碱样品,加入过量的盐酸,充分反应后,蒸发,灼烧,称重得bg固体,计算出纯碱样品纯度为
(2)将CO2通入NaOH和KOH的混合溶液中,恰好得到等物质的量混合的NaHCO3和 KHCO3的混合物ag,再将其与100mL 盐酸反应。(题中涉及的气体体积以标准状况计,填空时可以用带字母的数学式表示,不必化简)。
①该混合物中NaHCO3和KHCO3的质量比为
②如果反应后盐酸不足量,要计算生成CO2的体积,还需知道
③若该混合物与盐酸恰好完全反应,则盐酸的物质的量浓度为
④若NaHCO3和KHCO3不是以等物质的量混合,则ag固体混合物与足量的盐酸完全反应时,生成CO2的体积的取值范围是
您最近一年使用:0次



