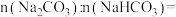计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含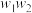 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为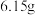 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为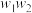 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
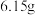 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
更新时间:2023-03-09 18:03:36
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】NA表示阿伏加 德罗常数的值,请完成下列填空:
(1)1 mol CH3+所含质子总数为_____ NA;标准状况下,11.2 L氯化氢中含有氯原子的数目为___ NA。
(2)常温常压下,2.24 L C2H4和C2H2的混合气体中含碳原子数目_____ (填“<”、“=”或“>”)0.2NA。
(3)标准状况下有①6.72L甲烷,②3.01×1023个氯化氢分子,③13.6gH2S气体,④0.2mol氨气。则下列对这四种气体关系从小到大排列的顺序为(填序号)
氢原子数________ ,密度_________ ,质量__________ ,体积___________ 。
(1)1 mol CH3+所含质子总数为
(2)常温常压下,2.24 L C2H4和C2H2的混合气体中含碳原子数目
(3)标准状况下有①6.72L甲烷,②3.01×1023个氯化氢分子,③13.6gH2S气体,④0.2mol氨气。则下列对这四种气体关系从小到大排列的顺序为(填序号)
氢原子数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积的关系如图所示(不考虑CO2在水中的溶解)。
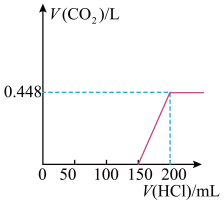
(1)写出 0~150mL 段发生反应的离子方程式为:____________ ;150mL ~200mL段发生反应的离子方程式为:___________________ ;
(2)所用盐酸的物质的量浓度为_______________ ;
(3)将上述氢氧化钠固体样品溶于水,所形成溶液的溶质为___________ 、_________ (写化学式),其物质的量分别为 ____________ 、_______________ 。

(1)写出 0~150mL 段发生反应的离子方程式为:
(2)所用盐酸的物质的量浓度为
(3)将上述氢氧化钠固体样品溶于水,所形成溶液的溶质为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)3.01×1023个氯气分子的物质的量是________ ,氯原子的物质的量是________ 。
(2)1.5molNa2SO4·10H2O中所含的Na+的物质的量是________ ,所含的SO42-的物质的量是________ ,所含H2O的数目是______ 。
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为______ 。
(4)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为_____ ,R的相对原子质量为________ 。含R的质量为1.6g的Na2R,其物质的量为_____ 。
(2)1.5molNa2SO4·10H2O中所含的Na+的物质的量是
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为
(4)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为
您最近一年使用:0次
【推荐1】将SO2通入用硫酸酸化的重铬酸钾溶液中,可制得硫酸铬钾KCr(SO4)2,反应的化学方程式为_______ ;如果溶液的酸碱性控制不当,可能会有Cr(OH)SO4杂质生成。现从得到的硫酸铬钾产品中取出3.160g样品加入足量盐酸和BaCl2溶液后,得到白色沉淀5.126g。若产品中杂质只有Cr(OH)SO4,则该产品中KCr(SO4)2的质量分数为_______ (用百分数表示,保留1位小数)。[摩尔质量/g·mol-1:KCr(SO4)2283;Cr(OH)SO4165]
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在酸性溶液中用400mL 0.075mol·L-1的KMnO4溶液处理2g Cu2S和CuS的混合物,发生如下反应:8MnO4-+5Cu2S +44H+=10Cu2++5SO2+8Mn2++22H2O; 6MnO4-+5CuS +28H+=5Cu2++5SO2+6Mn2++14H2O反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1mol·L-1的FeSO4溶液完全反应。请完成以下问题:
(1)配平KMnO4与FeSO4反应的离子方程式:__________ MnO4-+_______ Fe2++__________ H+=__________ Mn2++__________ Fe3++__________ H2O
(2)KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为__________ mol
(3)混合物中Cu2S的质量分数为__________
(1)配平KMnO4与FeSO4反应的离子方程式:
(2)KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为
(3)混合物中Cu2S的质量分数为
您最近一年使用:0次
【推荐3】实验室可以用KClO3和50mL浓盐酸反应制取Cl2,反应原理如下:
KClO3+HCl→KCl+Cl2↑+H2O
(1)配平上述化学方程式并用双线桥标出电子转移方向与数目__________________ ;
(2)浓盐酸在上述反应中表现出来的性质是__ (填选项编号)
A.只有氧化性 B.只有还原性 C.还原性和酸性 D.氧化性和酸性
(3)若产生0.1mol Cl2,则转移电子的物质的量为_______ (保留两位小数)
(4)若反应中HCl的利用率只有50%,当氧化产物比还原产物比还原产物多7.1g时,浓盐酸的物质的量浓度为__________ .
KClO3+HCl→KCl+Cl2↑+H2O
(1)配平上述化学方程式并用双线桥标出电子转移方向与数目
(2)浓盐酸在上述反应中表现出来的性质是
A.只有氧化性 B.只有还原性 C.还原性和酸性 D.氧化性和酸性
(3)若产生0.1mol Cl2,则转移电子的物质的量为
(4)若反应中HCl的利用率只有50%,当氧化产物比还原产物比还原产物多7.1g时,浓盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将10.8g表面被氧化的金属钠投入到足量的水中得到溶液200mL,并生成2.24L的气体(标准状况下)。往得到的溶液中通入一定量的CO2气体,充分反应后将溶液低温蒸干,得到固体27.4g。求:
(1)原金属中单质钠的质量分数(保留一位小数)___ ;
(2)所得200mL溶液的物质的量浓度___ ;
(3)通入的CO2在标准状况下的体积___ 。
(1)原金属中单质钠的质量分数(保留一位小数)
(2)所得200mL溶液的物质的量浓度
(3)通入的CO2在标准状况下的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】把一块表面已部分被氧化为氧化钠的钠块1.08g放入20g水中,得到标准状况下氢气224mL。求:
①被氧化前钠块的质量__________________ 。
②所得溶液中溶质的质量分数_____________ (计算结果均保留两位有效数字)
①被氧化前钠块的质量
②所得溶液中溶质的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠___ g。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。_______
(3)计算并确定该钠-钾合金的化学式__________ 。
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
(3)计算并确定该钠-钾合金的化学式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】取一定物质的量浓度的 NaOH 溶液 100 mL,向其通入一定量的 CO2气体,得到溶液 A,向A 中逐滴缓慢加入 2 mol·L-1的盐酸,产生CO2的体积 (标准状况)与所加盐酸的体积之间关系如图所示。(假设产生的 CO2全部逸出)
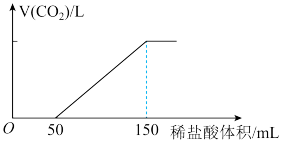
(1)A 溶液中的溶质为______________ ,其物质的量之比是_________ 。
(2)通入的CO2的物质的量为_________ 。
(3)原NaOH溶液的物质的量浓度是_________ 。

(1)A 溶液中的溶质为
(2)通入的CO2的物质的量为
(3)原NaOH溶液的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组同学对由NaHCO3和KHCO3组成的某均匀混合物进行实验,测得如下数据(盐酸的物质的量浓度相等):
(1)盐酸的物质的量浓度是多少?_____
(2)混合物中,n(NaHCO3)∶n(KHCO3)是多少?__________
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| 标准状况下,V(CO2) | 2.24L | 3.36L | 3.36L |
(1)盐酸的物质的量浓度是多少?
(2)混合物中,n(NaHCO3)∶n(KHCO3)是多少?
您最近一年使用:0次

 ,并且杂质分布均匀)。为测定其组成,称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加
,并且杂质分布均匀)。为测定其组成,称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加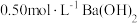 溶液至30.00mL时恰好完全沉淀。
溶液至30.00mL时恰好完全沉淀。 溶液中溶质的物质的量为
溶液中溶质的物质的量为