下列依据热化学方程式得出的结论正确的是( )
A.已知 2SO2 + O2 2SO3 为放热反应,则 SO2 的能量一定高于 SO3 的能量 2SO3 为放热反应,则 SO2 的能量一定高于 SO3 的能量 |
B.由 C(s) + O2 (g) ═ CO(g)△H=-110.5 kJ•mol﹣1 可知碳的燃烧热为 110.5 kJ•mol﹣1 O2 (g) ═ CO(g)△H=-110.5 kJ•mol﹣1 可知碳的燃烧热为 110.5 kJ•mol﹣1 |
| C.若 C(石墨,s) = C(金刚石,s)△H>0,则石墨比金刚石稳定 |
| D.已知 2C(s) +2O2 (g)═2CO2 (g) △H1,2C(s) + O2 (g) ═ 2CO(g)△H2,则△H1>△H2 |
更新时间:2020-11-12 17:46:34
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】发射火箭的燃料常用联氨(N2H4)、液氢(H2),氧化剂有液氧(O2)、液态 等。下列叙述
等。下列叙述错误 的是
 等。下列叙述
等。下列叙述| A.液氢和液氧燃烧放出大量热量,产物对环境友好 |
B.发射场因液态 产生大量 产生大量 而呈红棕色 而呈红棕色 |
| C.液氢和液氧在气化过程中发生了吸热反应 |
D. 和 和 反应中产物总能量小于反应物总能量 反应中产物总能量小于反应物总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】氢气和氧气发生反应的过程,可用如下模型表示(“-”表示化学键),下列说法不正确 的是

| A.过程I是吸热过程 |
| B.该反应为放热反应 |
| C.状态a的总能量大于状态d的总能量 |
| D.该反应的能量转化形式只能以热能的形式进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法或表示方法中正确的是
| A.相同条件下,等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应ΔH1>ΔH2 |
| B.由C(石墨)→C(金刚石) ΔH=+1.9kJ/mol ,可知金刚石比石墨稳定 |
| C.在稀溶液中,H+ (aq)+ OH-(aq) =H2O(l) ΔH =-57.3 kJ/mol,若将含0.5 mol硫酸的浓硫酸与含1 molNaOH的溶液混合,放出的热量大于57.3 kJ |
| D.已知在101KPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量。则有关氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH =+285.8kJ/mol |
您最近一年使用:0次
【推荐2】苯基甲基乙炔( )可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
)可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:

已知: ,下列说法正确的是
,下列说法正确的是
 )可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
)可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
已知:
 ,下列说法正确的是
,下列说法正确的是A. 中最多4个碳原子共线 中最多4个碳原子共线 |
B.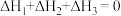 |
| C.产物Ⅱ比产物I稳定,两者互为立体异构体 |
| D.反应I的活化能大于反应Ⅱ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是( )
| A.101kPa时,2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1,则H2的燃烧热ΔH=-572kJ·mol-1 |
B.一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ 2NH3(g) ΔH=-92.4kJ·mol-1,此条件下将1.5mol H2和过量N2充分反应,放出热量46.2kJ |
| C.若将等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| D.已知:2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列热化学方程式中ΔH的数值表示可燃物燃烧热或中和热的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-802.3kJ·mol-1 |
B.C(s)+ O2(g)=CO(g) ΔH=-393.5kJ·mol-1 O2(g)=CO(g) ΔH=-393.5kJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1 |
| D.OH-(aq)+CH3COOH(aq)=CH3COO-(aq)+H2O(l) ΔH=-54.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法正确 的是()
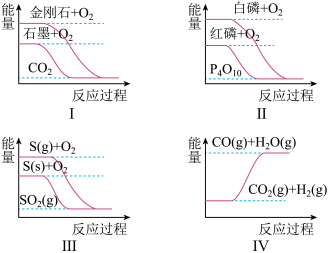

| A.金刚石比石墨稳定 |
| B.红磷转变为白磷是吸热反应 |
| C.S(g)+O2(g) === SO2(g) ΔH1;S(s)+O2(g) === SO2(g) ΔH2,则ΔH1>ΔH2 |
| D.CO(g)+H2O(g) === CO2(g)+H2(g) ΔH>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.1molH2与0.5molO2反应放出的热量就是H2的燃烧热 |
| B.已知含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)= CH3COONa(aq)+H2O(l)△H=-57.4 kJ·mol-1 |
| C.已知2C(s)+2O2=(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
| D.使用氢气作燃料有助于控制温室效应 |
您最近一年使用:0次

 )在铜基催化剂上的反应机理如下(该反应为可逆反应)
)在铜基催化剂上的反应机理如下(该反应为可逆反应)
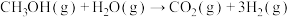 是热能转化为化学能的过程
是热能转化为化学能的过程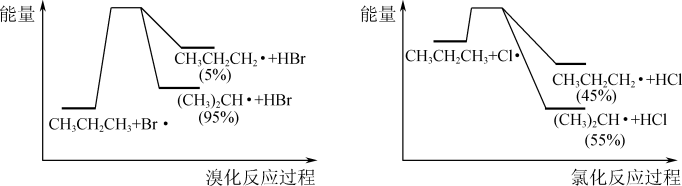
 ,则
,则 反应的
反应的
 偏小
偏小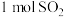 和
和 置于密闭容器中充分反应,放出热量
置于密闭容器中充分反应,放出热量 ,则:
,则:






