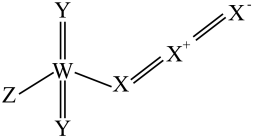
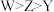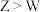X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲+乙=丁+己,甲+丙=戊+己;0.1mol·L−1丁溶液的pH为13(25℃).下列说法正确的是
| A.原子半径:W>Z>Y>X |
| B.Y元素在周期表中的位置为第3周期第ⅣA族 |
| C.1mol甲与足量的乙完全反应共转移1mol电子 |
| D.化合物甲中只有离子键 |
更新时间:2020-11-25 23:33:48
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各组原子中,彼此化学性质一定相似的是
| A.最外层都只有1个电子的基态X、Y原子 |
| B.2p轨道上有1对成对电子的基态X原子与3p轨道上有1对成对电子的基态Y原子 |
| C.原子核外电子排布式为1s2的基态X原子与原子核外电子排布式为1s22s2的基态Y原子 |
| D.原子核外M层上仅有2个电子的基态X原子与原子核外N层上仅有2个电子的基态Y原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,W的最高正价与最低负价代数和为0,W、X、Y形成的化合物甲的结构如图所示,Z原子M层上有2个未成对电子且此能级无空轨道。下列说法正确的是


| A.简单离子半径大小:Z>X>Y |
| B.简单氢化物的沸点:Z>X |
| C.X、Y形成的化合物只含离子键 |
| D.化合物甲中阴离子的空间构型为三角锥形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】短周期元素X、Y、Z、W原子序数依次增大,X原子的最外层有5个电子,Y是迄今发现的非金属性最强的元素,Z的原子半径是短周期元素原子中最大的,W与Y属于同一主族。下列说法错误的是
| A.简单离子半径:Y>Z |
| B.对应氢化物的稳定性:Y>X |
| C.Z和W两种元素组成的物质为离子化合物 |
| D.Z、X、Y对应的最高正价依次升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】科学家利用原子序数依次递增的W、X、Y、Z四种短周期元素,“组合”成一种具有高效催化性能的超分子,其分子结构示意图如图所示(短线代表共价键)。其中W、X、Z分别位于不同周期,Z是同周期中金属性最强的元素。下列说法正确的是
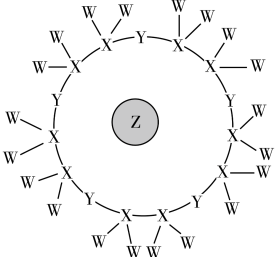

| A.简单离子半径:Z>Y>W |
| B.Y与W、X、Z均能形成至少两种化合物 |
| C.氢化物的沸点: Y>X |
| D.l mol ZW与水发生反应生成1mol W2,转移电子2mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,这四种元素仅处于两个周期,其中X元素的最外层电子数是其层数的3倍,这四种元素构成的一种离子化合物的结构如图所示。下列说法正确的是( )
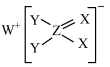
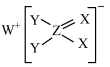
| A.原子半径Y>Z>X |
| B.单质W在其同族元素形成的单质中熔点最低 |
| C.Z的最高价氧化物对应的水化物是中强酸 |
| D.该化合物中的所有元素均满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
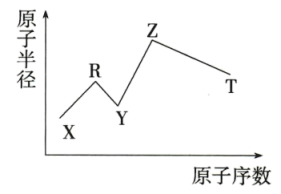
【推荐2】现有短周期主族元素X、Y、Z、R、T,R原子最外层电子数是电子层数的2倍,Z是金属元素,且在短周期中其原子半径最大,Y与Z能形成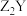 、
、 型化合物,Z与T形成化学式为
型化合物,Z与T形成化学式为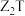 的化合物,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
的化合物,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
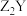 、
、 型化合物,Z与T形成化学式为
型化合物,Z与T形成化学式为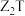 的化合物,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
的化合物,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
A.原子半径和离子半径均满足: |
B.最高价氧化物对应的水化物的酸性: |
C.简单氢化物的稳定性: |
| D.由X、Y、Z、T四种元素组成的化合物的水溶液一定呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】W、X、Y、Z为原子序数依次增大的4种元素,它们的最外层电子数分别为1、6、7、1。W-的核外电子结构与氦相同,X和Y的次外层有8个电子,Y-和Z+的核外电子结构相同。下列叙述正确的是
| A.W元素的三种核素的氧化物互为同素异形体 |
| B.W元素和其他3种元素均能形成共价化合物 |
| C.Z元素和其他3种元素均能形成离子化合物 |
| D.W元素与其他3种元素均能形成18电子微粒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素; Z原子的最外层电子数是其最内层电子数的 ;W的最高正价和最低负价的代数和为0。下列说法正确的是
;W的最高正价和最低负价的代数和为0。下列说法正确的是
 ;W的最高正价和最低负价的代数和为0。下列说法正确的是
;W的最高正价和最低负价的代数和为0。下列说法正确的是| A.原子半径:X<Y<Z<W |
| B.Z的氢化物中只含离子键 |
| C.最高价氯化物对应水化物的酸性:Y>W |
| D.X和W两种元素形成的化合物,既能与强酸反应又能与强碱反应 |
您最近一年使用:0次