下列说法正确的是( )
| A.非金属性:Cl>S | B.第ⅠA族元素都是碱金属元素 |
| C.碱性:LiOH>NaOH | D.卤族元素最高化合价均为+7价 |
更新时间:2020-11-18 21:32:38
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】有关性质的比较中,不能用元素周期律解释的是
| A.热稳定性:HCl>HBr | B.金属性:Mg>Be |
| C.碱性:KOH>Ca(OH)2 | D.酸性:H2SO4>HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关元素性质的递变规律错误的是
| A.VIA族元素原子得电子能力:Se>S>O |
| B.原子半径:Na>Cl>F |
| C.金属性:Na>Mg>Al |
| D.酸性:HClO4>H2SO4>H3PO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】由下列事实进行归纳推测,推测不合理的是
| 选项 | 事实 | 推测 |
| A | Mg与水反应缓慢,Ca与水反应较快 | Ba与水反应会更快 |
| B | Si和Ge都是半导体材料 | 第IVA族元素的单质都可作半导体 |
| C | Al与Cl形成共价键,Mg与Cl形成离子键 | Na和Cl形成离子键 |
| D | HCl在1500℃时分解,HI在300℃时分解 | HBr的分解温度介于二者之间 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】运用元素周期律分析下面的推断,其中错误的是
①铍(Be)的最高价氧化物对应的水化物可能具有两性;②铊(Tl)位于周期表第六周期且与铝同族,其单质既能与盐酸反应产生氢气,又能与 溶液反应产生氢气;③砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸;④锂溶于水生成一种强碱;⑤硫酸锶
溶液反应产生氢气;③砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸;④锂溶于水生成一种强碱;⑤硫酸锶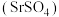 是难溶于水的白色固体;⑥硒化氢
是难溶于水的白色固体;⑥硒化氢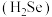 是无色、有毒、比
是无色、有毒、比 稳定的气体
稳定的气体
①铍(Be)的最高价氧化物对应的水化物可能具有两性;②铊(Tl)位于周期表第六周期且与铝同族,其单质既能与盐酸反应产生氢气,又能与
 溶液反应产生氢气;③砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸;④锂溶于水生成一种强碱;⑤硫酸锶
溶液反应产生氢气;③砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸;④锂溶于水生成一种强碱;⑤硫酸锶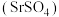 是难溶于水的白色固体;⑥硒化氢
是难溶于水的白色固体;⑥硒化氢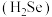 是无色、有毒、比
是无色、有毒、比 稳定的气体
稳定的气体| A.①②③④ | B.②④⑥ | C.①③⑤ | D.②④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】判断 的非金属性比
的非金属性比 强,可依据的事实是
强,可依据的事实是
 的非金属性比
的非金属性比 强,可依据的事实是
强,可依据的事实是| A.氧气无色无味,硫淡黄色 |
| B.常温下氧气是气体,硫是固体 |
C.气态氢化物的热稳定性: |
D.硫最高化合价是 |
您最近一年使用:0次



