已知化学反应N2+3H2=2NH3的能量变化如图所示,
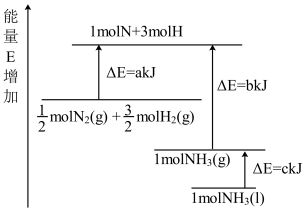
(1)1mol N 和3mol H 生成1mol NH3(g)是_________ 能量的过程(填“吸收”或“释放”)。
(2) N2(g)+
N2(g)+ H2(g)=NH3(g) △H =
H2(g)=NH3(g) △H =_________ ;

(1)1mol N 和3mol H 生成1mol NH3(g)是
(2)
 N2(g)+
N2(g)+ H2(g)=NH3(g) △H =
H2(g)=NH3(g) △H =
更新时间:2020-12-10 17:34:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有科学家预言,氢能将成为21世纪的主要能源之一,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是____ (只答一点即可)。
(2)在101kPa下,1gH2完全燃烧生成液态水放出143.9kJ的热量,请回答下列问题:
①该反应的生成物总能量____ (填“大于”“小于”或“等于”)反应物总能量。
②氢气的燃烧热为_____ 。
③该反应的热化学方程式为____ 。
④若1molH2完全燃烧生成1mol气态水放出241kJ的热量,已知H-O的键能为463kJ·mol-1,H-H的键能为436kJ·mol-1,计算O=O的键能为_____ kJ·mol-1。
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) △H1=-72.5kJ·mol-1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H2=-64.4kJ·mol-1;
MgNi2(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) △H3。
则△H3=_____ kJ·mol-1。
(1)氢能被称为绿色能源的原因是
(2)在101kPa下,1gH2完全燃烧生成液态水放出143.9kJ的热量,请回答下列问题:
①该反应的生成物总能量
②氢气的燃烧热为
③该反应的热化学方程式为
④若1molH2完全燃烧生成1mol气态水放出241kJ的热量,已知H-O的键能为463kJ·mol-1,H-H的键能为436kJ·mol-1,计算O=O的键能为
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) △H1=-72.5kJ·mol-1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H2=-64.4kJ·mol-1;
MgNi2(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) △H3。
则△H3=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ. (1)下列条件的改变能增大活化分子百分数的是_____________ 。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。

则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=__________ kJ·mol-1。
Ⅱ.2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
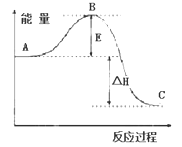
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示___________ ,E表示______________ ;该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,理由是____________ ;
(2)图中△H=_________ kJ·mol-1。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。

则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=
Ⅱ.2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示
(2)图中△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。CH4(g)+2H2O(g) CO2(g)+4H2(g)ΔH3=+akJ·mol-1
CO2(g)+4H2(g)ΔH3=+akJ·mol-1
(1)写出甲烷的结构式___________
(2)C=O的键能为_______________ kJ/mol(用含a、b、c、d的式子表示)
(3)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应。测得甲烷物质的量随时间变化如下表所示。0~10min内用H2O的浓度表示该反应的平均速率为υ(H2O)=_____________
(4)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是_______________ 。
a.混合气体的平均相对分子质量保持不变b.CO2和H2的体积分数比为1﹕4
c.混合气体的密度保持不变d.1molCO2生成的同时有4molH-H键断裂
(5)写出甲烷燃料电池,以KOH溶液为介质时,负极的电极反应式______
 CO2(g)+4H2(g)ΔH3=+akJ·mol-1
CO2(g)+4H2(g)ΔH3=+akJ·mol-1| 化学键 | C—H | H—H | H—O |
| 键能kJ/mol | b | c | d |
(1)写出甲烷的结构式
(2)C=O的键能为
(3)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应。测得甲烷物质的量随时间变化如下表所示。0~10min内用H2O的浓度表示该反应的平均速率为υ(H2O)=
| 时间/min | 0 | 10 | 20 | 40 | 50 | 60 |
| n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | 0.10 |
(4)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变b.CO2和H2的体积分数比为1﹕4
c.混合气体的密度保持不变d.1molCO2生成的同时有4molH-H键断裂
(5)写出甲烷燃料电池,以KOH溶液为介质时,负极的电极反应式
您最近一年使用:0次



