甲醇是一种重要的化工原料和新型燃料。下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A,B两极上产生的气体体积相同。
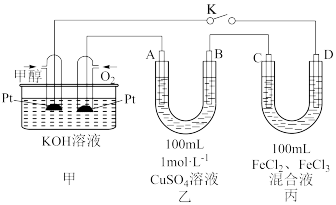
(1)甲中正极的电极反应式为________________ 。
(2)乙装置中初始时电解的化学方程式为________________ 。
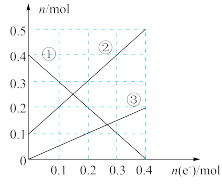
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如下图,曲线②是________ 离子变化,则D极的电极反应式为________________ ,混合液中c(Fe3+)=________ 。反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要________ mL 5.0 mol•L-1 NaOH溶液。

(1)甲中正极的电极反应式为
(2)乙装置中初始时电解的化学方程式为
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如下图,曲线②是

更新时间:2020-12-23 09:50:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】原电池和电解池都能实现能量的置换。回答下列问题:
(1)可将化学能转化为电能是_________ 池;
(2)下列反应能设计成原电池的是:__________
①2FeCl3+Fe=3FeCl2
②AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl
③NaOH+HCl=NaCl+H2O
(3)用FeCl3溶液腐蚀印刷电路铜板的离子方程式为:________________________ 。
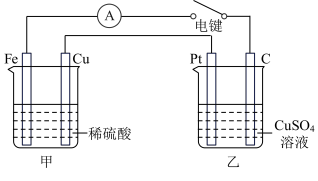
(4)右图装置当闭合电键时,电表显示有电流通过。则Pt极的电极反应式:___________ ;当甲中产生0.1mol气体时,乙中析出铜的质量应为________ g。
(1)可将化学能转化为电能是
(2)下列反应能设计成原电池的是:
①2FeCl3+Fe=3FeCl2
②AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl
③NaOH+HCl=NaCl+H2O
(3)用FeCl3溶液腐蚀印刷电路铜板的离子方程式为:
(4)右图装置当闭合电键时,电表显示有电流通过。则Pt极的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】认真观察下列装置,回答下列问题:
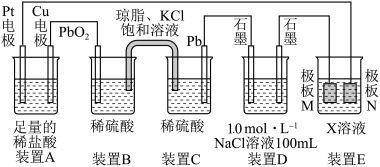
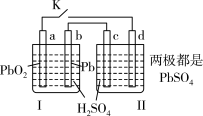
(1)装置B中PbO2上发生的电极反应方程式为________________
(2)装置A中总反应的离子方程式为_____________________________ 。
(3)若装置E中的目的是在Cu材料上镀银,则X为________ ,极板N的材料为________ 。
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为________ L(标准状况下)。
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。
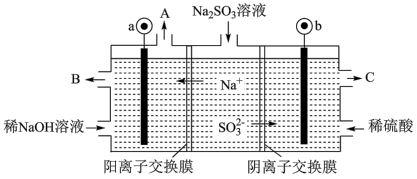
①图中a极连接电源的___________ 极,
②b极电极反应式为____________________________________________

(1)装置B中PbO2上发生的电极反应方程式为
(2)装置A中总反应的离子方程式为
(3)若装置E中的目的是在Cu材料上镀银,则X为
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。

①图中a极连接电源的
②b极电极反应式为
您最近一年使用:0次
【推荐3】电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效。广谱。快速。安全的杀菌消毒剂。目前已开发出用电解法制取C1O2的新工艺如图所示。
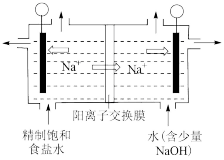
图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极的电极反应式为_______ ;电解过程中右侧电极区pH_______ (填“增大”。“减小”或“不变”)。
(2)燃料电池因具有发电效率高。环境污染少等优点而备受人们关注。用于笔记本电脑的甲醇(CH3OH) 燃料电池示意图如下,b是_______ 极,写出a电极的电极反应式_______ 。
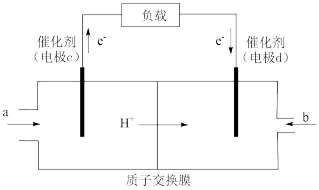
(3)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。
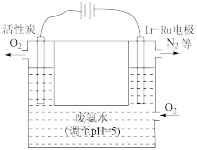
①为了不影响H2O2的产量,需要向废氨水中加入适量HNO3调节溶液的pH约为5,则所得溶液中c( )
)_______ c( )(填“〉”。"<”或“=”)。
)(填“〉”。"<”或“=”)。
②Ir—Ru惰性电极吸附O2生成H2O2,其电极反应式为_______ 。
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效。广谱。快速。安全的杀菌消毒剂。目前已开发出用电解法制取C1O2的新工艺如图所示。

图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极的电极反应式为
(2)燃料电池因具有发电效率高。环境污染少等优点而备受人们关注。用于笔记本电脑的甲醇(CH3OH) 燃料电池示意图如下,b是

(3)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

①为了不影响H2O2的产量,需要向废氨水中加入适量HNO3调节溶液的pH约为5,则所得溶液中c(
 )
) )(填“〉”。"<”或“=”)。
)(填“〉”。"<”或“=”)。②Ir—Ru惰性电极吸附O2生成H2O2,其电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
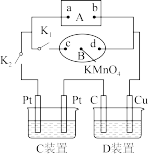
【推荐1】如图所示,A为新型高效的甲烷燃料电池,采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料、电解质溶液见图。
(1)甲烷燃料电池正极、负极的电极反应式分别为____ ;____ 。
(2)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向d端移动,则电源a端为___ 极,通电一段时间后,观察到滤纸c端出现的现象是_____ 。
(3)已知C装置中溶液为AgNO3溶液,D装置的溶液为Cu(NO3)2溶液,打开K1,关闭K2,通电一段时间后,D装置中Cu极的电极反应式为____ ,C装置中总反应的离子方程式为___ 。
(4)若C装置中AgNO3溶液足量,且溶液体积为1L,电解一段时间后,C装置中产生O2的体积为0.56 L(标准状况下),则电路通过的电子的物质的量为___ ,溶液的pH为___ (忽略溶液体积变化)。

(1)甲烷燃料电池正极、负极的电极反应式分别为
(2)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向d端移动,则电源a端为
(3)已知C装置中溶液为AgNO3溶液,D装置的溶液为Cu(NO3)2溶液,打开K1,关闭K2,通电一段时间后,D装置中Cu极的电极反应式为
(4)若C装置中AgNO3溶液足量,且溶液体积为1L,电解一段时间后,C装置中产生O2的体积为0.56 L(标准状况下),则电路通过的电子的物质的量为
您最近一年使用:0次
【推荐2】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________ (填字母)。

a.碳棒 b.锌板 c.铜板 d.钠块
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

①E为该燃料电池的________ (填“正”或“负”)极。F电极上的电极反应式为__________
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_________ 。
③0.4molCuSO4和0.4molNaCl溶于水,配成1L溶液,用该镁燃料电池用惰性电极进行电解,当一个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积为_______ L。
(3)如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

①b处应通入______ (填“CH4”或“O2”),a处电极上发生的电极反应式是_________________ ;
②电镀结束后,装置Ⅰ中溶液的pH_____________ ;(填写“变大”“变小”或“不变”)装置Ⅱ中Cu2+的物质的量浓度_______________ ;(填写“变大”“变小”或“不变”)
③在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8g,则装置Ⅰ中理论上消耗甲烷________ L(标况)。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

a.碳棒 b.锌板 c.铜板 d.钠块
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。

①E为该燃料电池的
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因
③0.4molCuSO4和0.4molNaCl溶于水,配成1L溶液,用该镁燃料电池用惰性电极进行电解,当一个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积为
(3)如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

①b处应通入
②电镀结束后,装置Ⅰ中溶液的pH
③在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8g,则装置Ⅰ中理论上消耗甲烷
您最近一年使用:0次