化合物甲由两种元素组成,为研究其组成和性质,进行如下实验:
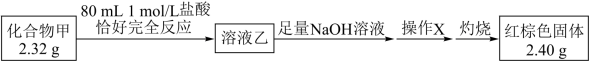
经分析甲的组成元素与红棕色固体相同,其中金属元素的单质能被磁铁吸引。
请回答:
(1)化合物甲的组成元素是_______ ,称取 2.32 g化合物甲应选择_______ 天平。
(2)化合物甲与盐酸反应的化学方程式是_______ 。
(3)溶液乙与铜反应在工业上可用于制作印刷电路板,其离子方程式是_______ 。
(4)上操作X的名称是_______ 、_______ 、_______ 。

经分析甲的组成元素与红棕色固体相同,其中金属元素的单质能被磁铁吸引。
请回答:
(1)化合物甲的组成元素是
(2)化合物甲与盐酸反应的化学方程式是
(3)溶液乙与铜反应在工业上可用于制作印刷电路板,其离子方程式是
(4)上操作X的名称是
20-21高一上·浙江绍兴·阶段练习 查看更多[1]
(已下线)【浙江新东方】在线化学 (21)
更新时间:2021-01-02 20:31:55
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A~H是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色。

请回答下列问题:
(1)元素B在周期表中的位置是______ ,C的电子式为______ ,H的结构式为______ 。
(2)反应①的化学方程式为_______________________ 。
(3)A与盐酸反应的离子方程式为___________________________ 。
(4)F溶液显________ (填“酸性”、“中性”或“碱性”),原因是____________________ (用离子方程式表示)。

请回答下列问题:
(1)元素B在周期表中的位置是
(2)反应①的化学方程式为
(3)A与盐酸反应的离子方程式为
(4)F溶液显
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某混合物X由Na2O、Fe2O3、Cu、SiO2中的一种或几种物质组成。某兴趣小组对X进行如下实验探究:

(1)混合物X中一定有_______ 。
(2)写出过程II中得到蓝色溶液所发生的离子反应方程式_______ ;________ 。
(3)混合物中铜的物质的量为___________ mol。

(1)混合物X中一定有
(2)写出过程II中得到蓝色溶液所发生的离子反应方程式
(3)混合物中铜的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组为了探究铁粉与水蒸气反应的产物,做了下面实验。资料:在不同温度下,铁粉与水蒸气反应的产物不同:
Fe +H2O FeO+H2;3Fe + 4H2O
FeO+H2;3Fe + 4H2O Fe3O4 + 4H2
Fe3O4 + 4H2
实验一:某兴趣小组用如图所示装置,使铁粉与过量水蒸气充分反应并检验固体产物的组成。

(1)实验过程中,应先点燃_______ (选填“酒精灯”或“酒精喷灯”);目的是________ ,装置中石棉绒的作用是________ 。
(2)若在实验中的某段时间内生成0.2g H2,则这段时间内参加反应的铁粉质量至少是_____ g。
实验二:铁粉完全反应后,兴趣小组对硬质玻璃管中生成的FeO和Fe3O4的质量进行测定,实验流程如图:
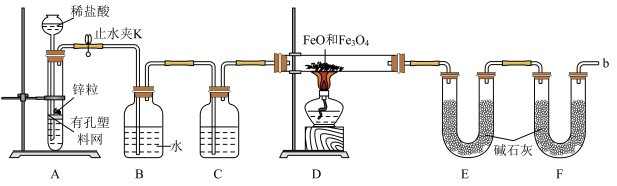
(1)实验前检查装置A的气密性:关闭止水夹K,从长颈漏斗向试管内加水,至长颈漏斗中管内的液面高于管外液面,静置一段时间,若液面高度差_____ ,则气密性良好。
(2)装置A中发生的反应方程式_______ 。
(3)为了安全,在点燃酒精灯之前,在F装置出口b处必须_______ 。
(4)装置C中所放试剂为______ ,装置B的作用是_______ 。
(5)干燥管E右边又连接干燥管F的目的是______ 。若无干燥管F,测得Fe3O4的质量将____ (填“偏大”、“偏小”或“无影响”)。
Fe +H2O
 FeO+H2;3Fe + 4H2O
FeO+H2;3Fe + 4H2O Fe3O4 + 4H2
Fe3O4 + 4H2实验一:某兴趣小组用如图所示装置,使铁粉与过量水蒸气充分反应并检验固体产物的组成。

(1)实验过程中,应先点燃
(2)若在实验中的某段时间内生成0.2g H2,则这段时间内参加反应的铁粉质量至少是
实验二:铁粉完全反应后,兴趣小组对硬质玻璃管中生成的FeO和Fe3O4的质量进行测定,实验流程如图:

(1)实验前检查装置A的气密性:关闭止水夹K,从长颈漏斗向试管内加水,至长颈漏斗中管内的液面高于管外液面,静置一段时间,若液面高度差
(2)装置A中发生的反应方程式
(3)为了安全,在点燃酒精灯之前,在F装置出口b处必须
(4)装置C中所放试剂为
(5)干燥管E右边又连接干燥管F的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是________ ,证明Fe3+存在的现象是________ 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式:________ 。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式:①________ ,④________ 。
(4)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为__ 。
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液
A.①③ B.③② C.③① D.①②③
(5)写出向⑤的溶液中通入⑥的离子方程式:____ 。
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的离子方程式:
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式:①
(4)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液
A.①③ B.③② C.③① D.①②③
(5)写出向⑤的溶液中通入⑥的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某工厂的工业废水中含有大量的FeSO4、较多的CuSO4和少量Na2SO4,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液)

(1)试剂①为______ ;操作a所需要的玻璃仪器为烧杯、玻璃棒、______ 。
(2)若取2mL溶液D加入试管中,然后滴加氢氧化钠溶液,产生的现象是______ ,此现象涉及氧化还原反应的化学方程式是______ 。
(3)为防止FeSO4溶液变质,应在溶液中加入少量______ ,其原因是______ (请用离子方程式解释原因)。
(4)回收的FeSO4经一系列变化后可制的一种新型绿色净水剂高铁酸钠(Na2FeO4)。其制备原理如下,请配平离子方程式:______ 。
_____Fe3++_____ClO-+_____OH-=_____FeO +______Cl-+______H2O
+______Cl-+______H2O

(1)试剂①为
(2)若取2mL溶液D加入试管中,然后滴加氢氧化钠溶液,产生的现象是
(3)为防止FeSO4溶液变质,应在溶液中加入少量
(4)回收的FeSO4经一系列变化后可制的一种新型绿色净水剂高铁酸钠(Na2FeO4)。其制备原理如下,请配平离子方程式:
_____Fe3++_____ClO-+_____OH-=_____FeO
 +______Cl-+______H2O
+______Cl-+______H2O
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:
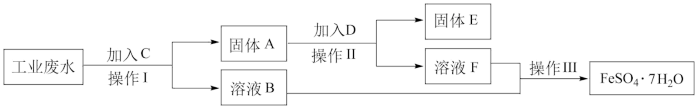
(1)操作Ⅱ的名称为______ 。
(2)加入的试剂D为______ ,加入试剂C后,所发生的离子反应方程式为______ 。
(3)操作Ⅲ为______ 、______ 、过滤、洗涤、干燥;
(4)由于硫酸亚铁溶液露置于空气中容易变质,请设计一个简单的实验方案验证硫酸亚铁溶液是否变质。(请写出必要的实验步骤、现象和结论)______ 。

(1)操作Ⅱ的名称为
(2)加入的试剂D为
(3)操作Ⅲ为
(4)由于硫酸亚铁溶液露置于空气中容易变质,请设计一个简单的实验方案验证硫酸亚铁溶液是否变质。(请写出必要的实验步骤、现象和结论)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫酸亚铁铵又称莫尔盐,是浅绿色晶体。它在空气中比一般亚铁盐稳定,是常用的Fe2+试剂。某实验小组利用工业废铁屑制取莫尔盐,并测定其组成,他们进行了以下实验。
Ⅰ.莫尔盐的制取

(把图中“一定实验步骤”换成“加热蒸发、浓缩结晶”)
请回答下列问题。
(1)废铁屑中含氧化铁,无需在制备前除去,理由是__________________ (用离子方程式回答),实验前都需将废铁屑放入碳酸钠溶液中煮沸,倾倒出液体,用水洗净铁屑。从以下仪器中选择组装,完成该操作必需的仪器有________ (填编号)。
①铁架台 ②玻璃棒 ③广口瓶 ④石棉网 ⑤烧杯 ⑥漏斗 ⑦酒精灯
(2)步骤2中加热方式___________ (填“直接加热”﹑“水浴加热”或“沙浴”);必须在铁屑少量剩余时,进行热过滤,其原因是___________________________________ 。
II.莫尔盐组成的测定
①将摩尔盐低温烘干后,称取7.84 g加热至100℃失去结晶水,质量变为5.68 g。
②选择下图所示的部分装置连接起来,检查气密性后,将上述5.68g固体放入A装置的锥形瓶中,再向锥形瓶中加入足量NaOH浓溶液,充分吸收产生的气体并测出气体质量为0.68 g。
③向A中加入适量3%的H 2 O 2溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后,测得其质量为1.6 g。

根据上述实验回答下列问题。
(3)步骤②中,选择的装置是A接_______ 接_______ (填代号),A装置中未使用分液漏斗的理由是______________ 。
(4)向锥形瓶中加入NaOH溶液的操作方法是_______ ;吸收A中产生的气体所用试剂应是_______ 。实验小组的同学为保证A中产生的气体被完全吸收以准确测量其质量,他们在A中反应停止后再进行的操作是______________ 。
(5)根据上述实验数据计算,摩尔盐中 =
=_______ 。
Ⅰ.莫尔盐的制取

(把图中“一定实验步骤”换成“加热蒸发、浓缩结晶”)
请回答下列问题。
(1)废铁屑中含氧化铁,无需在制备前除去,理由是
①铁架台 ②玻璃棒 ③广口瓶 ④石棉网 ⑤烧杯 ⑥漏斗 ⑦酒精灯
(2)步骤2中加热方式
II.莫尔盐组成的测定
①将摩尔盐低温烘干后,称取7.84 g加热至100℃失去结晶水,质量变为5.68 g。
②选择下图所示的部分装置连接起来,检查气密性后,将上述5.68g固体放入A装置的锥形瓶中,再向锥形瓶中加入足量NaOH浓溶液,充分吸收产生的气体并测出气体质量为0.68 g。
③向A中加入适量3%的H 2 O 2溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后,测得其质量为1.6 g。

根据上述实验回答下列问题。
(3)步骤②中,选择的装置是A接
(4)向锥形瓶中加入NaOH溶液的操作方法是
(5)根据上述实验数据计算,摩尔盐中
 =
=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】硫酸铈铵[(NH4)4Ce(SO4)4]是分析化学常用的滴定剂。以氟碳铈矿(含CeFCO3、BaF2、SiO2等)为原料制备硫酸铈铵的工艺流程如图所示。

已知部分信息如下:
①Ce3+在空气中易被氧化为Ce4+。
②“沉铈”时发生的反应之一: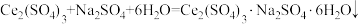 。
。
回答下列问题:
(1)CeFCO3中电负性最大的是___________ (填元素符号),画出H2O的VSEPR模型:___________ 。
(2)“焙烧”中常采用高压空气、逆流操作(空气从焙烧炉下部通入,矿粉从中上部加入),这样操作的目的是___________ 。
(3)“酸浸”中,铈浸出率与温度的关系如下左图所示,铈浸出率与硫酸浓度的关系如下右图所示。工业生产应选择的适宜条件是___________ 。

(4)“沉铈”时,硫脲作___________ (填“还原剂”或“氧化剂”)。
(5)“溶解”时,为防止Ce3+被氧化,可以加入___________ (填标号)。
a.KMnO4 b.NaClO c.CH3CHO
(6)在有机合成中,硫酸铈铵常作合成丙酸异戊酯的催化剂。其他条件相同,酯产率与催化剂质量的关系如图所示。工业生产中,选择的最佳催化剂质量为___________ g。

(7)测定产品纯度。称取ωg产品溶于水,配制成250mL溶液,准确量取25.00mL配制的溶液于锥形瓶中,加入VmL0.10mol·L-1Na2Fe(SO4)2溶液,恰好完全反应。该产品纯度为___________ %。(杂质不参与反应,滴定反应为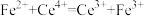 )
)

已知部分信息如下:
①Ce3+在空气中易被氧化为Ce4+。
②“沉铈”时发生的反应之一:
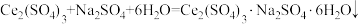 。
。回答下列问题:
(1)CeFCO3中电负性最大的是
(2)“焙烧”中常采用高压空气、逆流操作(空气从焙烧炉下部通入,矿粉从中上部加入),这样操作的目的是
(3)“酸浸”中,铈浸出率与温度的关系如下左图所示,铈浸出率与硫酸浓度的关系如下右图所示。工业生产应选择的适宜条件是

(4)“沉铈”时,硫脲作
(5)“溶解”时,为防止Ce3+被氧化,可以加入
a.KMnO4 b.NaClO c.CH3CHO
(6)在有机合成中,硫酸铈铵常作合成丙酸异戊酯的催化剂。其他条件相同,酯产率与催化剂质量的关系如图所示。工业生产中,选择的最佳催化剂质量为

(7)测定产品纯度。称取ωg产品溶于水,配制成250mL溶液,准确量取25.00mL配制的溶液于锥形瓶中,加入VmL0.10mol·L-1Na2Fe(SO4)2溶液,恰好完全反应。该产品纯度为
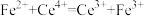 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业上纳米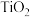 的制备过程是以
的制备过程是以 为载体,用
为载体,用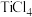 和水蒸气反应生成
和水蒸气反应生成 ,再控制温度生成纳米
,再控制温度生成纳米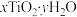 ,测定产物
,测定产物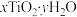 组成的方法如下:
组成的方法如下:
步骤一:取样品2.100g用稀硫酸充分溶解得到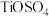 溶液,再用足量铝将
溶液,再用足量铝将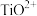 还原为
还原为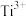 ,过滤并洗涤,将所得滤液和洗涤液混合并注入250mL容量瓶,定容得到待测液。
,过滤并洗涤,将所得滤液和洗涤液混合并注入250mL容量瓶,定容得到待测液。
步骤二:取待测液于锥形瓶中,加入几滴指示剂,用0.1mol/L的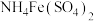 标准溶液滴定,将
标准溶液滴定,将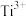 氧化为
氧化为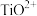 ,三次滴定测得数据记录如下:
,三次滴定测得数据记录如下:
回答下列问题:
(1)若对步骤一所得的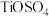 溶液加水稀释,溶液中会产生少量偏钛酸(
溶液加水稀释,溶液中会产生少量偏钛酸(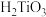 )沉淀,写出该反应的离子方程式
)沉淀,写出该反应的离子方程式___________ 。
(2)已知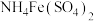 溶液显酸性,滴定时,将标准溶液注入
溶液显酸性,滴定时,将标准溶液注入___________ (填“酸”或“碱”)式滴定管中。
(3)上述滴定实验中,可选择___________ 为指示剂,判断到达滴定终点的方法是___________ 。
(4)下列关于滴定分析的操作,错误的是___________ 。
A.滴定时要适当控制滴定速率
B.用量筒量取25.00mL待测液转移至锥形瓶
C.滴定时应一直观察滴定管中溶液体积的变化
D.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
E.在接近终点时,滴加药品应慢慢控制滴定管,使滴定管尖嘴悬挂一滴液体,用锥形瓶内壁将其靠下,并用蒸馏水将其冲入锥形瓶内。
(5)通过分析、计算,该样品的组成为___________ (写出计算过程);若滴定前滴定管尖端有气泡,滴定过程中气泡消失,则测得 比实际值
比实际值___________ (填“偏大”、“偏小”或“无影响”)。
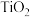 的制备过程是以
的制备过程是以 为载体,用
为载体,用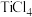 和水蒸气反应生成
和水蒸气反应生成 ,再控制温度生成纳米
,再控制温度生成纳米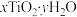 ,测定产物
,测定产物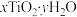 组成的方法如下:
组成的方法如下:步骤一:取样品2.100g用稀硫酸充分溶解得到
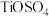 溶液,再用足量铝将
溶液,再用足量铝将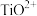 还原为
还原为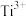 ,过滤并洗涤,将所得滤液和洗涤液混合并注入250mL容量瓶,定容得到待测液。
,过滤并洗涤,将所得滤液和洗涤液混合并注入250mL容量瓶,定容得到待测液。步骤二:取待测液于锥形瓶中,加入几滴指示剂,用0.1mol/L的
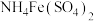 标准溶液滴定,将
标准溶液滴定,将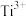 氧化为
氧化为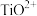 ,三次滴定测得数据记录如下:
,三次滴定测得数据记录如下:| 实验编号 | 待测溶液的体积/mL | 滴定前标准液的体积读数/mL | 滴定后标准液的体积读数/mL |
| 1 | 25.00 | 0.20 | 24.22 |
| 2 | 25.00 | 1.21 | 29.21 |
| 3 | 25.00 | 1.50 | 25.48 |
(1)若对步骤一所得的
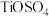 溶液加水稀释,溶液中会产生少量偏钛酸(
溶液加水稀释,溶液中会产生少量偏钛酸(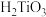 )沉淀,写出该反应的离子方程式
)沉淀,写出该反应的离子方程式(2)已知
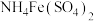 溶液显酸性,滴定时,将标准溶液注入
溶液显酸性,滴定时,将标准溶液注入(3)上述滴定实验中,可选择
(4)下列关于滴定分析的操作,错误的是
A.滴定时要适当控制滴定速率
B.用量筒量取25.00mL待测液转移至锥形瓶
C.滴定时应一直观察滴定管中溶液体积的变化
D.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
E.在接近终点时,滴加药品应慢慢控制滴定管,使滴定管尖嘴悬挂一滴液体,用锥形瓶内壁将其靠下,并用蒸馏水将其冲入锥形瓶内。
(5)通过分析、计算,该样品的组成为
 比实际值
比实际值
您最近一年使用:0次



