(1)50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
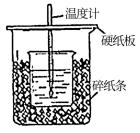
①从实验装置上看,图中尚缺少的一种玻璃用品是_______ 。
②烧杯间填满碎纸条的作用是_______ 。
③大烧杯上如不盖硬纸板,求得的中和热数值将_______ (填“偏大”“偏小”或“无影响”)。
(2)酸碱中和滴定是中学化学常见实验。
某学校化学课外小组用0.2000mol·L-1盐酸滴定未知浓度的氢氧化钠溶液,选择甲基橙作指示剂,试回答下列问题。
①滴定过程中,眼睛应注视_______ 。
②滴定终点时的现象:______________ 。
③根据下表数据,计算被测烧碱溶液的物质的量浓度是________ mol·L-1.(保留四位有效数字)
④下列实验操作对滴定结果产生什么影响(填“偏高”、“偏低”或“无影响”)?
a.观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果_______ 。
b.若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果_______ 。

①从实验装置上看,图中尚缺少的一种玻璃用品是
②烧杯间填满碎纸条的作用是
③大烧杯上如不盖硬纸板,求得的中和热数值将
(2)酸碱中和滴定是中学化学常见实验。
某学校化学课外小组用0.2000mol·L-1盐酸滴定未知浓度的氢氧化钠溶液,选择甲基橙作指示剂,试回答下列问题。
①滴定过程中,眼睛应注视
②滴定终点时的现象:
③根据下表数据,计算被测烧碱溶液的物质的量浓度是
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
a.观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果
b.若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果
更新时间:2021-01-09 20:04:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组用0.50mol/L NaOH和0.50mol/L  溶液进行中和热的测定。
溶液进行中和热的测定。
Ⅰ.配制250mL 0.50mol/L NaOH溶液
(1)需要称量NaOH固体___________ g。
(2)配制NaOH溶液所需要的仪器:托盘天平、药匙、烧杯、玻璃棒、量筒、___________ 。
Ⅱ.测定中和热的实验装置如图所示。
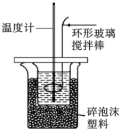
(3)取50mL NaOH溶液和30mL 溶液进行实验,实验数据如表所示。
溶液进行实验,实验数据如表所示。
① 溶液与NaOH溶液混合均匀的正确操作是
溶液与NaOH溶液混合均匀的正确操作是___________ (填字母)。
a.用温度计小心搅拌 b.揭开硬纸板用玻璃棒搅拌
c.轻轻地振荡烧杯 d.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
②填写表中的空白。___________
③近似认为0.50mol/L NaOH溶液和0.50mol/L 溶液的密度都是1
溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容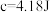 /(g·℃)。则测得中和反应的反应热
/(g·℃)。则测得中和反应的反应热 =
=___________ kJ/mol。(结果精确到0.1)
④上述实验测得结果与理论值产生偏差的原因可能是___________ (填字母)。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把溶液倒入盛有 溶液的小烧杯中
溶液的小烧杯中
D.用温度计测定NaOH溶液的起始温度后直接测定 溶液的温度
溶液的温度
 溶液进行中和热的测定。
溶液进行中和热的测定。Ⅰ.配制250mL 0.50mol/L NaOH溶液
(1)需要称量NaOH固体
(2)配制NaOH溶液所需要的仪器:托盘天平、药匙、烧杯、玻璃棒、量筒、
Ⅱ.测定中和热的实验装置如图所示。

(3)取50mL NaOH溶液和30mL
 溶液进行实验,实验数据如表所示。
溶液进行实验,实验数据如表所示。| 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 ( 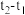 )/℃ )/℃ | ||
 溶液 溶液 | NaOH溶液 | 平均值 | |||
| 1 | 27.0 | 27.4 | 27.2 | 31.2 | ___________ |
| 2 | 25.9 | 25.9 | 25.9 | 31.5 | |
| 3 | 26.4 | 26.2 | 26.3 | 30.5 | |
 溶液与NaOH溶液混合均匀的正确操作是
溶液与NaOH溶液混合均匀的正确操作是a.用温度计小心搅拌 b.揭开硬纸板用玻璃棒搅拌
c.轻轻地振荡烧杯 d.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
②填写表中的空白。
③近似认为0.50mol/L NaOH溶液和0.50mol/L
 溶液的密度都是1
溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容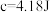 /(g·℃)。则测得中和反应的反应热
/(g·℃)。则测得中和反应的反应热 =
=④上述实验测得结果与理论值产生偏差的原因可能是
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把溶液倒入盛有
 溶液的小烧杯中
溶液的小烧杯中D.用温度计测定NaOH溶液的起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】利用如图所示装置测定中和热的实验步骤如下:

 用量筒量取100mL 0.50
用量筒量取100mL 0.50 盐酸倒入小烧杯中,测出盐酸温度;
盐酸倒入小烧杯中,测出盐酸温度;
 用另一量筒量取100mL 0.55
用另一量筒量取100mL 0.55 NaOH溶液,并用同一温度计测出其温度;
NaOH溶液,并用同一温度计测出其温度;
 将
将 和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)仪器 的名称是
的名称是___________ ,a的材质能否用铜丝代替?___________  填“能”或“不能”
填“能”或“不能” ,其原因是:
,其原因是:___________ 。烧杯间填满碎泡沫塑料的作用是___________ 。
(2)配制100mL 0.55mol/L的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及___________ ,___________ 。
(3)倒入NaOH和盐酸溶液的正确操作是___________ 填字母
填字母 。
。
(4)假设盐酸和氢氧化钠溶液的密度都是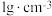 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容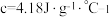 。为了计算中和热,某学生实验记录数据如下:
。为了计算中和热,某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热
___________  结果保留一位小数
结果保留一位小数 。
。
(5)某同学利用上述装置做甲组实验,测得中和热的数值偏低,试分析可能的原因___________。
(6)实验中改用80mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量___________  填“相等”“不相等”
填“相等”“不相等” 。反应过程中NaOH溶液的浓度为0.55
。反应过程中NaOH溶液的浓度为0.55 不是0.50
不是0.50 的原因是
的原因是___________ 。用同浓度的稀氨水代替稀氢氧化钠溶液和稀盐酸反应,所测ΔH ___________ 。 填“偏大”、“偏小”或“不变”
填“偏大”、“偏小”或“不变”

 用量筒量取100mL 0.50
用量筒量取100mL 0.50 盐酸倒入小烧杯中,测出盐酸温度;
盐酸倒入小烧杯中,测出盐酸温度; 用另一量筒量取100mL 0.55
用另一量筒量取100mL 0.55 NaOH溶液,并用同一温度计测出其温度;
NaOH溶液,并用同一温度计测出其温度; 将
将 和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)仪器
 的名称是
的名称是 填“能”或“不能”
填“能”或“不能” ,其原因是:
,其原因是:(2)配制100mL 0.55mol/L的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及
(3)倒入NaOH和盐酸溶液的正确操作是___________
 填字母
填字母 。
。| A.沿玻璃棒缓慢倒入 | B.分三次倒入 | C.一次迅速倒入 | D.一边搅拌一边一次滴入 |
(4)假设盐酸和氢氧化钠溶液的密度都是
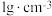 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容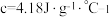 。为了计算中和热,某学生实验记录数据如下:
。为了计算中和热,某学生实验记录数据如下:| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
 | 20.0 | 20.2 | 23.2 |
 | 20.2 | 20.4 | 23.4 |
 | 20.3 | 20.5 | 25.6 |

 结果保留一位小数
结果保留一位小数 。
。(5)某同学利用上述装置做甲组实验,测得中和热的数值偏低,试分析可能的原因___________。
| A.测量完盐酸的温度再次测最NaOH溶液温度时,温度计上残留的酸液未用水冲洗干净。 |
| B.做本实验的当天室温很低 |
| C.大小烧杯口不平齐,小烧杯口未接触泡沫塑料板 |
| D.NaOH溶液沿玻璃棒缓慢倒入 |
(6)实验中改用80mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
 填“相等”“不相等”
填“相等”“不相等” 。反应过程中NaOH溶液的浓度为0.55
。反应过程中NaOH溶液的浓度为0.55 不是0.50
不是0.50 的原因是
的原因是 填“偏大”、“偏小”或“不变”
填“偏大”、“偏小”或“不变”
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为测定某H2C2O4溶液的浓度,取25.00mL该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L KMnO4标准溶液滴定。
(1)滴定实验反应的离子方程式为:__ MnO4-+___ H2C2O4+___ H+=___ Mn2++ 8H2O+___ ( )
(2)滴定时,KMnO4溶液应装在_______________ (填“酸式滴定管”或“碱式滴定管”)中,达到滴定终点的现象为 _________________________________ 。
(3)若滴定时,没用标准液洗涤滴定管,会使得草酸溶液的物质的量浓度_______ (填“偏高”、“偏低”、“无影响”)
(4)取0.50 mol·L-1 H2SO4溶液30 mL与同浓度的NaOH溶液50 mL做中和热的实验,发现|△H|<57.3 kJ·mol-1,产生此偏差的原因可能是______ (填字母)。
a.实验装置保温、隔热效果差
b.用量身量取NaOH溶液的体积时仰视读数
c.一次性把NaOH溶液倒入盛有H2SO4溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(1)滴定实验反应的离子方程式为:
(2)滴定时,KMnO4溶液应装在
(3)若滴定时,没用标准液洗涤滴定管,会使得草酸溶液的物质的量浓度
(4)取0.50 mol·L-1 H2SO4溶液30 mL与同浓度的NaOH溶液50 mL做中和热的实验,发现|△H|<57.3 kJ·mol-1,产生此偏差的原因可能是
a.实验装置保温、隔热效果差
b.用量身量取NaOH溶液的体积时仰视读数
c.一次性把NaOH溶液倒入盛有H2SO4溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学用Ba(OH)2晶体配制Ba(OH)2溶液,并用盐酸测定Ba(OH)2溶液的物质的量浓度。
(1)配制250mL 0.1 mol•L−1Ba(OH)2溶液:准确称取:Ba(OH)2·8H2O试样w克,置于烧杯中,加适量蒸馏水,溶解,将溶液转入________________ 中,洗涤,____________ ,摇匀。
(2)准确量取配制的Ba(OH)2溶液25.00mL于锥形瓶中,滴加酚酞指示剂,将________ (填“0.02”、“0.05”、 “0.25”或“1.50”) mol•L−1盐酸装入50mL_________ (填 “酸”或“碱”)式滴定管,滴定至终点,记录数据。重复滴定2次,平均消耗盐酸19.80mL。
(3)测得Ba(OH)2溶液溶质的物质的量浓度___________ (填 “>” 或“<”)0.1 mol•L−1。
(4)下列有关说法正确的是__________________ 。
A.滴定过程中,眼睛要时刻注视滴定管中液面的变化
B.锥形瓶用水洗涤后,再用待测的Ba(OH)2溶液润洗
C.滴定前读数准确,滴定完毕俯视读数,测定结果偏高
D.当滴入半滴盐酸后,溶液变无色且半分钟内不恢复,停止滴定
(1)配制250mL 0.1 mol•L−1Ba(OH)2溶液:准确称取:Ba(OH)2·8H2O试样w克,置于烧杯中,加适量蒸馏水,溶解,将溶液转入
(2)准确量取配制的Ba(OH)2溶液25.00mL于锥形瓶中,滴加酚酞指示剂,将
(3)测得Ba(OH)2溶液溶质的物质的量浓度
(4)下列有关说法正确的是
A.滴定过程中,眼睛要时刻注视滴定管中液面的变化
B.锥形瓶用水洗涤后,再用待测的Ba(OH)2溶液润洗
C.滴定前读数准确,滴定完毕俯视读数,测定结果偏高
D.当滴入半滴盐酸后,溶液变无色且半分钟内不恢复,停止滴定
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】0128应用纳米技术制备的纳米金属燃料已应用到社会生活和高科技领域.一些原子序数较小的金属、非金属和常用燃料的单位质量燃烧热的比较如图所示。请回答下列问题:
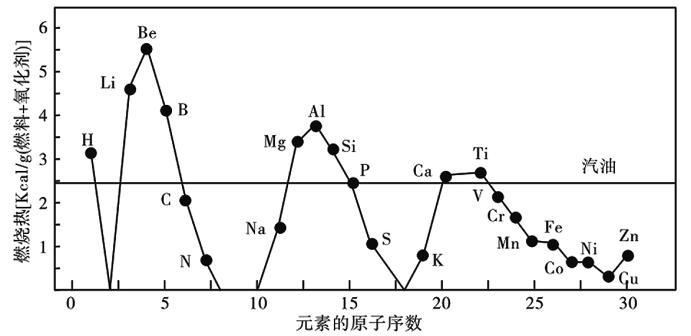
(1)结合元素在地壳中的含量,在单位质量燃烧热大于汽油和氢单质的物质中,最具发展潜力的两种新型燃料可以是_______ (填写元素符号)。这些物质作为燃料使用,除具有高燃烧热值外,还具有的优点是____ (填一项)。
(2)Be粉和MnO2粉末在高温下可以反应(类似铝热反应),每消耗1gBe放出akJ热量,请写出该反应的热化学方程式_________ 。
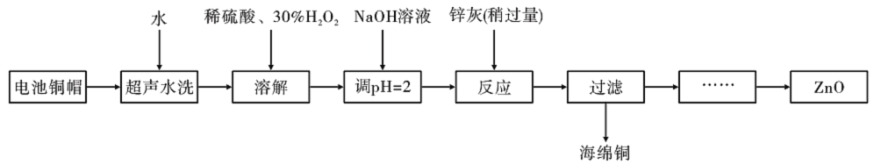
(3)废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收Cu并制备ZnO的部分实验过程如图:
①溶解铜帽时加入H2O2的目的是_________ (用化学方程式表示)。
②铜帽溶解完全后,需将溶液中过量的H2O2除去。除去H2O2的简便方法是___ 。
为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式为:2Cu2++4I-=2CuI(白色)↓+I2 2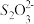 +I2=I-+
+I2=I-+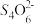 。
。
③滴定选用的指示剂为_____ ,滴定终点观察到的现象为_____ 。
④若滴定前溶液中的H2O2没有除尽,所测定的Cu2+含量将会______ (填“偏高”、“偏低”或“不变”)。

(1)结合元素在地壳中的含量,在单位质量燃烧热大于汽油和氢单质的物质中,最具发展潜力的两种新型燃料可以是
(2)Be粉和MnO2粉末在高温下可以反应(类似铝热反应),每消耗1gBe放出akJ热量,请写出该反应的热化学方程式
(3)废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收Cu并制备ZnO的部分实验过程如图:

①溶解铜帽时加入H2O2的目的是
②铜帽溶解完全后,需将溶液中过量的H2O2除去。除去H2O2的简便方法是
为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式为:2Cu2++4I-=2CuI(白色)↓+I2 2
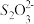 +I2=I-+
+I2=I-+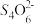 。
。③滴定选用的指示剂为
④若滴定前溶液中的H2O2没有除尽,所测定的Cu2+含量将会
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某种胃药的有效成分为碳酸钙,某实验小组为测定其中碳酸钙的含量,取10粒药片(0.1g/粒)研碎后溶解,加入25.00mL1.0mol/L的稀盐酸反应,最后用1.0mol/LNaOH溶液中和过量的盐酸,测定所消耗的NaOH溶液体积如下:
(1)配制100mL1.0mol/L的稀盐酸,需要2.5mol/L的盐酸的体积为___ mL。
(2)药片中碳酸钙的质量分数为___ 。
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
(2)药片中碳酸钙的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】柠檬含有丰富的营养成分,具有辅助生津开胃、化痰止咳等功效。但需适量食用,因为柠檬中含有比较多的酸性物质,如果长期大量食用可能会导致胃酸分泌过多,引起腹痛反酸等不适症状。某同学为测定柠檬的酸度[规定:中和1克柠檬中的酸性物质所需的氢氧化钾(KOH)的毫克数],进行了下列实验:称取ag鲜柠檬,切成小块后用榨汁机榨取汁液,过滤后取滤液,稀释成250mL溶液待用用滴定管取出25.00mL待测液于锥形瓶中,加入几滴指示剂,然后用0.1000 mol·L-1KOH 标准溶液滴定,平行滴定3次,所测得的实验数据如下表:
请回答下列问题:
(1)在实验室完成过滤操作所需的玻璃仪器主要有烧杯、______ 。
(2)实验中取用待测液时可用图 1 中的_____ (填“a”或“b”)量取;若某同学量取待测液时,滴定管读数如图2所示,则量取的待测液体积为_____ mL。
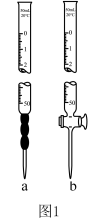
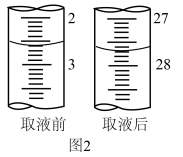
(3)本实验可选用____ 作指示剂,滴定过程中眼睛要注视_______ ,到达滴定终点时的现象是______ 。
(4)将以下操作所导致的测定结果(填“偏大”、“偏小”或“无影响”)填写在对应的横线上
①在加待测液前锥形瓶用少量水洗涤____ 。
②到达滴定终点时俯视读数____ 。
③碱式滴定管量取 KOH 溶液时,未进行润洗____ 。
| 实验编号 | 1 | 2 | 3 |
| 消耗标准溶液体积/mL | 20.05 | 19.95 | 20.00 |
(1)在实验室完成过滤操作所需的玻璃仪器主要有烧杯、
(2)实验中取用待测液时可用图 1 中的


(3)本实验可选用
(4)将以下操作所导致的测定结果(填“偏大”、“偏小”或“无影响”)填写在对应的横线上
①在加待测液前锥形瓶用少量水洗涤
②到达滴定终点时俯视读数
③碱式滴定管量取 KOH 溶液时,未进行润洗
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为_______ mol·L-1
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol·L-1的稀盐酸。
①该学生需要量取_______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填表示“偏大”、“偏小”或“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面_______
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_______
(4)①假设该同学成功配制了0.400mol·L-1的盐酸,他又用该盐酸中和1L0.0100mol·L-1的NaOH溶液,则该同学需取_______ mL盐酸。如果他要配制500ml0.100mol·L-1NaOH溶液,他要用托盘天平称量_______ gNaOH固体。
②假设该同学用新配制的盐酸中和含0.4gNaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是_______ 。(填字母)
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19 g·cm-3 HCl的质量分数:36.5%) |
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填表示“偏大”、“偏小”或“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(4)①假设该同学成功配制了0.400mol·L-1的盐酸,他又用该盐酸中和1L0.0100mol·L-1的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4gNaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氧化还原滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001mol·L-1酸性KMnO4溶液滴定未知浓度的无色NaHSO3溶液。反应的离子方程式为2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O
请完成下列问题:
(1)实验中用___ (填“酸”或“碱”)式滴定管盛装酸性KMnO4溶液;
(2)本实验___ (填“需要”或“不需要”)使用指示剂,滴定终点的现象是___ ;
(3)①滴定前平视液面,刻度为amL,滴定后俯视刻度为bmL,则根据(b−a)mL计算得到的待测液浓度值会___ (填“偏小”“偏大”或“不变”);
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测液浓度值会___ (填“偏小”“偏大”或“不变”)。
请完成下列问题:
(1)实验中用
(2)本实验
(3)①滴定前平视液面,刻度为amL,滴定后俯视刻度为bmL,则根据(b−a)mL计算得到的待测液浓度值会
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测液浓度值会
您最近一年使用:0次



