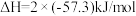1g氨气完全分解为氮气、氢气时,吸收2.72kJ的热量,下列热化学方程式正确的是
①N2(g)+3H2(g)=2NH3(g) △H=﹣46.2kJ/mol
②N2(g)+3H2(g)=2NH3(g) △H=﹣92.4kJ/mol
③NH3(g)= N2(g)+
N2(g)+ H2(g) △H=+46.2kJ/mol
H2(g) △H=+46.2kJ/mol
④2NH3(g)=N2(g)+3H2(g) △H=﹣92.4kJ/mol。
①N2(g)+3H2(g)=2NH3(g) △H=﹣46.2kJ/mol
②N2(g)+3H2(g)=2NH3(g) △H=﹣92.4kJ/mol
③NH3(g)=
 N2(g)+
N2(g)+ H2(g) △H=+46.2kJ/mol
H2(g) △H=+46.2kJ/mol④2NH3(g)=N2(g)+3H2(g) △H=﹣92.4kJ/mol。
| A.全部 | B.①②③ | C.①② | D.②③ |
20-21高二上·陕西宝鸡·期中 查看更多[4]
陕西省宝鸡市渭滨中学2020-2021学年度高二上学期期中考试化学试题(已下线)1.1.2 热化学方程式 燃烧热(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第02讲 热化学方程式与燃烧热(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)河南省平顶山许昌济源洛阳2023-2024学年高三上学期第一次质量检测化学试题
更新时间:2021-01-12 00:05:41
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关能量变化的叙述正确的是
| A.NaHCO3与盐酸反应属于放热反应 |
| B.C(石墨,s)=C(金刚石,s)ΔH>0,说明石墨比金刚石稳定 |
| C.需要加热才能进行的反应一定是吸热反应 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于盖斯定律描述不正确的是
| A.化学反应的反应热不仅与反应体系的始态和终态有关,也与反应的途径有关 |
| B.盖斯定律遵守能量守恒定律 |
| C.利用盖斯定律可间接计算通过实验难测定的反应的反应热 |
| D.利用盖斯定律可以计算有副反应发生的反应的反应热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列说法正确的是( )
| A.在稀溶液中,1 mol H2SO4(aq)与1 mol Ba(OH)2(aq)完全中和所放出的热量为中和热 |
| B.表明参加反应物质的量和反应热的关系的化学方程式叫做热化学方程式 |
| C.凡是在加热或点燃条件下进行的反应都是吸热反应 |
| D.101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】分析表中的四个热化学方程式,判断氢气和丙烷的标准燃烧热分别是
| “嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ∙mol-1 ②2H2(l)+O2(l)=2H2O(g) ΔH=-482.6kJ∙mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷(C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g) ΔH=-2013.8kJ∙mol-1 ④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2221.5kJ∙mol-1 |
| A.-571.6kJ∙mol-1,-2221.5kJ∙mol-1 | B.-285.5kJ∙mol-1,-2013.8kJ∙mol-1 |
| C.-285.8kJ∙mol-1,-2221.5kJ∙mol-1 | D.-241.3kJ∙mol-1,-2013.8kJ∙mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】将2.0 g H2(g)在O2(g)中完全燃烧,生成H2O(g),放出热量Q kJ。则下列说法正确的是
| A.若使用H2(l),则放出热量大于Q kJ | B.若生成H2O(l),则放出热量大于Q kJ |
| C.若使用O2(s),则放出热量大于Q kJ | D.电解18.0 g液态水,需要吸收Q kJ的热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】N2H4是一种高效清洁的燃料。0.5molN2H4(g)完全燃烧生成氮气和气态水时,放出267kJ热量。则下列热化学方程式中正确的是
A. N2H4(g)+ N2H4(g)+ O2(g)═ O2(g)═ N2(g)+H2O(g)△H=+267kJ•mol-1 N2(g)+H2O(g)△H=+267kJ•mol-1 |
| B.N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=+534kJ•mol-1 |
| C.N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ•mol-1 |
| D.N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-133kJ•mol-1 |
您最近一年使用:0次


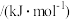
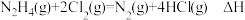 ,下列推断正确的是
,下列推断正确的是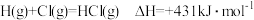
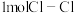 键吸收能量比断裂
键吸收能量比断裂 键多
键多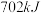
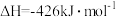
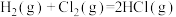
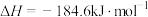 ,则每生成1molHCl,放出的热量为184.6kJ
,则每生成1molHCl,放出的热量为184.6kJ
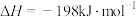 ,则在一定条件下,
,则在一定条件下, 和
和 充分反应后,释放的热量为198kJ
充分反应后,释放的热量为198kJ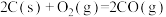
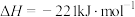 ,则C的燃烧热为
,则C的燃烧热为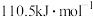
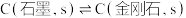
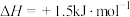 ,可判断石墨比金刚石更稳定
,可判断石墨比金刚石更稳定 燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热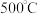 、
、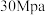 下,将
下,将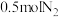 和
和 置于密闭的容器中充分反应生成
置于密闭的容器中充分反应生成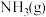 ,放热
,放热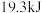 ,其热化学方程式为:
,其热化学方程式为: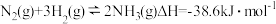
 在光照和点燃条件的
在光照和点燃条件的 相同
相同 和
和 反应的中和热
反应的中和热 ,则
,则 和
和 反应的中和热
反应的中和热