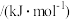已知几种化学键的键能和热化学方程式如下:
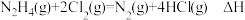 ,下列推断正确的是
,下列推断正确的是
化学键 | H-N | N-N | Cl-Cl |
| H-Cl |
键能 | 391 | 193 | 243 | 945 | 431 |
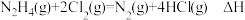 ,下列推断正确的是
,下列推断正确的是A.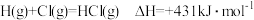 |
B.断裂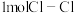 键吸收能量比断裂 键吸收能量比断裂 键多 键多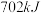 |
C.上述反应中,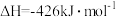 |
| D.上述反应中,断裂了极性键和非极性键,只形成了极性键 |
更新时间:2021-02-07 13:52:30
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】有关化学键的键能数据如表所示:
碳的燃烧热ΔH=-395 kJ·mol-1,假设单质碳中只存在C—C键且基本结构单元为正四面体,则x的值为
| 化学键 | C=O | O=O | C—C |
| 键能/kJ·mol-1 | x | 498.8 | 345.6 |
| A.619.7 | B.1 239.4 | C.792.5 | D.1 138.1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知1mol二氧化硅晶体中化学键的数目为4NA,有关键能数据如表所示:
又知Si(s)+O2(g)=SiO2(s) ∆H=-989.2kJ·mol-1,则1molSi中Si-Si键的数目为
| 化学键 | Si-O | O=O | Si-Si |
| 键能/(kJ·mol-1) | 460 | 498.8 | 176 |
又知Si(s)+O2(g)=SiO2(s) ∆H=-989.2kJ·mol-1,则1molSi中Si-Si键的数目为
| A.4NA | B.3NA | C.2NA | D.NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】法匹拉韦是治疗新冠肺炎的种药物,其结构简式如图所示,下列说法错误的是
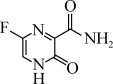

| A.该分子中N、O、F的第一电离能由大到小的顺序为F>N>O |
| B.该分子中C-H键的键能大于N-H键的键能 |
| C.该分子中所有C原子都为sp2杂化 |
| D.该分子可形成分子间氢键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知C3N4晶体很可能具有比金刚石更大的硬度,且原子间以单键结合。下列有关C3N4晶体的说法中正确的是( )
| A.C3N4晶体是分子晶体 |
| B.C3N4晶体中C—N键的键长比金刚石中的C—C键的键长长 |
| C.C3N4晶体中C、N原子个数之比为4∶3 |
| D.C3N4晶体中粒子间通过共价键相结合 |
您最近一年使用:0次