SF6是一种优良的气体绝缘材料,分子结构中只存在S—F键。发生反应的热化学方程式为:S(s)+ 3F2(g) = SF6(g) ΔH= -1220 kJ/mol。已知:1mol S(s)转化为气态硫原子吸收能量280kJ,断裂1mol F—F键需吸收的能量为160 kJ,则断裂1mol S—F键需吸收的能量为
| A.76.67 kJ | B.276.67 kJ |
| C.130 kJ | D.330 kJ |
12-13高二下·福建莆田·阶段练习 查看更多[5]
四川省成都外国语学校2021-2022学年高二上学期期中化学试题【全国百强校】河南省林州市第一中学2018-2019学年高二上学期9月月考化学试题(已下线)2013届北京市朝阳区高三上学期期末考试化学试卷(已下线)2012-2013学年福建省莆田一中高二下学期第一学段考试化学试卷福建省莆田市第一中学2016-2017学年高二下学期期中考试化学试题
更新时间:2017-05-11 22:28:37
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】N4分子结构如图所示,已知断裂1molN-N键吸收167kJ热量,生成1molN≡N键放出942kJ热量。根据以上信息和数据,则由N2生成1mol气态N4的ΔH为


| A.+882kJ/mol | B.+441kJ/mol | C.-882kJ/mol | D.-441kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】反应CO(g)+ 2H2(g)=CH3OH(g)的能量变化如图所示,下列说法正确的是
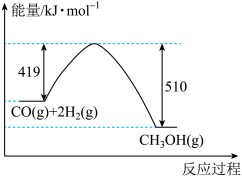

| A.由图可知,l mol CH3OH(g)的能量低于2mol H2(g)的能量 |
| B.断开1 molH2(g)中的化学键需要吸收209.5 kJ的能量 |
| C.CO(g)+ 2H2(g) = CH3OH ( l)ΔH= -91 kJ•mol-1 |
| D.CH3OH (g)= CO(g)+ 2 H2(g)ΔH = 91 kJ•mol-1 |
您最近一年使用:0次



