同学们在实验室中进行了铁粉与水蒸气的反应。
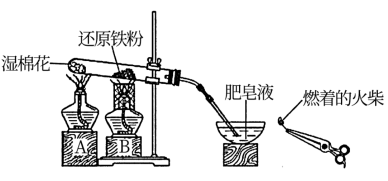
(1)铁粉与水蒸气反应的化学方程式是_______ 。
(2)B处酒精灯上网罩的作用是_______ 。
(3)实验开始时,应先点燃_______ (填“A”或“B”)处的酒精灯。实验开始后,用燃着的火柴点燃肥皂泡时的现象是_______ 。
(4)同学们对反应后黑色固体的成分展开了探究:将黑色固体用足量的FeCl3溶液浸泡,除去未反应的铁,有关反应的离子方程式是_______ 。然后过滤,将滤渣洗涤、干燥后,用磁铁吸引,观察到_______ ,证明黑色固体中含有Fe3O4。

(1)铁粉与水蒸气反应的化学方程式是
(2)B处酒精灯上网罩的作用是
(3)实验开始时,应先点燃
(4)同学们对反应后黑色固体的成分展开了探究:将黑色固体用足量的FeCl3溶液浸泡,除去未反应的铁,有关反应的离子方程式是
更新时间:2021-01-27 13:15:02
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】中学阶段,铁在纯氧中燃烧或与水蒸气在高温下反应可获得 ,
, 又可以表示为
又可以表示为 。某化学兴趣小组利用如图所示装置进行“铁与水蒸气反应”的实验,并检验产物的性质。请回答下列问题:
。某化学兴趣小组利用如图所示装置进行“铁与水蒸气反应”的实验,并检验产物的性质。请回答下列问题:
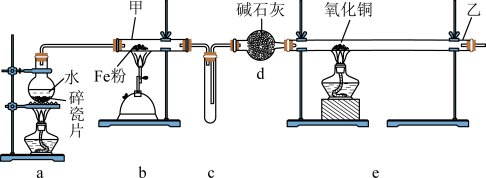
(1)组装好仪器后,应先进行的操作为_______ 。
(2)整套装置中,最先点燃_______ (填“a”、“b”或“e”)处的酒精灯或酒精喷灯,装置d中碱石灰作用是_______ 。
(3)写出仪器甲中发生反应的化学方程式:_______ ,还原剂为_______ 。
(4)若将 溶于足量的稀硫酸后发生反应的离子方程式为
溶于足量的稀硫酸后发生反应的离子方程式为_______ ,取少量该溶液于试管中,滴加几滴淀粉-KI溶液,观察到溶液变蓝,产生该现象的原因为_______ (请用离子方程式解释)。
(5)装置e中的实验现象为_______ ,本实验装置的不足之处为_______ 。
 ,
, 又可以表示为
又可以表示为 。某化学兴趣小组利用如图所示装置进行“铁与水蒸气反应”的实验,并检验产物的性质。请回答下列问题:
。某化学兴趣小组利用如图所示装置进行“铁与水蒸气反应”的实验,并检验产物的性质。请回答下列问题:
(1)组装好仪器后,应先进行的操作为
(2)整套装置中,最先点燃
(3)写出仪器甲中发生反应的化学方程式:
(4)若将
 溶于足量的稀硫酸后发生反应的离子方程式为
溶于足量的稀硫酸后发生反应的离子方程式为(5)装置e中的实验现象为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某化学兴趣小组利用如图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:

(1)A装置的作用是________________ ,B中反应的化学方程式为_____________ 。
(2)D的作用是____________________________________________________________ 。
(3)E中的现象是__________________________________________________________ 。
(4)A、B两个装置中应先点燃_______ 处的酒精灯,点燃E处酒精灯之前应进行的操作是_______________________________________________________________________ 。

(1)A装置的作用是
(2)D的作用是
(3)E中的现象是
(4)A、B两个装置中应先点燃
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某同学利用如图所示实验装置进行铁与水蒸气反应的实验,并对反应后硬质试管中固体物质的组成进行了探究。

请回答下列问题:
(1)硬质试管中湿棉花的作用是________________ 。
(2)铁与水蒸气的反应中,氧化剂是________ (填化学式,下同),还原剂是________ 。
(3)该同学对反应后硬质试管中固体物质的组成提出了如下假设:
假设1:只有Fe;
假设2:只有________ ;
假设3:既有Fe也有Fe3O4。
(4)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6 g,反应后固体物质的质量为6.6 g。从上述数据分析,反应后硬质试管中固体物质的组成为__________________ 。写出该反应的化学方程式________________________

请回答下列问题:
(1)硬质试管中湿棉花的作用是
(2)铁与水蒸气的反应中,氧化剂是
(3)该同学对反应后硬质试管中固体物质的组成提出了如下假设:
假设1:只有Fe;
假设2:只有
假设3:既有Fe也有Fe3O4。
(4)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6 g,反应后固体物质的质量为6.6 g。从上述数据分析,反应后硬质试管中固体物质的组成为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
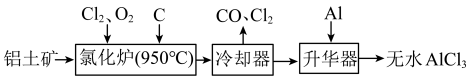
【推荐1】无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下:
(1)氧化铁的颜色为___________ 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为___________ 。
(3)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,请配平该反应的离子方程式:___________ 。
 +___________Cl2+___________= ___________
+___________Cl2+___________= ___________ +___________Cl-+___________
+___________Cl-+___________ ;
;
(4)升华器中主要含有AlCl3和FeCl3,需加入少量Al除去其中的FeCl3杂质,请设计实验方案检验FeCl3杂质是否除净:___________ 。
(5)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取l6.25g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32g。
①写出加入过量NaOH溶液时发生反应的离子方程式:___________ 、___________ 。
②AlCl3产品的纯度为___________ 。
(1)氧化铁的颜色为
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为
(3)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,请配平该反应的离子方程式:
 +___________Cl2+___________= ___________
+___________Cl2+___________= ___________ +___________Cl-+___________
+___________Cl-+___________ ;
;(4)升华器中主要含有AlCl3和FeCl3,需加入少量Al除去其中的FeCl3杂质,请设计实验方案检验FeCl3杂质是否除净:
(5)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取l6.25g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32g。
①写出加入过量NaOH溶液时发生反应的离子方程式:
②AlCl3产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某同学在探究铁生锈的条件时,将铁钉浸没在食盐水中,一段时间后,发现试管底部出现了黑色粉末。该同学对此黑色粉末的组成做了如下几种猜想:①Fe;②Fe2O3;③Fe3O4;④FeCl3。请完成下列问题。
(1)你认为该同学的上述猜想中,不做实验就可排除的是_______ ,理由是________ 。你认为黑色粉末还可能是_______ ,理由是_______ 。
(2)该同学将黑色粉末干燥后,用磁铁靠近,发现粉末能被磁铁吸引,于是得出结论:黑色粉末一定是铁粉。你认为该同学的结论对吗?_______ ,理由是________ 。
(1)你认为该同学的上述猜想中,不做实验就可排除的是
(2)该同学将黑色粉末干燥后,用磁铁靠近,发现粉末能被磁铁吸引,于是得出结论:黑色粉末一定是铁粉。你认为该同学的结论对吗?
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、B、C、D、E均为中学化学中常见物质,且均含有同一种元素,A为金属单质,它们之间的转化关系如图所示,其中②③反应用到同一种非金属单质(反应条件和其它产物已略去,物质状态均指在常温常压下)。
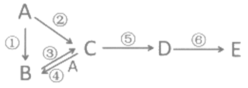
请回答:
(1)若E为红棕色粉末状固体,C的溶液遇KSCN溶液时变成红色。E的化学式为___ ,④的离子方程式为___ 。在B溶液中加入NaOH溶液,并置于空气中,产生的现象为___ ,此过程中发生氧化还原反应的化学方程式是___ 。
(2)若C为淡黄色粉末状固体,E可用于焙制糕点的发酵剂。B的电子式为___ 。若B在空气中可转化为E,用一个化学方程式表示为___ 。

请回答:
(1)若E为红棕色粉末状固体,C的溶液遇KSCN溶液时变成红色。E的化学式为
(2)若C为淡黄色粉末状固体,E可用于焙制糕点的发酵剂。B的电子式为
您最近一年使用:0次



