用 生产某些含氯有机物时会产生副产物
生产某些含氯有机物时会产生副产物 。利用反应A可实现氯元素的循环使用。
。利用反应A可实现氯元素的循环使用。
反应A: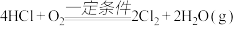
已知:Ⅰ.反应A中
 被氧化,放出
被氧化,放出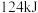 的热量。
的热量。
Ⅱ.
断开
 键与断开
键与断开
 键所需能量相差
键所需能量相差_______  。
。
 生产某些含氯有机物时会产生副产物
生产某些含氯有机物时会产生副产物 。利用反应A可实现氯元素的循环使用。
。利用反应A可实现氯元素的循环使用。反应A:
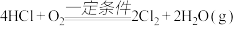
已知:Ⅰ.反应A中

 被氧化,放出
被氧化,放出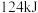 的热量。
的热量。Ⅱ.

断开

 键与断开
键与断开
 键所需能量相差
键所需能量相差 。
。
更新时间:2021-02-16 13:57:06
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】根据所给信息完成下列热化学方程式:
(1)已知1 mol C(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3 kJ热量,请写出该反应的热化学方程式:_____________________________________________________ 。
(2)1.7 g NH3(g)发生催化氧化反应生成气态产物,放出22.67 kJ的热量:_________ 。
(3)已知:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol−1,请写出1 mol NH3分解对应的热化学方程式:
2NH3(g) ΔH=-92.4 kJ·mol−1,请写出1 mol NH3分解对应的热化学方程式:_____________________________________________________ 。
(4)已知一些化学键的键能数据如表所示:
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:________ 。
(1)已知1 mol C(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3 kJ热量,请写出该反应的热化学方程式:
(2)1.7 g NH3(g)发生催化氧化反应生成气态产物,放出22.67 kJ的热量:
(3)已知:N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4 kJ·mol−1,请写出1 mol NH3分解对应的热化学方程式:
2NH3(g) ΔH=-92.4 kJ·mol−1,请写出1 mol NH3分解对应的热化学方程式:(4)已知一些化学键的键能数据如表所示:
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/kJ·mol-1 | 414 | 489 | 565 | 155 |
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)已知:
试计算N2+3H2=2NH3的∆H是多少?___
(2)已知:H2和CH4的燃烧热分别为∆H=-286KJ/mol和∆H-890KJ/mol,则112L标况下的H2和CH4的混合气体完全燃烧生成的CO2和液态水时放出3695KJ的热量,则混合气体中H2和CH4的物质的量之比是多少?___
| 化学键 | H-H | N≡N | N-H |
| 拆开1mol该键吸收能量KJ/mol | 436 | 946 | 391 |
试计算N2+3H2=2NH3的∆H是多少?
(2)已知:H2和CH4的燃烧热分别为∆H=-286KJ/mol和∆H-890KJ/mol,则112L标况下的H2和CH4的混合气体完全燃烧生成的CO2和液态水时放出3695KJ的热量,则混合气体中H2和CH4的物质的量之比是多少?
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2(g)+6H2O(l)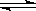 4NH3(g)+3O2(g) △H = akJ•mol-1
4NH3(g)+3O2(g) △H = akJ•mol-1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下:
①该反应的a______ 0(填“>”、“<”或“=”)
②已知:N2(g)+3H2(g)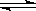 3NH3(g) △H = -92.4kJ•mol-1
3NH3(g) △H = -92.4kJ•mol-1
2H2(g) + O2(g)==2H2O(l) △H = -571.6 kJ•mol-1
则2N2(g) + 6H2O(l)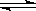 4NH3(g) + 3O2(g)△H =
4NH3(g) + 3O2(g)△H = _________ 。
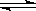 4NH3(g)+3O2(g) △H = akJ•mol-1
4NH3(g)+3O2(g) △H = akJ•mol-1进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下:
T/K | 303 | 313 | 323 |
NH3生成量/(10-6mol) | 4.8 | 5.8 | 6.0 |
①该反应的a
②已知:N2(g)+3H2(g)
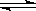 3NH3(g) △H = -92.4kJ•mol-1
3NH3(g) △H = -92.4kJ•mol-12H2(g) + O2(g)==2H2O(l) △H = -571.6 kJ•mol-1
则2N2(g) + 6H2O(l)
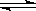 4NH3(g) + 3O2(g)△H =
4NH3(g) + 3O2(g)△H =
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)室温下,2g苯(C6H6)完全燃烧生成液态水和CO2,放出83.6kJ的热量,写出1molC6H6完全燃烧的热化学方程式:______ 。
(2)已知:Fe2O3(s)+ C(s)=
C(s)= CO2(g)+2Fe(s)△H=+akJ•mol-1;C(s)+O2(g)=CO2(g)△H=-bkJ•mol-1,则2Fe(s)+
CO2(g)+2Fe(s)△H=+akJ•mol-1;C(s)+O2(g)=CO2(g)△H=-bkJ•mol-1,则2Fe(s)+ O2(g)=Fe2O3(s)的△H=
O2(g)=Fe2O3(s)的△H=________ 。
(3)已知几种化学键的键能如表所示:
则反应Cl2(g)+3F2(g) 2ClF3(g)的△H=
2ClF3(g)的△H=_____________ kJ·mol-1。
(4)如图是乙烷、二甲醚燃烧过程中的能量变化图。
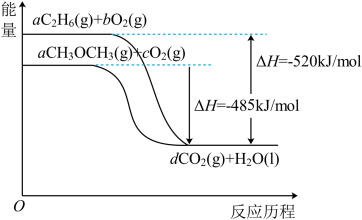
请回答下列问题:
①乙烷的燃烧热ΔH=_______ kJ·mol-1。
②根据题图写出二甲醚完全燃烧时的热化学方程式__________ 。
(2)已知:Fe2O3(s)+
 C(s)=
C(s)= CO2(g)+2Fe(s)△H=+akJ•mol-1;C(s)+O2(g)=CO2(g)△H=-bkJ•mol-1,则2Fe(s)+
CO2(g)+2Fe(s)△H=+akJ•mol-1;C(s)+O2(g)=CO2(g)△H=-bkJ•mol-1,则2Fe(s)+ O2(g)=Fe2O3(s)的△H=
O2(g)=Fe2O3(s)的△H=(3)已知几种化学键的键能如表所示:
| 化学键 | Cl—Cl | F—F | Cl—F |
| 键能/ kJ·mol—1 | 242 | 159 | 172 |
 2ClF3(g)的△H=
2ClF3(g)的△H=(4)如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
①乙烷的燃烧热ΔH=
②根据题图写出二甲醚完全燃烧时的热化学方程式
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得5g甲醇在氧气中是充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇的标准燃烧热热化学方程式:_____________________________ 。
(2)亚硝酸氯(结构式为 是有机合成中的重要试剂,可由Cl2和NO在通常反应条件下制得,反应方程式为
是有机合成中的重要试剂,可由Cl2和NO在通常反应条件下制得,反应方程式为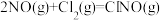 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:
当Cl2与NO反应生成ClNO的过程中转移了2mol电子,理论上放出的热量为_________ kJ。(用数字和字母表示)
(3)已知: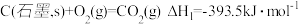
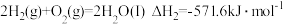

根据盖斯定律,计算298K时,面C(石墨,s)和 生成
生成 反应的焓变
反应的焓变
________ 。
(1)实验测得5g甲醇在氧气中是充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇的标准燃烧热热化学方程式:
(2)亚硝酸氯(结构式为
 是有机合成中的重要试剂,可由Cl2和NO在通常反应条件下制得,反应方程式为
是有机合成中的重要试剂,可由Cl2和NO在通常反应条件下制得,反应方程式为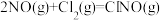 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:| 化学键 | Cl-Cl | Cl-N | N=O | N=O(NO) |
键能 | 243 | a | 607 | 630 |
当Cl2与NO反应生成ClNO的过程中转移了2mol电子,理论上放出的热量为
(3)已知:
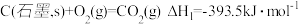
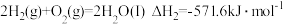

根据盖斯定律,计算298K时,面C(石墨,s)和
 生成
生成 反应的焓变
反应的焓变
您最近半年使用:0次

 、
、 分子中的化学键需要吸收的能量分别为
分子中的化学键需要吸收的能量分别为 、
、 ,
, 与
与 反应生成
反应生成 的能量变化如图所示:
的能量变化如图所示:
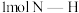 键需要吸收的能量为
键需要吸收的能量为

