根据元素周期律,由下列事实进行归纳推测,推测不合理 的是
| 选项 | 事实 | 推测 |
| A. |  和 和 都难溶于水 都难溶于水 |  也难溶于水 也难溶于水 |
| B. | Si与 高温时反应,S与 高温时反应,S与 加热能反应 加热能反应 | P与 在高温时能反应 在高温时能反应 |
| C. | Si是半导体材料,同族的Ge也是半导体材料 | 第ⅣA族的元素的单质都可作半导体材料 |
| D. | HCl在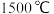 时分解,HI在 时分解,HI在 时分解 时分解 | HBr的分解温度介于二者之间 |
| A.A | B.B | C.C | D.D |
更新时间:2021-03-04 18:15:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】应用元素周期律的有关知识,可以预测我们不熟悉的一些元素的单质及其化合物的性质。下列预测中正确的是
①Be的最高价氧化物的水化物可能具有两性
②Tl(对应元素位于第IIIA族)与盐酸和NaOH溶液作用均能产生氢气
③At(第VIIA族元素)的单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是 ,其溶液是一种强碱溶液
,其溶液是一种强碱溶液
⑤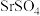 (Sr位于第IIA族)是难溶于水的白色固体
(Sr位于第IIA族)是难溶于水的白色固体
⑥ 是无色、有毒、比
是无色、有毒、比 稳定的气体
稳定的气体
①Be的最高价氧化物的水化物可能具有两性
②Tl(对应元素位于第IIIA族)与盐酸和NaOH溶液作用均能产生氢气
③At(第VIIA族元素)的单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是
 ,其溶液是一种强碱溶液
,其溶液是一种强碱溶液⑤
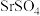 (Sr位于第IIA族)是难溶于水的白色固体
(Sr位于第IIA族)是难溶于水的白色固体⑥
 是无色、有毒、比
是无色、有毒、比 稳定的气体
稳定的气体| A.①②③④ | B.②④⑥ | C.①③⑤ | D.②④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2016年IUPAC命名117号元素为Ts(中文名tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
| A.Ts的同位素原子具有相同的电子数 | B.中子数为176的Ts核素符号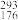 Ts Ts |
| C.Ts在同族元素中非金属性最弱 | D.Ts是第七周期第ⅦA族元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】应用元素周期律可预测我们不知道的一些元素及其化合物的性质,下列预测合理的是
A.S与Se同主族, 无色,有毒,比 无色,有毒,比 稳定 稳定 |
| B.At与Cl同主族,AgAt可溶于水 |
| C.Be的氧化物可能具有两性 |
D.Li在氧气中剧烈燃烧,产物是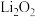 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列排列顺序正确的是
(1)热稳定性:H2O>HF>H2S (2)原子半径:Na>Mg>O(3)酸性:H3PO4>H2SO4>HClO4 (4)碱性强弱:NaOH>Mg(OH)2>Al(OH)3
(1)热稳定性:H2O>HF>H2S (2)原子半径:Na>Mg>O(3)酸性:H3PO4>H2SO4>HClO4 (4)碱性强弱:NaOH>Mg(OH)2>Al(OH)3
| A.(1)(3) | B.(2)(4) | C.(1)(4) | D.(2)(3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下面是某学生利用数据分析的情况,其中正确的是
| A.根据气体的相对分子质量,不可以比较相同状况下气体密度的大小 |
| B.根据甲烷和乙烷的熔点,不能比较二者晶体中的分子间作用力的大小 |
| C.比较同主族金属元素原子半径的大小,可以推断元素的金属性强弱 |
| D.根据液体密度的大小,可以判断液体的挥发性的强弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】应用元素周期律分析下列推断,其中正确的组合是( )
①第ⅡA族单质的熔点随原子序数的增大而降低
②砹(At)是第VIIA族,其氢化物的稳定性大于HCl
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
①第ⅡA族单质的熔点随原子序数的增大而降低
②砹(At)是第VIIA族,其氢化物的稳定性大于HCl
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
| A.①③⑥ | B.②④⑥ | C.③④⑤ | D.①③④ |
您最近一年使用:0次

 (FeO)中通入
(FeO)中通入 ,加热除去FeO
,加热除去FeO 时,可以将胶头滴管插入
时,可以将胶头滴管插入 溶液底部挤出NaOH溶液
溶液底部挤出NaOH溶液

