碱式氯化铜(不溶于水的绿色晶体)是一种农药,分子式:CuCl2·3Cu(OH)2·XH2O(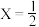 ,1,2).为验证其组成并确定X值,某学生设计了以下几步实验:
,1,2).为验证其组成并确定X值,某学生设计了以下几步实验:
①取a g的晶体研成粉末
②晶体在空气中加热至确认质量不再变化为止(铜仍为二价),冷却后称其质量为b g
③另取a g的晶体,溶于足量稀硝酸中充分溶解得到溶液
④向③得到的溶液中加入足量的硝酸银溶液,最后得到纯净固体称量为c g。
若以上操作均正确,试回答下列问题:
(1)以上实验中用到玻璃棒的步骤有_______ (填序号)。
(2)步骤②中晶体应放在_______ (填仪器名称)中灼烧。
(3)步骤④主要包括:加入足量硝酸银溶液→_______ →_______ →晾干→称量。
(4)碱式氯化铜的摩尔质量为_______ (用含a、c的代数式表示。)
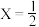 ,1,2).为验证其组成并确定X值,某学生设计了以下几步实验:
,1,2).为验证其组成并确定X值,某学生设计了以下几步实验:①取a g的晶体研成粉末
②晶体在空气中加热至确认质量不再变化为止(铜仍为二价),冷却后称其质量为b g
③另取a g的晶体,溶于足量稀硝酸中充分溶解得到溶液
④向③得到的溶液中加入足量的硝酸银溶液,最后得到纯净固体称量为c g。
若以上操作均正确,试回答下列问题:
(1)以上实验中用到玻璃棒的步骤有
(2)步骤②中晶体应放在
(3)步骤④主要包括:加入足量硝酸银溶液→
(4)碱式氯化铜的摩尔质量为
更新时间:2021-03-07 17:48:27
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某研究性学习小组拟探究热CuCl2·2H2O的热稳定性,进行如下操作:
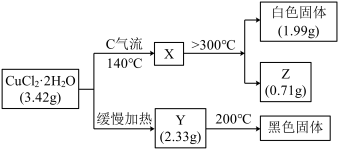
上述所列物质都是纯净物,请回答:
(1)气流C的结构式______ ,白色固体的化学式________ 。
(2)已知Y的摩尔质量为233 g·mol-1,完成CuCl2·2H2O缓慢加热分解的化学方程式__________ 。

上述所列物质都是纯净物,请回答:
(1)气流C的结构式
(2)已知Y的摩尔质量为233 g·mol-1,完成CuCl2·2H2O缓慢加热分解的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】为探究黑色固体Y(仅含两种元素)的组成和性质,设计并完成如图实验。请回答:
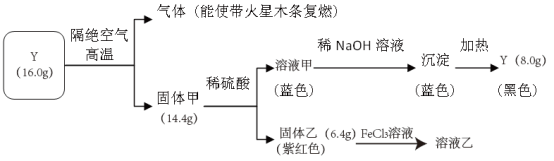
(1)Y的化学式是___ ;
(2)固体乙与FeCl3溶液反应的化学方程式是___ ;
(3)固体甲与稀硫酸反应的离子方程式是___ 。

(1)Y的化学式是
(2)固体乙与FeCl3溶液反应的化学方程式是
(3)固体甲与稀硫酸反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】凤凰石的主要成分为水合铜硅酸盐,还含有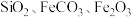 等杂质,以凤凰石为原料生产媒染剂无水
等杂质,以凤凰石为原料生产媒染剂无水 的工业流程如下:
的工业流程如下:
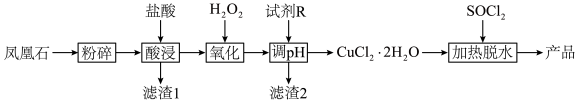
已知: ;
;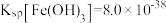 ;
;
回答下列问题:
(1)已知 是一种二元弱酸,则其第二步电离的方程式为
是一种二元弱酸,则其第二步电离的方程式为___________ ,常温下 的
的 溶液的
溶液的 约为
约为___________ (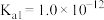 、
、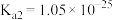 ),“氧化”步骤发生反应的离子方程式为
),“氧化”步骤发生反应的离子方程式为___________ 。
(2)加入“试剂R”调解溶液pH将溶液中铁元素转化为氢氧化物沉淀而除去,“试剂R”最好是___________(填字母)。
(3) 遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出
遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出 水解的化学方程式:
水解的化学方程式:___________ 。 脱水时
脱水时 可抑制
可抑制 的水解,其抑制原理主要包含两点:①
的水解,其抑制原理主要包含两点:① 与水反应减少了水的量;②
与水反应减少了水的量;②___________ 。
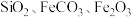 等杂质,以凤凰石为原料生产媒染剂无水
等杂质,以凤凰石为原料生产媒染剂无水 的工业流程如下:
的工业流程如下:
已知:
 ;
;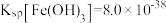 ;
;
回答下列问题:
(1)已知
 是一种二元弱酸,则其第二步电离的方程式为
是一种二元弱酸,则其第二步电离的方程式为 的
的 溶液的
溶液的 约为
约为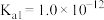 、
、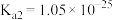 ),“氧化”步骤发生反应的离子方程式为
),“氧化”步骤发生反应的离子方程式为(2)加入“试剂R”调解溶液pH将溶液中铁元素转化为氢氧化物沉淀而除去,“试剂R”最好是___________(填字母)。
A. | B. | C. | D. |
(3)
 遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出
遇水剧烈水解生成两种气体,常用作脱水剂(水解过程中元素的化合价不变),写出 水解的化学方程式:
水解的化学方程式: 脱水时
脱水时 可抑制
可抑制 的水解,其抑制原理主要包含两点:①
的水解,其抑制原理主要包含两点:① 与水反应减少了水的量;②
与水反应减少了水的量;②
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为测定某三价铁配合物(化学式表示为Ka[Feb(C2O4)c]·xH2O)的组成,做了如下实验:
步骤1:称取1.9640g Ka[Feb(C2O4)c]·xH2O晶体,配制成250.00mL溶液.
步骤2:取所配溶液25.00mL于锥形瓶中,加入1mol/LH2SO45.0mL,加热到70~85℃,用0.01000mol/LKMnO4溶液滴定至终点(5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O),消耗KMnO4溶液48.00mL。
步骤3:向反应后的溶液中加入一定量锌粉。加热至黄色恰好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤4:继续用0.01000mol/LKMnO4溶液滴定步骤3所得溶液至终点,消耗KMnO4溶液8.00mL。
(1)步骤2中滴定终点的现象是_______
(2)步骤3中加入锌粉的目的是__________
(3)步聚4中发生反应的离于方程式为__________
(4)通过计算确定该三价铁配合物的化学式________ (写出计算过程)。
步骤1:称取1.9640g Ka[Feb(C2O4)c]·xH2O晶体,配制成250.00mL溶液.
步骤2:取所配溶液25.00mL于锥形瓶中,加入1mol/LH2SO45.0mL,加热到70~85℃,用0.01000mol/LKMnO4溶液滴定至终点(5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O),消耗KMnO4溶液48.00mL。
步骤3:向反应后的溶液中加入一定量锌粉。加热至黄色恰好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤4:继续用0.01000mol/LKMnO4溶液滴定步骤3所得溶液至终点,消耗KMnO4溶液8.00mL。
(1)步骤2中滴定终点的现象是
(2)步骤3中加入锌粉的目的是
(3)步聚4中发生反应的离于方程式为
(4)通过计算确定该三价铁配合物的化学式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】正丁醚常用作有机反应的溶剂。实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:
(CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:
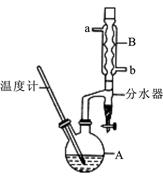
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70 mL水的温度分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11 g。请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加 。
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振摇后静置,粗产物应 (填“上”或“下”)口倒出。
(4)步骤③中最后一次水洗的目的为 。
(5)步骤⑤中,加热蒸馏时应收集 (填选项字母)左右的馏分。
A.100℃ B.117℃ C.135℃ D.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为 ,下层液体的主要成分为 。
(7)本实验中,正丁醚的产率为 (精确到1%)。
 (CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:
(CH3CH2CH2CH2)2O,反应物和产物的相关数据如下表:| 相对分子质量 | 沸点/℃ | 密度/(g/cm3) | 水中的溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |

①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。
③分离提纯:待A中液体冷却后将其缓慢倒入盛有70 mL水的温度分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11 g。请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为:应先加 。
(2)加热A前,需先从 (填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振摇后静置,粗产物应 (填“上”或“下”)口倒出。
(4)步骤③中最后一次水洗的目的为 。
(5)步骤⑤中,加热蒸馏时应收集 (填选项字母)左右的馏分。
A.100℃ B.117℃ C.135℃ D.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为 ,下层液体的主要成分为 。
(7)本实验中,正丁醚的产率为 (精确到1%)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】碱式碳酸铜可用作木材防腐剂、水体杀藻剂等,研究性学习小组设计以下方案制备碱式碳酸铜并进行相关实验探究。
Ι.以铜屑为原料制备碱式碳酸铜的装置如下:
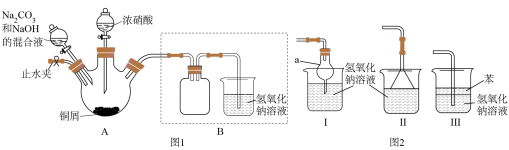
步骤1连接好装置,检查装置的气密性,装药品。
步骤2往三颈烧瓶中加入适量的浓硝酸,使铜屑完全反应。
步骤3往步骤2反应后的溶液中加入一定比例的Na2CO3和NaOH的混合液,加热。
步骤4将三颈烧瓶中的混合物过滤、洗涤、烘干,获得产物。
已知:ⅰ.碱式碳酸铜为草绿色或绿色结晶物,易溶于酸,不溶于水,在100℃的水中易分解;
ⅱ.NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO3+NaNO2+H2O;
NO不能单独与NaOH溶液反应。
(1)步骤2中浓硝酸与铜屑反应的离子方程式为___________________ 。
(2)步骤2反应一段时间后,须打开止水夹,通入一段时间的空气,目的是_______ 。
(3)步骤3对装置A的加热方式最好采用____________ 。
(4)装置Ι中仪器a的名称为____ ,Ⅰ、Ⅱ、Ⅲ三个装置不能替代图1中B装置的是_____ (填装置序号)。
(5)欲检验步骤4获得的产物中是否含有NO3-,所需的试剂可以是__________ 。
Ⅱ.探究在一定温度下,不同的原料配比对产物的影响,实验数据如下:
注:“+”越多表示沉淀量越多
(6)分析表格数据可得:制备碱式碳酸铜最佳的原料配比n[Cu(NO3)2]:n(NaOH) : n(Na2CO3) =___ 。
Ⅲ.产物组成的测定
(7)碱式碳酸铜的成分有多种,化学式可表示为mCu(OH)2·n CuCO3。为测定Ι中所得碱式碳酸铜的组成,学习小组同学准确称取3.820 g样品溶于适量的硫酸中,加水配成l00 mL溶液,取l0.00 mL溶液于锥形瓶中,加适量水稀释,调节溶液pH至3~4,加入过量的KI(2 Cu2++ 4 I-= 2 CuI↓ + I2),用0.l000 mol·L-1Na2S2O3标准溶液滴定(2 S2O32-+ I2= 2I-+ S4O62-),接近终点时,加入淀粉指示剂,继续滴定至终点,蓝色消失。进行平行实验后,测得平均消耗Na2S2O3标准溶液的体积为35.00 mL。该碱式碳酸铜的化学式为_____
Ι.以铜屑为原料制备碱式碳酸铜的装置如下:

步骤1连接好装置,检查装置的气密性,装药品。
步骤2往三颈烧瓶中加入适量的浓硝酸,使铜屑完全反应。
步骤3往步骤2反应后的溶液中加入一定比例的Na2CO3和NaOH的混合液,加热。
步骤4将三颈烧瓶中的混合物过滤、洗涤、烘干,获得产物。
已知:ⅰ.碱式碳酸铜为草绿色或绿色结晶物,易溶于酸,不溶于水,在100℃的水中易分解;
ⅱ.NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO3+NaNO2+H2O;
NO不能单独与NaOH溶液反应。
(1)步骤2中浓硝酸与铜屑反应的离子方程式为
(2)步骤2反应一段时间后,须打开止水夹,通入一段时间的空气,目的是
(3)步骤3对装置A的加热方式最好采用
(4)装置Ι中仪器a的名称为
(5)欲检验步骤4获得的产物中是否含有NO3-,所需的试剂可以是
Ⅱ.探究在一定温度下,不同的原料配比对产物的影响,实验数据如下:
| 实验序号 | V[Cu(NO3)2] /mL (0.5 mol·L-1) | V(NaOH) / mL (0.5 mol·L-1) | V(Na2CO3)/ mL (0.25 mol·L-1) | 沉淀数量 | 沉淀颜色 |
| 1 | 2.0 | 2.0 | 1.6 | + | 浅绿色 |
| 2 | 2.0 | 2.0 | 2.0 | + + | 浅绿色 |
| 3 | 2.0 | 2.0 | 2.4 | + + + | 蓝色 |
| 4 | 2.0 | 2.0 | 2.8 | + + + | 蓝色 |
(6)分析表格数据可得:制备碱式碳酸铜最佳的原料配比n[Cu(NO3)2]:n(NaOH) : n(Na2CO3) =
Ⅲ.产物组成的测定
(7)碱式碳酸铜的成分有多种,化学式可表示为mCu(OH)2·n CuCO3。为测定Ι中所得碱式碳酸铜的组成,学习小组同学准确称取3.820 g样品溶于适量的硫酸中,加水配成l00 mL溶液,取l0.00 mL溶液于锥形瓶中,加适量水稀释,调节溶液pH至3~4,加入过量的KI(2 Cu2++ 4 I-= 2 CuI↓ + I2),用0.l000 mol·L-1Na2S2O3标准溶液滴定(2 S2O32-+ I2= 2I-+ S4O62-),接近终点时,加入淀粉指示剂,继续滴定至终点,蓝色消失。进行平行实验后,测得平均消耗Na2S2O3标准溶液的体积为35.00 mL。该碱式碳酸铜的化学式为
您最近一年使用:0次



