科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l )的燃烧热 分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
(1)用太阳能分解10 mol水消耗的能量是______ kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为______ ;
(3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃)
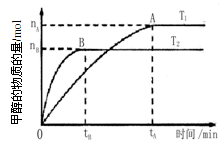
下列说法正确的是______ (填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为n(CH3OH)= mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时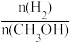 增大
增大
(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为 ,则容器内的压强与起始压强之比为
,则容器内的压强与起始压强之比为______ 。
 分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:(1)用太阳能分解10 mol水消耗的能量是
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃)

下列说法正确的是
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为n(CH3OH)=
 mol·L-1·min-1
mol·L-1·min-1②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时
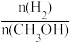 增大
增大(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为
 ,则容器内的压强与起始压强之比为
,则容器内的压强与起始压强之比为
12-13高二上·天津·期中 查看更多[6]
(已下线)2011-2012学年天津一中高二上学期期中考试化学试卷2014-2015山西省大同市一中高二上学期期中化学试卷(已下线)2014届浙江效实中学高一下学期期中考试化学(1-3班)试卷(已下线)2012-2013学年河南省许昌市六校高一第六次联考化学试卷(已下线)2011-2012学年江西省南昌三中高二上学期期中考试化学试卷(已下线)2011-2012学年天津市天津一中高二上学期期中考试化学试卷
更新时间:2016-12-08 19:29:53
|
【知识点】 化学电源
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】铅蓄电池在日常生活中应用广泛。回答下列问题:
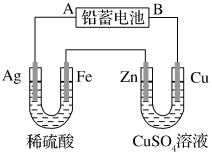
(1)铅蓄电池放电时的工作原理为Pb+PbO2+2H2SO4=2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题:
①A是铅蓄电池的________ 极。
②Ag电极的电极反应式是_______________ ,该电极的电极产物共________ g。
③Cu电极的电极反应式是_______________ ,CuSO4溶液的浓度________ (填“减小”“增大”或“不变”)。
(2)铅蓄电池的PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___________ ;
PbO2也可以石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液制取。阳极发生的电极反应式为___________ ,阴极上观察到的现象是____________ ;若电解液中不加入Cu(NO3)2,阴极发生的电极反应式为________________ ,这样做的主要缺点是________________ 。
(3)将Na2S溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应:S2--2e-=S,(n-1)S+S2-=Sn2-。
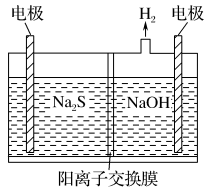
电解时阴极的电极反应式:_________________ 。电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成____________________ 。

(1)铅蓄电池放电时的工作原理为Pb+PbO2+2H2SO4=2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题:
①A是铅蓄电池的
②Ag电极的电极反应式是
③Cu电极的电极反应式是
(2)铅蓄电池的PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为
PbO2也可以石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液制取。阳极发生的电极反应式为
(3)将Na2S溶液加入如图所示的电解池的阳极区,用铅蓄电池进行电解,电解过程中阳极区发生如下反应:S2--2e-=S,(n-1)S+S2-=Sn2-。

电解时阴极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】燃料电池是很有发展前途的新的动力电源,氢氧燃料电池因其绿色环保、能量转换率高而备受关注。通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在碱式介质中,负极反应的物质为_____ ,正极反应的物质为_____ 碱式电池的电极反应:负极:_____ ,正极:_____ 。电解质溶液pH的变化_____ (填“变大”,“变小”,“不变”)。
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之,下列不正确的是_____。(单选)
(3)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:

①该电池放电时正极反应式为_____ 。
②放电时每转移3mol电子,正极有_____ mol 被还原。
被还原。
(4)铅蓄电池因其电压稳定、使用方便、安全可靠、价格低康,当前在燃油车上应用依然占主导地位,电池反应式为: ,下列有关说法正确的是_____。(双选)
,下列有关说法正确的是_____。(双选)

(1)在碱式介质中,负极反应的物质为
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之,下列不正确的是_____。(单选)
| A.太阳光催化分解水制氯气比电解水气氢气更为科学 |
| B.氢氧燃料电池作为汽车动力更能保护环境 |
C.以稀 、KOH为介质的氢氧燃料电池的负极电极反应式相同 、KOH为介质的氢氧燃料电池的负极电极反应式相同 |
D.以稀 、KOH为介质的氢氧燃料电池的总反应式相同 、KOH为介质的氢氧燃料电池的总反应式相同 |

①该电池放电时正极反应式为
②放电时每转移3mol电子,正极有
 被还原。
被还原。(4)铅蓄电池因其电压稳定、使用方便、安全可靠、价格低康,当前在燃油车上应用依然占主导地位,电池反应式为:
 ,下列有关说法正确的是_____。(双选)
,下列有关说法正确的是_____。(双选)
A.Pb为电池的负极,发生氧化反应,电极方程式为: |
| B.铅蓄电池放电时,正、负电极质量均增大 |
C.铅蓄电池放电时, 定向移动去 定向移动去 极 极 |
| D.放电过程中,正极区附近pH减小 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)高铁酸钾(K2FeO4)的还原产物常常是Fe(OH)3,常常用于水处理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置。试回答下列问题:
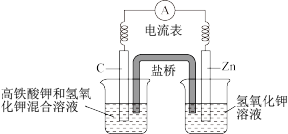
①该电池放电时正极的电极反应式为___________ ;
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向___________ (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向___________ (填“左”或“右”)移动。
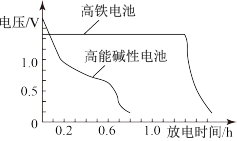
③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得高铁电池的优点有___________ 。
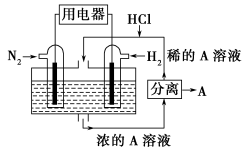
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,电池正极的电极反应式是___________ ,A是___________ 。
(1)高铁酸钾(K2FeO4)的还原产物常常是Fe(OH)3,常常用于水处理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置。试回答下列问题:

①该电池放电时正极的电极反应式为
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向

③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得高铁电池的优点有
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,电池正极的电极反应式是

您最近一年使用:0次



