燃料电池是很有发展前途的新的动力电源,氢氧燃料电池因其绿色环保、能量转换率高而备受关注。通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在碱式介质中,负极反应的物质为_____ ,正极反应的物质为_____ 碱式电池的电极反应:负极:_____ ,正极:_____ 。电解质溶液pH的变化_____ (填“变大”,“变小”,“不变”)。
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之,下列不正确的是_____。(单选)
(3)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:

①该电池放电时正极反应式为_____ 。
②放电时每转移3mol电子,正极有_____ mol 被还原。
被还原。
(4)铅蓄电池因其电压稳定、使用方便、安全可靠、价格低康,当前在燃油车上应用依然占主导地位,电池反应式为: ,下列有关说法正确的是_____。(双选)
,下列有关说法正确的是_____。(双选)

(1)在碱式介质中,负极反应的物质为
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之,下列不正确的是_____。(单选)
| A.太阳光催化分解水制氯气比电解水气氢气更为科学 |
| B.氢氧燃料电池作为汽车动力更能保护环境 |
C.以稀 、KOH为介质的氢氧燃料电池的负极电极反应式相同 、KOH为介质的氢氧燃料电池的负极电极反应式相同 |
D.以稀 、KOH为介质的氢氧燃料电池的总反应式相同 、KOH为介质的氢氧燃料电池的总反应式相同 |

①该电池放电时正极反应式为
②放电时每转移3mol电子,正极有
 被还原。
被还原。(4)铅蓄电池因其电压稳定、使用方便、安全可靠、价格低康,当前在燃油车上应用依然占主导地位,电池反应式为:
 ,下列有关说法正确的是_____。(双选)
,下列有关说法正确的是_____。(双选)
A.Pb为电池的负极,发生氧化反应,电极方程式为: |
| B.铅蓄电池放电时,正、负电极质量均增大 |
C.铅蓄电池放电时, 定向移动去 定向移动去 极 极 |
| D.放电过程中,正极区附近pH减小 |
更新时间:2023-06-18 16:44:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如图所示的原电池装置中
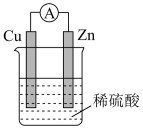
(1)正极的电极反应方程式是_______ 。
(2)该原电池的中反应离子方程式_______ 。

(1)正极的电极反应方程式是
(2)该原电池的中反应离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)今有氢氧燃料电池,则正极通入的气体是________ ,负极通入的气体是________ ,电解质溶液为稀硫酸时,电极反应式为:正极____________ ;负极___________ ,电池的总反应式为__________ ;
(2)如把H2改为甲烷、KOH作导电物质,则电极反应式为:负极___________ 。
(2)如把H2改为甲烷、KOH作导电物质,则电极反应式为:负极
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据铜锌原电池示意图,回答下列问题:

(1)锌为___________ 极,电极反应式为___________ ;铜为___________ 极,电极反应为___________ ,原电池总离子反应式是___________ 。
(2)若以该电池作为电源,以石墨碳棒为电极电解CuCl2溶液,在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量___________ (填“增加”、“不变”或“减少”);电子从电池的锌极沿导线流向电解池的___________ (填“阴极”或“阳极”,下同);在电解池中Cu2+向___________ 移动,在该电极上析出铜的质量为________ g。

(1)锌为
(2)若以该电池作为电源,以石墨碳棒为电极电解CuCl2溶液,在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2021年我国自主研发的神舟十三号载人飞船成功进入太空,其轨道舱和推进舱使用太阳能电池阵——镍镉蓄电池组系统,返回舱使用的是银锌蓄电池组。
(1)飞船在光照区运行时,太阳能电池帆板将____ 能转化为____ 能。除供给飞船使用放电,多余部分用镍镉蓄电池储存起来,其工作原理为Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是
Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是___ 。
A.放电时负极反应式为Cd+2OH--2e-=Cd(OH)2
B.放电时电子由镍电极经导线流向镉电极
C.充电时阳极反应式为Ni(OH)2+OH--2e-=NiOOH+H2O
D.充电时电解质溶液中的OH-移向镉电极
(2)返回舱使用的是银锌蓄电池组,其工作原理为:Zn+Ag2O+H2O 2Ag+Zn(OH)2。
2Ag+Zn(OH)2。
①其负极的电极材料为____ ,负极反应类型为____ 。
②在电池使用的过程中,电解质溶液中KOH的物质的量浓度____ (填“增大”、“减小”或“不变”)。
③当电池工作时通过电路对外提供了1mol电子,则正极质量减轻____ g。
(1)飞船在光照区运行时,太阳能电池帆板将
 Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是
Cd(OH)2+2Ni(OH)2。下列有关镍镉电池的说法正确的是A.放电时负极反应式为Cd+2OH--2e-=Cd(OH)2
B.放电时电子由镍电极经导线流向镉电极
C.充电时阳极反应式为Ni(OH)2+OH--2e-=NiOOH+H2O
D.充电时电解质溶液中的OH-移向镉电极
(2)返回舱使用的是银锌蓄电池组,其工作原理为:Zn+Ag2O+H2O
 2Ag+Zn(OH)2。
2Ag+Zn(OH)2。①其负极的电极材料为
②在电池使用的过程中,电解质溶液中KOH的物质的量浓度
③当电池工作时通过电路对外提供了1mol电子,则正极质量减轻
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.如图为相互串联的甲、乙两个电解池。

(1)甲池若为用电解原理精炼铜的装置,A极电极反应式为___________ 。电解一段时间后,电解质溶液的浓度___________ 。(填“增大”、“减小”或“不变”)。
(2)甲池若为铁制品上镀银的装置,A极材料是___________ 。
(3)乙池中发生反应的离子方程式为___________ 。
II.锂-空气二次电池的探索和研发成为储能领域的研究热点。
(4)锂-空气电池工作和充电原理如图所示。下列说法正确的是___________(填标号)。
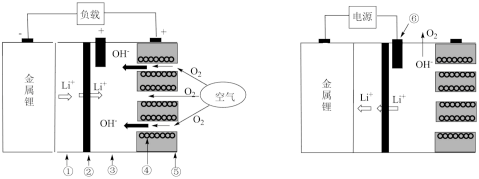
①有机电解液②固体电解质③水性电解液④催化剂⑤纳米碳片⑥充电专用电板
III.利用电化学方法可以将 有效地转化为
有效地转化为 (其中C元素的化合价为
(其中C元素的化合价为 价),装置如下图所示。
价),装置如下图所示。
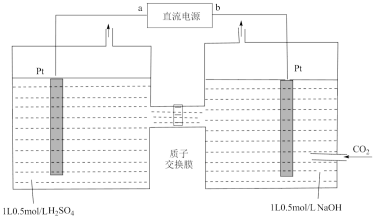
(5)若以碱性氢氧燃料电池为直流电源,则燃料电池中b极电极反应式为___________ 。
(6)装置工作时,阴极除有 生成外,还可能生成副产物降低电解效率。
生成外,还可能生成副产物降低电解效率。
已知:电解效率= 。
。
①副产物可能是___________ (写出一种即可)。
②标准状况下,当阳极生成氧气体积为224mL时,测得整个阴极区内的 ,电解效率为
,电解效率为___________ (忽略电解前后溶液的体积变化)。

(1)甲池若为用电解原理精炼铜的装置,A极电极反应式为
(2)甲池若为铁制品上镀银的装置,A极材料是
(3)乙池中发生反应的离子方程式为
II.锂-空气二次电池的探索和研发成为储能领域的研究热点。
(4)锂-空气电池工作和充电原理如图所示。下列说法正确的是___________(填标号)。

①有机电解液②固体电解质③水性电解液④催化剂⑤纳米碳片⑥充电专用电板
| A.锂-空气电池配置了充电专用电极,可防止充电时空气极(纳米碳片)发生腐蚀 |
B.该电池放电时正极反应式为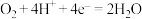 |
C.当有 (标况)在纳米碳片上参加反应,金属锂电极会损失2.8g (标况)在纳米碳片上参加反应,金属锂电极会损失2.8g |
| D.若用铅蓄电池给锂-空气电池充电,Pb电极应与充电专用电极相接 |
III.利用电化学方法可以将
 有效地转化为
有效地转化为 (其中C元素的化合价为
(其中C元素的化合价为 价),装置如下图所示。
价),装置如下图所示。
(5)若以碱性氢氧燃料电池为直流电源,则燃料电池中b极电极反应式为
(6)装置工作时,阴极除有
 生成外,还可能生成副产物降低电解效率。
生成外,还可能生成副产物降低电解效率。已知:电解效率=
 。
。①副产物可能是
②标准状况下,当阳极生成氧气体积为224mL时,测得整个阴极区内的
 ,电解效率为
,电解效率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。
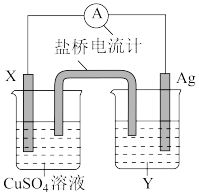
请回答下列问题:
(1)电极 X 的材料是__________ 填化学式);电解质溶液 Y 是______ 填化学式)。
(2)银电极发生______ 填“氧化”或“还原”)反应,其电极反应式为_________ ;X 电极反应式为_____ 。
II. 高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放 电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
请回答下列问题:
(1)已知放电时负极反应为 Zn-2e-+2OH- ===Zn(OH)2,则正极反应 为_____________ 。
(2)放电时,_____ (填“正”或“负”)极附近溶液的 pH 升高。
(3)高铁电池充电时,电池的负极与电源的_____ (填“正极”或“负极”),充 电时与电池负极相连的电极反应为__________ 。
III.近几年开发的甲醇燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子和 水分子通过。其工作原理的示意图如下:

请回答下列问题: (1)该燃料电池的总反应为_________ 。
(2)Pt(a)电极是电池的_____ (填“正”或“负”)极,电极反应式为:__________ ; Pt(b)电极反应式为___________ 。

请回答下列问题:
(1)电极 X 的材料是
(2)银电极发生
II. 高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放 电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)已知放电时负极反应为 Zn-2e-+2OH- ===Zn(OH)2,则正极反应 为
(2)放电时,
(3)高铁电池充电时,电池的负极与电源的
III.近几年开发的甲醇燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子和 水分子通过。其工作原理的示意图如下:

请回答下列问题: (1)该燃料电池的总反应为
(2)Pt(a)电极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
正极电极反应式为______________ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为_____________ ,当线路中转移0.2 mol电子时,则被腐蚀铜的质量为_____________ g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为______________ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
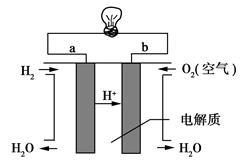
①氢氧燃料电池的总反应化学方程式是:________________ 。
②电池工作一段时间后硫酸溶液的浓度_____________ (填“增大”、“减小”或“不变”)。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
正极电极反应式为
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的总反应化学方程式是:
②电池工作一段时间后硫酸溶液的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图为原电池装置示意图。
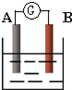
(1)若A为Pb,B为PbO2,电解质溶液为H2SO4溶液,电池的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。则该电池在工作时,A电极的质量将_______ (填“增加”、“减小”或“不变”)。若该电池反应消耗了0.1mol H2SO4,则转移电子的数目为_______ (设NA为阿伏伽德罗常数的值)
(2)若A、B均为铂片,电解质溶液为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A极的电极反应式:__________________________ ;该电池工作一段时间后,溶液的碱性将___________ (填“增强”、“减弱”或“不变”)。

(1)若A为Pb,B为PbO2,电解质溶液为H2SO4溶液,电池的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。则该电池在工作时,A电极的质量将
(2)若A、B均为铂片,电解质溶液为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铅(Pb)与碳(C)为同主族元素,序数为82,是一种金属元素,常温下不溶于浓硫酸。可用作耐硫酸腐蚀、防电离辐射、蓄电池等的材料。铅的一种氧化物二氧化铅( )可以导电。
)可以导电。
(1)已知Pb原子核外共有6个电子层,写出Pb在周期表中的位置______ 。
(2)有一种Pb的核素含有126个中子,请用2X表示该核素的组成______ 。
(3)Pb的常见价态有+2、+4,且+2价更稳定, 可以与浓盐酸共热产生黄绿色气体,则反应的化学方程式为
可以与浓盐酸共热产生黄绿色气体,则反应的化学方程式为______ 。
(4)铅蓄电池是常见的______ 电池(填一次或二次),广泛用于汽车、电瓶车的供电装置。电池工作时总反应为: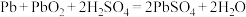 ,写出电池工作时负极的电极反应式
,写出电池工作时负极的电极反应式______ 。
 )可以导电。
)可以导电。(1)已知Pb原子核外共有6个电子层,写出Pb在周期表中的位置
(2)有一种Pb的核素含有126个中子,请用2X表示该核素的组成
(3)Pb的常见价态有+2、+4,且+2价更稳定,
 可以与浓盐酸共热产生黄绿色气体,则反应的化学方程式为
可以与浓盐酸共热产生黄绿色气体,则反应的化学方程式为(4)铅蓄电池是常见的
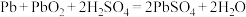 ,写出电池工作时负极的电极反应式
,写出电池工作时负极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示为氢氧燃料电池的原理示意图,回答下列问题:

(1)下列叙述不正确的是_______ (填标号)。
A.a电极是负极
B.b电极的电极反应式为4OH--4e-=O2↑+2H2O
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储存在电池内的新型发电装置
(2)若电解质溶液为KOH溶液,则电极反应式:a电极_______ ;b电极_______ 。
(3)若将氢气换成甲烷(CH4),电解质溶液仍为KOH溶液,则a电极的电极反应式为_______ 。

(1)下列叙述不正确的是
A.a电极是负极
B.b电极的电极反应式为4OH--4e-=O2↑+2H2O
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储存在电池内的新型发电装置
(2)若电解质溶液为KOH溶液,则电极反应式:a电极
(3)若将氢气换成甲烷(CH4),电解质溶液仍为KOH溶液,则a电极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氨气是一种重要工作原料,在工农业生产中具有重要的应用。
(1)已知:N2(g)+O2(g)="2NO(g) " △ H=180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
则N2(g)+3H2(g)=2NH3(g)的△H=_________________________ 。
(2)工业合成氨气的反应为N2(g)+3H2(g) 2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是
2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是__________________ 。
①增大压强 ②增大反应物的浓度 ③使用催化荆 ④降低温度
(3)①实验室常用加热氯化铵固体和氢氧化钙固体的混合物来制取氨气,写出反应的化学方程式___________________ 。实验室还可在_________ (填一种试剂)中滴加浓氨水的方法快速制取少量氨气。
②常温下氨气极易溶于水,溶液可以导电。氨水中水电离出的c(OH-)_______ 10-7mol·L-1(填写“>”、“<”或“=”);
③将相同体积、PH之和为14的氨水和盐酸混合后,溶液中离子浓度由大到小的顺序为_________________________ 。
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行图所示实验:(其中a、b均为碳棒)
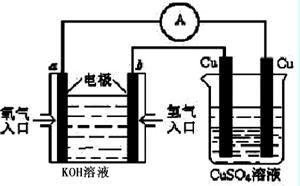
①氢氧燃料电池具有广阔的发展前景。如下图所示:
右边Cu电极反应式是__________________________ 。a电极的电极反应式_________________________
②工业上生产氢气是将水蒸气通过红热的炭,产生水煤气:
C(s) + H2O(g)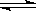 H2(g) + CO(g) △H=+131.3 kJ/mol
H2(g) + CO(g) △H=+131.3 kJ/mol
该反应在低温下不能自发进行的原因是_____ 。
A.△H>0 B.温度较低时,△H影响为主
C.△S<0 D.温度较低时,△S影响为主
(1)已知:N2(g)+O2(g)="2NO(g) " △ H=180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
则N2(g)+3H2(g)=2NH3(g)的△H=
(2)工业合成氨气的反应为N2(g)+3H2(g)
 2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是
2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是①增大压强 ②增大反应物的浓度 ③使用催化荆 ④降低温度
(3)①实验室常用加热氯化铵固体和氢氧化钙固体的混合物来制取氨气,写出反应的化学方程式
②常温下氨气极易溶于水,溶液可以导电。氨水中水电离出的c(OH-)
③将相同体积、PH之和为14的氨水和盐酸混合后,溶液中离子浓度由大到小的顺序为
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行图所示实验:(其中a、b均为碳棒)

①氢氧燃料电池具有广阔的发展前景。如下图所示:
右边Cu电极反应式是
②工业上生产氢气是将水蒸气通过红热的炭,产生水煤气:
C(s) + H2O(g)
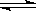 H2(g) + CO(g) △H=+131.3 kJ/mol
H2(g) + CO(g) △H=+131.3 kJ/mol该反应在低温下不能自发进行的原因是
A.△H>0 B.温度较低时,△H影响为主
C.△S<0 D.温度较低时,△S影响为主
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)按要求写出下列电极反应式
①氢氧燃料电池酸性环境下,负极反应式:___________ ,正极反应式:___________ 。
②氢氧燃料电池碱性环境下,负极反应式:___________ ,正极反应式:___________ 。
(2)铅酸蓄电池是常用的化学电源,其电极材料分别是 和
和 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。
①铅酸蓄电池的负极材料是___________ ,正极反应式为___________ 。
②电池工作时,溶液中 移向
移向___________ 极(填“正”或“负”)。
③电池工作时,电解质溶液的
___________ (填“增大”“减小”或“不变”)。
④若有 电子从负极流出,则参加反应的
电子从负极流出,则参加反应的 是
是___________  ,负极的质量变化是增大
,负极的质量变化是增大___________ g。
(1)按要求写出下列电极反应式
①氢氧燃料电池酸性环境下,负极反应式:
②氢氧燃料电池碱性环境下,负极反应式:
(2)铅酸蓄电池是常用的化学电源,其电极材料分别是
 和
和 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。①铅酸蓄电池的负极材料是
②电池工作时,溶液中
 移向
移向③电池工作时,电解质溶液的

④若有
 电子从负极流出,则参加反应的
电子从负极流出,则参加反应的 是
是 ,负极的质量变化是增大
,负极的质量变化是增大
您最近一年使用:0次



