禽流感病毒是一种没有超常抵抗力的病毒。研究证明,许多常用消毒药物如漂粉精、漂白粉、高锰酸钾等,可以将禽流感病毒杀灭。氯气与氢氧化钙充分反应,使次氯酸钙成为主要成分,得到漂粉精,其稳定性比漂白粉高。将漂粉精溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的离子方程式为___ 。另取少许上层清液,先滴加适量的____ (填化学式)酸化,再滴加_ (填化学式)溶液即可检验Cl-的存在,发生反应的离子方程式为___ 。再取少许上层清液,滴加几滴酚酞溶液,溶液呈红色,随后溶液迅速褪色,说明漂粉精溶液呈__ 性并具有___ 性。
更新时间:2021/03/14 22:37:11
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)要确定一瓶药品为氯化钠,可用焰色试验确定______ 的存在,用硝酸银溶液和稀硝酸确定______ 的存在。
(2)制取氢氧化铁胶体时应向沸腾的蒸馏水中滴加几滴______ 溶液,然后用激光笔来照射生成的胶体,并从侧面观察,这个实验叫______ 。
(3)实验室保存过氧化钠时应密封保存,主要是隔绝二氧化碳和______ 。
(2)制取氢氧化铁胶体时应向沸腾的蒸馏水中滴加几滴
(3)实验室保存过氧化钠时应密封保存,主要是隔绝二氧化碳和
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】H1N1病毒是一种病毒。研究证明,许多常用消毒药物如漂粉精、漂白粉、高锰酸钾等,可以将H1N1病毒杀灭。氯气与氢氧化钙溶液充分反应,得到以次氯酸钙[Ca(ClO)2]为主要成分的漂粉精,其稳定性比漂白粉高。将漂粉精溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的离子方程式为______________________________ 。另取少许上层清液,先滴加适量的硝酸酸化,再滴加________ (填化学式)溶液即可检验Cl-的存在,发生反应的离子方程式为____________________________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按如图的方法做“渗析”实验提纯淀粉胶体:在一个半透膜袋中装入由淀粉胶体和少量食盐溶液组成的液态分散系,将此袋系在玻璃棒上并浸入水槽里的蒸馏水中。
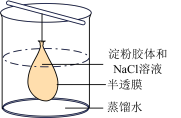
(1)约10 min后取水槽中的水约3 mL盛于洁净的试管中,并向试管内加少量AgNO3溶液发现有白色沉淀产生,再向试管中滴加足量稀硝酸后沉淀不溶解,生成白色沉淀的化学反应方程式是_____ ;另取水槽中的水约3 mL盛于另外一支洁净的试管中,并向试管内滴加少量碘水,未发现新现象,通过两项实验说明,不能透过半透膜的粒子是_______ 。
(2)检验是否达到渗析目的的操作方法是:不断更换水糟中的蒸馏水,更换若干次后,取少量_______ 于试管中,滴加_______ 溶液,若_______ ,则证明NaCl已完全除去。
(3)若半透膜破损,如何检验其破损,写出操作及现象_______ 。
(4)为尽可能全部除去淀粉溶液里的食盐,可采取的措施是_______ (填入正确选项前的字母)。
A.将半透膜放在有流水的水槽中进行渗析
B.多次渗析,每次用水量不要太多
C.换大烧杯,用大量水进行渗析

(1)约10 min后取水槽中的水约3 mL盛于洁净的试管中,并向试管内加少量AgNO3溶液发现有白色沉淀产生,再向试管中滴加足量稀硝酸后沉淀不溶解,生成白色沉淀的化学反应方程式是
(2)检验是否达到渗析目的的操作方法是:不断更换水糟中的蒸馏水,更换若干次后,取少量
(3)若半透膜破损,如何检验其破损,写出操作及现象
(4)为尽可能全部除去淀粉溶液里的食盐,可采取的措施是
A.将半透膜放在有流水的水槽中进行渗析
B.多次渗析,每次用水量不要太多
C.换大烧杯,用大量水进行渗析
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】漂白粉在生活、工业生产中用途广泛,漂白粉除了具有漂白作用外,还能杀菌消毒。2003年抗“非典”期间,各商场漂白粉及其他漂白产品曾一度脱销。
(1)用Cl2和石灰乳制作漂白粉的反应方程式_______________ ,其成分是_________ ,有效成分是_________ (填名称)。
(2)用Cl2和石灰乳制作漂白粉的目的是 ( )
(3)瓶装漂白粉久置空气中会失效。用化学方程式表示漂白粉在空气中易失效的原因:
①_______________________________ ;
②_______________________________ 。
(1)用Cl2和石灰乳制作漂白粉的反应方程式
(2)用Cl2和石灰乳制作漂白粉的目的是 ( )
| A.转变为较HClO稳定且易储运的物质 | B.转变为更易溶于水的物质 |
| C.提高氯气原利用率 | D.增强漂白能力 |
①
②
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】NaClO是“84”消毒液的有效成分,洁厕灵的主要成分是盐酸;
①NaClO中Cl元素的化合价是____________ ;
②浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因_______ (已知酸性:H2CO3>HClO> )
)
③若将“84”消毒液与洁厕灵混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是____________ 。
①NaClO中Cl元素的化合价是
②浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,结合离子方程式解释原因
 )
)③若将“84”消毒液与洁厕灵混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)工业上将氯气通入石灰乳[Ca(OH)2]中制取漂白粉,化学方程式为__________________________
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为_____________________
(3)食盐不慎洒落在天然气的火焰上,观察到的现象是_______ ,该变化称为_______ 试验。
(4)在淀粉KI溶液中加入少量的NaClO溶液,并加入少量的稀硫酸,溶液立即变蓝,该反应的离子方程式是_____________________
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学方程式为
(3)食盐不慎洒落在天然气的火焰上,观察到的现象是
(4)在淀粉KI溶液中加入少量的NaClO溶液,并加入少量的稀硫酸,溶液立即变蓝,该反应的离子方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】用离子方程式(不能用离子方程式的用化学方程式)解释下列实验事实
⑴用纸层析法分离Fe3+、Cu2+时,氨熏显色后出现蓝色斑点_______________________________________________________________________ 。
⑵用新制的氢氧化铜检验牙膏中的甘油______________________________________________________________________ 。
⑶用AgNO3溶液、稀硝酸和NaNO2溶液直接检验火柴头中的氯元素_______________________________________________________________________ 。
⑷用水杨酸和乙酸酐在酸性条件下制备阿司匹林________________________________________________________________________ 。
⑴用纸层析法分离Fe3+、Cu2+时,氨熏显色后出现蓝色斑点
⑵用新制的氢氧化铜检验牙膏中的甘油
⑶用AgNO3溶液、稀硝酸和NaNO2溶液直接检验火柴头中的氯元素
⑷用水杨酸和乙酸酐在酸性条件下制备阿司匹林
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)一种变色眼镜的镜片和普通照相感光胶片中含有卤化银.镜片变化是因 为卤化银在光的作用下发生化学反应,其反应式是_______ ,照相感光胶片曝光的化学反应是_______ .
(2)在我国干旱严重的华北地区,近年来利用飞机、高炮或火箭等运载工具向过冷支层中播撒碘化银(AgI)或干冰,实现人工增雨(或人工增雪),达到减灾的目的.下列有关人工增雨的评述中,你认为不甚理智的是_______ .
A.它对农业生产条件和大气环境的改善有一定的效益
B.它使用的碘化银中的重金属元素对土壤造成污染
C.它使用的 AgI 如换成干冰,可避免重金属元素对土壤的污染
D.它是人类彻底战胜自然的表现,体现了人类的力量是无穷的.
(2)在我国干旱严重的华北地区,近年来利用飞机、高炮或火箭等运载工具向过冷支层中播撒碘化银(AgI)或干冰,实现人工增雨(或人工增雪),达到减灾的目的.下列有关人工增雨的评述中,你认为不甚理智的是
A.它对农业生产条件和大气环境的改善有一定的效益
B.它使用的碘化银中的重金属元素对土壤造成污染
C.它使用的 AgI 如换成干冰,可避免重金属元素对土壤的污染
D.它是人类彻底战胜自然的表现,体现了人类的力量是无穷的.
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(I)现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有___ 。
(2)属于非电解质的有___ 。
(3)除去③中少量②的操作是___ ,化学方程式为___ 。
(4)若在⑦中缓慢加入①的水溶液,产生的现象是___ 。
(II)NaClO是“84”消毒液的有效成分。请回答下列问题。
(1)NaClO中Cl元素的化合价是________ ;
(2)用氢氧化钠溶液和氯气反应制备“84”消毒液,反应的离子方程式是________ 。
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是________ 。
(1)上述十种物质中,属于电解质的有
(2)属于非电解质的有
(3)除去③中少量②的操作是
(4)若在⑦中缓慢加入①的水溶液,产生的现象是
(II)NaClO是“84”消毒液的有效成分。请回答下列问题。
(1)NaClO中Cl元素的化合价是
(2)用氢氧化钠溶液和氯气反应制备“84”消毒液,反应的离子方程式是
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是
您最近一年使用:0次



