下图为四种粒子的结构示意图,完成以下填空:
A. B.
B.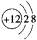 C.
C. D.
D.
(1)表示阳离子结构示意图的是___________ (填字母序号)。
(2)以上四种元素中的某元素R形成的氧化物为R2O3,则表示R的原子结构示意图的是(填字母序号)___________ 。
(3)A粒子的半径___________ B粒子的半径(填“大于”、“小于”或“等于”)。
(4)A粒子与B粒子形成的化合物是___________ 化合物(填“离子”或“共价”)。
A.
 B.
B.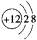 C.
C. D.
D.
(1)表示阳离子结构示意图的是
(2)以上四种元素中的某元素R形成的氧化物为R2O3,则表示R的原子结构示意图的是(填字母序号)
(3)A粒子的半径
(4)A粒子与B粒子形成的化合物是
更新时间:2021-03-17 08:24:49
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】现有六种微粒:
①镁原子;②硫离子;③氦原子;④核电荷数为+17,中子数为+18,核外有三个电子层,各层分别含有电子数为2,8,8;⑤核电荷数为+12,核外有两个电子层,各层含有电子数分别为2,8;⑥核电荷数为+17,质量数为37,核外有三个电子层,各层含有电子数分别为2,8,7。
(1)属于同种元素的是___________ ;
(2)核外电子排布相同的是___________ ;
(3)带电的微粒是___________ 。
①镁原子;②硫离子;③氦原子;④核电荷数为+17,中子数为+18,核外有三个电子层,各层分别含有电子数为2,8,8;⑤核电荷数为+12,核外有两个电子层,各层含有电子数分别为2,8;⑥核电荷数为+17,质量数为37,核外有三个电子层,各层含有电子数分别为2,8,7。
(1)属于同种元素的是
(2)核外电子排布相同的是
(3)带电的微粒是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期表是元素周期律的具体表现形式,是学习和研究化学的重要工具,下图是元素周期表的一部分。

(1)氧元素在周期表中的位置是第_______ 周期_______ 族,氧原子的电子式为_______ 。
(2)某元素的结构示意图为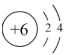 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号_______ 。
(3)元素性质呈现周期性变化的根本原因是_______。

(1)氧元素在周期表中的位置是第
(2)某元素的结构示意图为
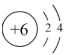 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号(3)元素性质呈现周期性变化的根本原因是_______。
| A.元素相对原子质量的递增 |
| B.元素原子半径呈现周期性变化 |
| C.元素原子核外电子排布呈现周期性变化 |
| D.元素金属性和非金属性呈现周期性变化 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】元素周期表的一部分,按要求完成各小题。
(1)金属性最强的单质与水反应的离子方程式为____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是____ 。
(3)①③⑤三种元素的原子半径由大到小的顺序为____ 。
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是____ 。向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是
(3)①③⑤三种元素的原子半径由大到小的顺序为
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】依据原子结构与元素周期表的知识,回答下列问题。
(1)比较原子半径大小:硫原子与氧原子_______ 、硫原子与磷原子_______ 。
(2)比较下列物质的酸性强弱:硝酸( )与磷酸(
)与磷酸( )
)_______ 、硫酸( )与高氯酸(
)与高氯酸( )
)_______ 。
(3)比较硫与氢气、氯气与氢气反应的剧烈程度_______ 。
(1)比较原子半径大小:硫原子与氧原子
(2)比较下列物质的酸性强弱:硝酸(
 )与磷酸(
)与磷酸( )
) )与高氯酸(
)与高氯酸( )
)(3)比较硫与氢气、氯气与氢气反应的剧烈程度
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氮化硅(Si3N4)陶瓷可代替金属制造发动机的耐热部件。工业上用气相沉淀法制备氨化硅: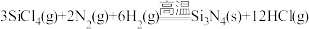 。请回答:
。请回答:
(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si___________ H(选填“<”或“>”)。
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是___________ 。
(3)氮化硅(Si3N4)的晶体类型为___________
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
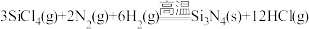 。请回答:
。请回答:(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是
(3)氮化硅(Si3N4)的晶体类型为
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
| A.是一种活泼的金属元素 |
| B.其电负性大于硫 |
| C.其单质可作为半导体材料 |
| D.其气态氢化物的稳定性低于硅的气态氢化物 |
您最近一年使用:0次



