下列叙述不正确的是
| A.影响化学反应速率的主要因素是反应物本身的性质 | B.反应速率是瞬时速率 |
| C.不能用固体物质表示反应速率 | D.温度是影响化学反应速率的一个外界因素 |
更新时间:2021-03-31 22:29:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法正确的是
| A.铁片与稀盐酸制取氢气时,加入NaNO3固体或Na2SO4固体都不影响生成氢气的速率 |
| B.加入反应物,单位体积内活化分子百分数增大,化学反应速率增大 |
| C.汽车尾气中NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢 |
| D.加入适宜的催化剂,非活化分子发生有效碰撞,化学反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列措施中,能够明显增大原反应化学反应速率的是
| A.在氨的催化氧化时,恒容条件下通入一定量的氮气 |
B.在利用Zn与 制取 制取 时,滴加少量硫酸铜溶液 时,滴加少量硫酸铜溶液 |
C.在 与NaOH溶液反应时,增大压强 与NaOH溶液反应时,增大压强 |
| D.在氯气与水反应时,增大水的用量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某实验小组为探究影响H2O2分解的因素设计表中实验,下列有关说法错误的是
| 溶液 | 温度 | 时间(收集50mLO2) | |
| ① | 10mL15%H2O2溶液 | 25℃ | 160s |
| ② | 10mL30%H2O2溶液 | 25℃ | 120s |
| ③ | 10mL15%H2O2溶液 | 50℃ | 50s |
| ④ | 10mL15%H2O2溶液+1mL5%FeCl3溶液 | 50℃ | 20s |
| A.实验①和②,可探究H2O2浓度对H2O2分解速率的影响 |
| B.实验①和③,可探究温度对H2O2分解速率的影响 |
| C.实验①和④,可探究催化剂对H2O2分解速率的影响 |
| D.由上述实验可知,增大H2O2浓度、升高温度都能加快H2O2分解速率 |
您最近一年使用:0次
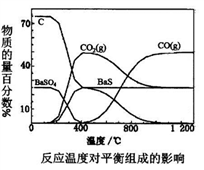
【推荐2】我国有世界储量第一的天然石膏(主要成分CaSO4),同时也有大量磷酸工业副产品石膏,可用于硫酸及水泥的联合生产。硫酸钙在高温下被CO还原,发生的反应有:
I.CaSO4(s)+4CO(g)⇌CaS(s)+4CO2(g) K1
II.CaSO4(s)+CO(g)⇌CaO(s)+SO2(g)+CO2(g) K2
III.3CaSO4(s)+CaS(s)⇌4CaO(s)+4SO2(g) K3
上述反应的平衡常数的对数值(lgK)与温度(T)的关系如图所示。下列说法错误的是( )
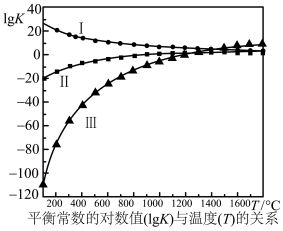
I.CaSO4(s)+4CO(g)⇌CaS(s)+4CO2(g) K1
II.CaSO4(s)+CO(g)⇌CaO(s)+SO2(g)+CO2(g) K2
III.3CaSO4(s)+CaS(s)⇌4CaO(s)+4SO2(g) K3
上述反应的平衡常数的对数值(lgK)与温度(T)的关系如图所示。下列说法错误的是( )

| A.反应II的△H>0 |
| B.lgK3=4lgK2−lgK1 |
| C.使用适当的催化剂能够加快反应速率,提高原料的平衡转化率 |
| D.调控适当的温度可以抑制反应I促进反应III而得到较纯净的CaO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某科研团队报道了一种新“光合作用”,即借助光将二氧化碳转化为甲烷的新型催化方法,其催化机理如图所示。下列关于该机理的说法错误的是
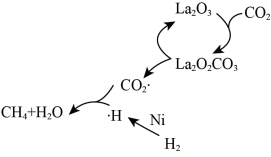
A. 是催化剂 是催化剂 |
| B.实现了光能转化为化学能 |
| C.有共价键的断裂与形成 |
D.总反应方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硫及其化合物之间的转化在生产中有重要作用。接触法制硫酸中, 制取
制取 的反应为
的反应为 (放热反应)。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
(放热反应)。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
 制取
制取 的反应为
的反应为 (放热反应)。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
(放热反应)。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是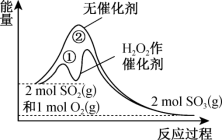
| A.该反应中存在极性共价键和非极性共价键的断裂和形成 |
B.使用催化剂能加快化学反应的速率并提高 的转化率 的转化率 |
C.达到化学平衡时, 的消耗速率和 的消耗速率和 的消耗速率相等 的消耗速率相等 |
D.使用 作催化剂时,温度越高,反应越快达到平衡 作催化剂时,温度越高,反应越快达到平衡 |
您最近一年使用:0次


 NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来

