下列有关说法正确的是
| A.铁片与稀盐酸制取氢气时,加入NaNO3固体或Na2SO4固体都不影响生成氢气的速率 |
| B.加入反应物,单位体积内活化分子百分数增大,化学反应速率增大 |
| C.汽车尾气中NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢 |
| D.加入适宜的催化剂,非活化分子发生有效碰撞,化学反应速率增大 |
更新时间:2020-01-24 10:11:45
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法不正确 的是
| A.增大反应物浓度,可增大单位体积内活化分子数目,从而使反应速率增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),不能增加活化分子的百分数 |
| C.活化分子间所发生的碰撞为有效碰撞 |
| D.升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子的百分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】黄鸣龙是唯一一个名字写进有机化学课本的中国人,Wolff-Kishner-黄鸣龙还原反应机理如下(R、R’均代表烃基),下列有关说法不正确的是


| A.肼的沸点高于氨气,原因是分子间氢键数目更多,且相对分子质量更大 |
| B.过程①发生加成反应,过程②、③均发生消去反应 |
C.过程④的反应历程可表示为: +OH— +OH—  +N2↑+H2O +N2↑+H2O |
D.应用该机理,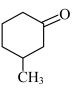 可以在碱性条件下转变为 可以在碱性条件下转变为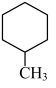 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A. 和 和 与 与 盐酸反应,反应速率相同 盐酸反应,反应速率相同 |
B. 盐酸与 盐酸与 溶液分别与大小、形状相同的大理石反应,反应速率相同 溶液分别与大小、形状相同的大理石反应,反应速率相同 |
| C.催化剂能降低分子活化时所需的能量,使单位体积内活化分子百分数增加 |
D. 盐酸与锌片反应,加入适量的 盐酸与锌片反应,加入适量的 溶液,反应速率不变 溶液,反应速率不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作、现象和解释或结论完全正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 分别向浓度为2 mol·L-1的盐酸和1 mol·L-1的硫酸中加入形状、质量相同的锌粒 | 盐酸中的锌粒表面产生气体的速率明显快 | 盐酸中的H+浓度大 |
| B | 除去氯化钠固体中的少量硝酸钾时,将固体溶于水,加热浓缩,降温结晶 | 析出大量固体 | 利用了硝酸钾的溶解度随温度变化大,而氯化钠变化小的特点 |
| C | 将甲烷,乙烯和氯化氢混合气体通入酸性高锰酸钾溶液中 | 紫色褪去 | 从高锰酸钾洗气瓶出来的气体含有甲烷、二氧化碳和少量未反应的氯化氢 |
| D | 量取10.00mL待测氢氧化钠溶液于锥形瓶中,加入2滴甲基橙,用0.10 mol·L-1盐酸滴定 | 滴加盐酸至10.00 mL时,锥形瓶内溶液颜色由黄色变为橙色,且半分钟内不变色 | 氢氧化钠溶液的浓度为0.10mol·L-1 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究小组用下图装置探究NaCl溶液对钢铁腐蚀的影响。

实验Ⅰ:向烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。
取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化。改变NaCl溶液的浓度继续实验,记录如下:
查阅资料:在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀。
下列说法不正确 的是:

实验Ⅰ:向烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。
取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化。改变NaCl溶液的浓度继续实验,记录如下:
| 实验 | a | b | 指针偏转方向 |
| Ⅱ | 0.1% | 0.01% | 向右 |
| Ⅲ | 0.1% | 3.5% | 向左 |
| Ⅳ | 3.5% | 饱和溶液 | 向右 |
下列说法
| A.实验Ⅰ加热后,指针发生偏转的原因可能是温度升高,Fe还原性增强,反应速率加快 |
| B.实验Ⅱ中b作正极 |
| C.甲同学由实验Ⅱ、Ⅲ、Ⅳ得出结论NaCl溶液的浓度越大,Fe越容易被腐蚀 |
| D.根据上述实验,对钢铁腐蚀有影响的因素是:温度、NaCl溶液的浓度、O2的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某研究欲利用甲烷消除NO2污染,CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)。在1L密闭容器中,控制不同温度,分别加入0.50 mol CH4和1.2 mol NO2,测得n(CH4)随时间变化的有关实验数据见表:
下列说法正确的是
组别 | 温度 | 时间 /min n /mol | 0 | 10 | 20 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 |
下列说法正确的是
| A.①组中,0~20 min内,用NO2表示的反应速率为0.0125 mol·Lˉ1·minˉ1 |
| B.由实验数据可知实验控制的温度T1<T2 |
| C.容器内混合气体的密度不变,说明反应已达到平衡状态 |
| D.若增大压强,则正反应速率加快,逆反应速率减慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.0 kJ·mol-1,下列有关说法正确的是
A.增大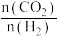 的值,可提高H2的转化率 的值,可提高H2的转化率 |
| B.升高温度能提高 CO2的反应速率和转化率 |
| C.达平衡时缩小容器体积,v(正)增大,v(逆)减小 |
| D.1 mol CO2和3 mol H2充分反应时放出的热量为 49.0 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
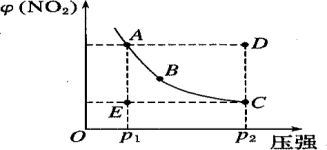
【推荐3】对于反应N2O4(g) 2NO2(g)在温度一定时,平衡体系中NO2 的体积分数φ (NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
2NO2(g)在温度一定时,平衡体系中NO2 的体积分数φ (NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
 2NO2(g)在温度一定时,平衡体系中NO2 的体积分数φ (NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
2NO2(g)在温度一定时,平衡体系中NO2 的体积分数φ (NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
| A.A、C 两点的正反应速率的关系为 A>C |
| B.A、B、C、D、E 各状态中,v(正)<v(逆)的是状态 E |
| C.维持 p1 不变,E→A 所需时间为 x;维持 p2 不变,D→C 所需时间为y,则 x<y |
| D.使E 状态从水平方向到达 C 状态,再沿平衡曲线到达A状态,从理论上来讲可选用的条件是从p1 突然加压至 p2,再由p2无限缓慢降压至p1 |
您最近一年使用:0次

 ,R.A.Ogg提出如下反应历程:
,R.A.Ogg提出如下反应历程: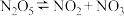



 与
与

