W、X、Y、Z 是原子序数依次增大的四种短周期元素。W 的气态氢化物能使紫色石蕊溶液变蓝,W、X和Y三种元素的最高价氧化物的水化物两两之间可以发生反应,W、X、Y、Z 的最外层电子数之和为 16。回答下列问题:
(1)Z 单质的电子式是__ 。W的气态氢化物能使紫色石蕊溶液变蓝的原因__ (用化学方程式表示)。
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是____ (用离子符号表示)。
(3)不能能证明Z的非金属性比W强的实验事实是____ (填字母)。
A.HZ的稳定性比WH3的稳定性性强
B.Z2与H2化合比W2与H2化合容易
C.HZ的水溶液酸性比WH3的水溶液酸性强
D.Z的最高价氧化物对应水化物的酸性比W强
(4)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式_ 。
(5) Y和Z两元素形成化合物中化学键的类型为____ 。
(6)用电子式表示X2O的形成过程____ 。
(7)砷(As)与W位于同一主族,下列推断正确的是_____ (填序号)。
①砷元素的最低负化合价为−3价
②砷的最高价氧化物对应的水化物属于酸
③热稳定性:AsH3>NH3
(1)Z 单质的电子式是
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是
(3)不能能证明Z的非金属性比W强的实验事实是
A.HZ的稳定性比WH3的稳定性性强
B.Z2与H2化合比W2与H2化合容易
C.HZ的水溶液酸性比WH3的水溶液酸性强
D.Z的最高价氧化物对应水化物的酸性比W强
(4)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式
(5) Y和Z两元素形成化合物中化学键的类型为
(6)用电子式表示X2O的形成过程
(7)砷(As)与W位于同一主族,下列推断正确的是
①砷元素的最低负化合价为−3价
②砷的最高价氧化物对应的水化物属于酸
③热稳定性:AsH3>NH3
更新时间:2021-04-09 23:10:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:

(1)地壳中含量居于第二位的元素是____ 。(填序号)
(2)②的最高价氧化物的分子式为___ ;⑦的最高价氧化物对应水化物的分子式为____ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___ (填字母)。
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为____ 。
②铯单质与H2O反应的化学反应方程式为____ 。
③预测铯单质的还原性比钠单质的还原性_____ (填“弱”或“强”)。
④下列推断正确的是____ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为___ 。

(1)地壳中含量居于第二位的元素是
(2)②的最高价氧化物的分子式为
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为
②铯单质与H2O反应的化学反应方程式为
③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、下表列出了①~⑦7种元素在周期表中的位置。
请回答下列问题:
(1)⑤的简单阴离子结构示意图为______ 。
(2)⑥的单质与⑦的简单阴离子反应的离子方程式为_____ 。
(3)④的氧化物与③的氢氧化物反应的化学方程式为______ 。
(4)①、②分别与氢元素组成含10个电子的阳离子的化学式分别为_____ 、______ 。
(5)铷被誉为“长眼睛”的金属,是本世纪最具潜力的光电材料,是因为铷最突出的特点在于它的原子核外电子很不稳定,可见光的能量足以使其原子电离。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置:第___________ 周期、第___________ 族。
ii.关于铷的下列说法中不正确的是___________ (填字母序号)。
a.与水反应比钠更剧烈 b.熔沸点高于钠 c.原子半径大于钾 d.金属性弱于钾
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | ① | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||
| 4 | ⑦ |
(1)⑤的简单阴离子结构示意图为
(2)⑥的单质与⑦的简单阴离子反应的离子方程式为
(3)④的氧化物与③的氢氧化物反应的化学方程式为
(4)①、②分别与氢元素组成含10个电子的阳离子的化学式分别为
(5)铷被誉为“长眼睛”的金属,是本世纪最具潜力的光电材料,是因为铷最突出的特点在于它的原子核外电子很不稳定,可见光的能量足以使其原子电离。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置:第
ii.关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈 b.熔沸点高于钠 c.原子半径大于钾 d.金属性弱于钾
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表列出了10种元素在元素周期表中的位置,请回答下列问题:
(1)写出元素①与⑦组成的分子的电子式:___________ ,画出⑦的离子结构示意图___________
(2)这10种元素中,化学性质最不活泼的是___________ (填元素符号,下同);②的简单气态氢化物与其最高价氧化物对应的水化物反应的化学方程式为___________ 。
(3)元素③④⑤的离子的半径由大到小的顺序为___________ (用离子符号表示);元素⑤⑨的最高价氧化物对应的水化物的碱性最强的是___________ (填化学式)。
(4)工业上用①的单质为原料在高温条件下生产⑥单质粗品的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 四 | ⑨ | ⑩ |
(2)这10种元素中,化学性质最不活泼的是
(3)元素③④⑤的离子的半径由大到小的顺序为
(4)工业上用①的单质为原料在高温条件下生产⑥单质粗品的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表的建立是化学发展史上的重要里程碑之一,部分元素在元素周期表中的位置如图:
(1)a、b、d、f、h五种元素原子的最外层电子数之和为_______ 。
(2)能比较得出h、j非金属性强弱的离子反应方程式为_______ (用化学符号表示,下同)。
(3)b、c、f、g四种元素简单离子中,半径最大的是_______ ,半径最小的是_______ 。
(4)写出d的最高价氧化物和b的最高价氧化物的水化物在水溶液中发生的离子反应方程式_______ 。
(5)比较e、g、h最高价含氧酸酸性强弱:_______ >_______ >_______ (写出具体物质化学式)。
| 族 周期 | ⅠA | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | f | ||||||
| 3 | b | c | d | e | g | h | |
| 4 | i | Ca | j |
(2)能比较得出h、j非金属性强弱的离子反应方程式为
(3)b、c、f、g四种元素简单离子中,半径最大的是
(4)写出d的最高价氧化物和b的最高价氧化物的水化物在水溶液中发生的离子反应方程式
(5)比较e、g、h最高价含氧酸酸性强弱:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素周期表体现了元素位置、结构和性质的关系,揭示了元素的内在联系。下表列出了①到⑧八种元素在周期表中的位置。
回答下列问题:
(1)元素①形成单质的电子式为_______ 。
(2)元素②的单质与水反应的离子方程式为_______ 。
(3)元素④⑤⑥的简单离子半径最大的是_______ (用离子符号表示)。
(4)用电子式表示元素③和元素⑥组成化合物的形成过程_______ 。
(5)元素④的单质与元素②最高价氧化物的水化物反应可以用于管道疏通,其原理为_______ (用离子方程式表示)。
(6)下列对元素⑦的说法正确的是_______ (填序号)。
a.原子最外层有6个电子
b.元素的非金属性:⑧>⑦
c.能形成 价的氧化物,该氧化物既有氧化性又有还原性
价的氧化物,该氧化物既有氧化性又有还原性
(7)从原子结构的角度解释元素⑥的非金属性强于元素⑤的原因_______ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 4 | ⑦ | ⑧ | ||||||
(1)元素①形成单质的电子式为
(2)元素②的单质与水反应的离子方程式为
(3)元素④⑤⑥的简单离子半径最大的是
(4)用电子式表示元素③和元素⑥组成化合物的形成过程
(5)元素④的单质与元素②最高价氧化物的水化物反应可以用于管道疏通,其原理为
(6)下列对元素⑦的说法正确的是
a.原子最外层有6个电子
b.元素的非金属性:⑧>⑦
c.能形成
 价的氧化物,该氧化物既有氧化性又有还原性
价的氧化物,该氧化物既有氧化性又有还原性(7)从原子结构的角度解释元素⑥的非金属性强于元素⑤的原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。

(1)在A、C、F、G四种元素中,非金属性最强的元素在周期表中的位置为_______ 。
(2)A、E、F三种元素的原子半径由大到小的顺序是_______ (填元素符号)。
(3)G元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是_______ 。
(4)元素C与D按原子个数比1∶1形成的化合物,其所含的化学键有_______ (填化学键类型)。
(5)下列事实能判断F和G的非金属性强弱的是_______ 。
①相同温度下,氢化物的溶解度大小
②氢化物的稳定性强弱
③最高价氧化物对应的水化物的酸性强弱

(1)在A、C、F、G四种元素中,非金属性最强的元素在周期表中的位置为
(2)A、E、F三种元素的原子半径由大到小的顺序是
(3)G元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是
(4)元素C与D按原子个数比1∶1形成的化合物,其所含的化学键有
(5)下列事实能判断F和G的非金属性强弱的是
①相同温度下,氢化物的溶解度大小
②氢化物的稳定性强弱
③最高价氧化物对应的水化物的酸性强弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)D在元素周期表中的位置是__ 。
(2)C2B的电子式是__ ;AB2的结构式是___ 。
(3)B、C、E的离子半径由大到小的顺序为___ (用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为___ 。
(4)B的气态氢化物与H2S相比沸点高的是__ (用化学式回答);原因是__ 。
(1)D在元素周期表中的位置是
(2)C2B的电子式是
(3)B、C、E的离子半径由大到小的顺序为
(4)B的气态氢化物与H2S相比沸点高的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E是原子序数依次增大的短周期元素,A、D在周期表中的相对位置如表,且元素A的最高正化合价与最低负化合价的绝对值相差2,B与D属于同主族元素;元素C是一种银白色金属,放置在空气中会迅速变暗。
(1)D的原子结构示意图为________
(2)元素E在元素周期表中位于第________ 族
(3)C、D、E离子半径的大小关系为_______ (用离子符号表示)
(4)元素B的单质与元素C的单质加热时生成化合物甲,化合物甲中所含化学键为___ ;试写出甲与水反应的离子方程式_____
(5)若乙是元素A的最简单气态氢化物,丙是元素C的最高价氧化物对应的水化物。
①pH相同的乙和丙的水溶液,分别用蒸馏水稀释到原来的x、y倍,稀释后两种溶液的pH仍然相同,则x______ y(填写“>”、“<”或“=” )
②在微电子工业中,乙的水溶液常用作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为_________ (不需要配平)。
| A | ||||
| D |
(2)元素E在元素周期表中位于第
(3)C、D、E离子半径的大小关系为
(4)元素B的单质与元素C的单质加热时生成化合物甲,化合物甲中所含化学键为
(5)若乙是元素A的最简单气态氢化物,丙是元素C的最高价氧化物对应的水化物。
①pH相同的乙和丙的水溶液,分别用蒸馏水稀释到原来的x、y倍,稀释后两种溶液的pH仍然相同,则x
②在微电子工业中,乙的水溶液常用作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。化合物F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如下图(图中部分产物未列出):

请填写下列空白:
(1)A是_______ ,C是_______ 。
(2)F的电子式_______ 。
(3)H与盐酸反应生成E的离子方程式是_______ 。
(4)E与F反应的化学方程式是_______ 。
(5)F与G的水溶液反应生成I和D的离子方程式是_______ 。

请填写下列空白:
(1)A是
(2)F的电子式
(3)H与盐酸反应生成E的离子方程式是
(4)E与F反应的化学方程式是
(5)F与G的水溶液反应生成I和D的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】卤族元素的单质能与H2反应
(1)用电子式表示HCl的形成过程_____________________________ 。
(2)依据上表,可以推测出:随着原子序数的递增,________ (填字母)。
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(3)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式___________________________________ 。
| H2+F2=2HF | 在暗处能剧烈化合并发生爆炸 |
| H2+Cl2=2HCl | 光照或点燃发生反应 |
| H2+Br2=2HBr | 加热至一定温度才能反应 |
| H2+I2=2HI | 不断加热才能缓慢反应,生成的HI会分解 |
(2)依据上表,可以推测出:随着原子序数的递增,
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(3)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期原子序数依次递增的 A、B、C、D、E、F 六种元素,已知B 原子最外层电子数是A 原子次外层电子数的 3 倍,是 D 原子最外层电子数的 2 倍;C 原子内层电子总数是最外层电子数 10 倍;A、B、D 三种元素的原子最外层电子数之和为 13; A 和B 原子最外层电子数之和与D 和 F 原子最外层电子数之和相等; E 和 F 是相邻元素。回答下列问题:
(1)E 元素的名称为__ ;其在元素周期表中的位置是__ 。
(2)AB2 的电子式为__ ;用电子式表示E 的氢化物的形成过程__ 。
(3)C 和 F 元素的最高价氧化物的水化物反应的化学方程式为__ ;
(4)B、C、D、F 四种元素原子半径由大到小的顺序是__ (填元素符号),离子半径最小的是__ (填离子符号)。
(5)B 和 E 的简单氢化物中沸点较高的是__ (填化学式),A 和B 的简单氢化物中稳定性较好的是__ (填化学式)。
(6)短周期元素M 与 D 元素位于不同主族,根据对角线规则二者某些性质相似。将 M 的最高价氧化物溶于 C 的最高价氧化物对应的水化物溶液中,发生反应的离子方程式为__ 。
(7)由 B、C 两种元素组成的化合物有两种,其中一种为淡黄色,该物质的电子式为__ 。
(1)E 元素的名称为
(2)AB2 的电子式为
(3)C 和 F 元素的最高价氧化物的水化物反应的化学方程式为
(4)B、C、D、F 四种元素原子半径由大到小的顺序是
(5)B 和 E 的简单氢化物中沸点较高的是
(6)短周期元素M 与 D 元素位于不同主族,根据对角线规则二者某些性质相似。将 M 的最高价氧化物溶于 C 的最高价氧化物对应的水化物溶液中,发生反应的离子方程式为
(7)由 B、C 两种元素组成的化合物有两种,其中一种为淡黄色,该物质的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有X、Y、Z、M、R、Q六种短周期主族元素,部分信息如下表所示:
回答下列问题:
(1)R在元素周期表中的位置为_______ 。
(2)根据表中数据推测,Y的原子半径的最小范围是_______ 。
(3)由元素Z、R组成的化合物属于_______ (填“离子”或“共价”)化合物。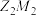 的电子式为
的电子式为_______ 。
(4)下列事实能作为比较元素Y与R的非金属性强弱依据的是_______(填字母)。
(5)以Q、Mg为电极材料,Z的最高价氧化物对应的水化物为电解质溶液,将两电极用导线相连插入该电解质溶液中可形成原电池,该电池中正极材料为_______ ,负极的电极反应式为_______ 。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4、+4 | -2 | -1、+7 | +3 | ||
| 其它信息 | 某种核素无中子 | 常用的半导体材料 | 短周期主族元素中原子半径最大 |
(1)R在元素周期表中的位置为
(2)根据表中数据推测,Y的原子半径的最小范围是
(3)由元素Z、R组成的化合物属于
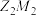 的电子式为
的电子式为(4)下列事实能作为比较元素Y与R的非金属性强弱依据的是_______(填字母)。
| A.常温下Y的单质呈固态,R的单质呈气态 |
B.稳定性: |
| C.Y与R形成的化合物中Y呈正价 |
D.酸性: |
您最近一年使用:0次



