(1)依据反应: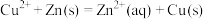 设计的原电池如图所示。
设计的原电池如图所示。
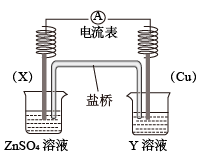
①电极X的材料是________ ;Y溶液可以是________ 溶液。
②电池放电过程中,盛有饱和 琼脂溶胶的盐桥中,向
琼脂溶胶的盐桥中,向 溶液扩散的离子是
溶液扩散的离子是________ (填离子符号)。
(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防护。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:_________ 。
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图所示的方案:
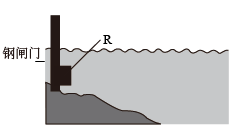
其中连接在铁闸门上的固体材料R可以采用________ (填写字母序号)。
a.铜 b.钠 c.锌 d.石墨
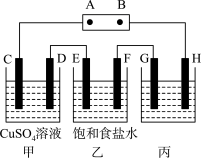
(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
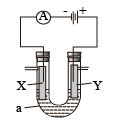
①若X、Y都是惰性电极,a是饱和 溶液,则电解的总反应式为
溶液,则电解的总反应式为________________ 。
②当电路中流通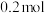 电子时,整个装置共放出气体
电子时,整个装置共放出气体________ L(标准状况下)。
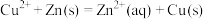 设计的原电池如图所示。
设计的原电池如图所示。
①电极X的材料是
②电池放电过程中,盛有饱和
 琼脂溶胶的盐桥中,向
琼脂溶胶的盐桥中,向 溶液扩散的离子是
溶液扩散的离子是(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防护。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图所示的方案:

其中连接在铁闸门上的固体材料R可以采用
a.铜 b.钠 c.锌 d.石墨
(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。

①若X、Y都是惰性电极,a是饱和
 溶液,则电解的总反应式为
溶液,则电解的总反应式为②当电路中流通
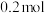 电子时,整个装置共放出气体
电子时,整个装置共放出气体
20-21高二下·广西钦州·阶段练习 查看更多[3]
广西钦州市浦北县浦北中学2020-2021学年高二3月月考化学试题(已下线)作业13 金属的腐蚀与防护-2021年高二化学暑假作业(人教版2019)重庆市巫山县官渡中学2020-2021年高二下学期第二次月考化学试题
更新时间:2021-04-13 12:04:02
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:___ 。当线路中转移0.4mol电子时,则被腐蚀铜的质量为:____ g。(已知:铜的相对原子量是64)
(2)将铝片和铜片用导线相连,一组插入溶液氢氧化钠中,一组插入浓硝酸中,分别形成了原电池,在这两个原电池中,负极分别为____ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

该酸式氢氧燃料电池的负极电极反应式是____ ,正极电极反应式是____ ,电池工作一段时间后电解质溶液pH___ (填“增大”“减小”或“不变”)。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为:
(2)将铝片和铜片用导线相连,一组插入溶液氢氧化钠中,一组插入浓硝酸中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

该酸式氢氧燃料电池的负极电极反应式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】小组合作,根据要求设计一个简单的原电池
| 设计思路及依据 | 实验装置 | 实验现象 | |
| Zn+2H+=Zn2++H2↑ |  | ||
| 确定 负极 | 选择负极反应物: | ||
| 选择负极材料: | |||
| 确定 正极 | 选择正极反应物: | ||
| 选择正极材料: | |||
| 构成闭 合回路 | 选择离子导体: | ||
| 选择电子导体: | |||
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】人们应用原电池原理制作了多种电池,以满足不同的需要。请回答下列问题。
(1)请你利用下列反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池,并回答下列问题:
①该电池的负极材料是___ ,电解质溶液是__ 。
②在外电路中,电子方向是从___ 极到____ 极。
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池。在这两个原电池中,负极分别为___ 。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将__ 能转化为__ 能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。在紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O 2Ag+Zn(OH)2,其负极的电极反应式为
2Ag+Zn(OH)2,其负极的电极反应式为__ 。
(4)目前正在研发的高能量密度燃料电池车,是以肼(N2H4)燃料电池作为动力来源,电池结构如图所示。
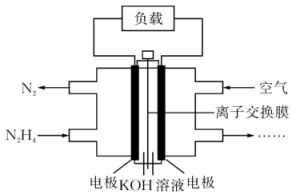
①起始时正极区与负极区KOH溶液浓度相同,工作一段时间后,KOH浓度较大的是___ (填“正”或“负”)极区。
②该电池负极的电极反应式为___ 。
(1)请你利用下列反应Cu+2Ag+=2Ag+Cu2+设计一个化学电池,并回答下列问题:
①该电池的负极材料是
②在外电路中,电子方向是从
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池。在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将
 2Ag+Zn(OH)2,其负极的电极反应式为
2Ag+Zn(OH)2,其负极的电极反应式为(4)目前正在研发的高能量密度燃料电池车,是以肼(N2H4)燃料电池作为动力来源,电池结构如图所示。

①起始时正极区与负极区KOH溶液浓度相同,工作一段时间后,KOH浓度较大的是
②该电池负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】金属腐蚀的分类
(1)金属腐蚀:金属或合金与周围的气体或液体发生_______ 反应而引起损耗的现象。
(2)化学腐蚀:金属与其表面接触的一些物质_______ 反应而引起的腐蚀。
(3)电化学腐蚀
①概念:_______ 的金属与_______ 接触时发生_______ 反应,_______ 的金属发生氧化反应而被腐蚀。
②分类:根据腐蚀过程中电解质溶液的不同,可分为_______ 腐蚀和_______ 腐蚀两种。
(1)金属腐蚀:金属或合金与周围的气体或液体发生
(2)化学腐蚀:金属与其表面接触的一些物质
(3)电化学腐蚀
①概念:
②分类:根据腐蚀过程中电解质溶液的不同,可分为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。

①红墨水柱两边的液面变为左低右高,则_______ (填“a”或“b”)试管内盛有食盐水。
②a试管中铁发生的是_______ (填“析氢”或“吸氧”)腐蚀,生铁中碳上发生的电极反应式为_______ 。
(2)如图两个图都是金属防护的例子。
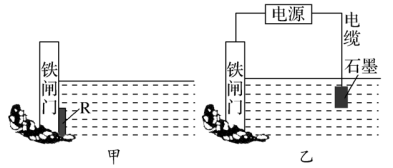
①为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用_______ (填字母),此方法叫做_______ 保护法。
A.铜 B.钠 C.锌 D.石墨
②图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的_______ (填“正”或“负”)极。
③以上两种方法中,_______ 填“甲”或“乙”)方法能使铁闸门保护得更好。
(1)如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。

①红墨水柱两边的液面变为左低右高,则
②a试管中铁发生的是
(2)如图两个图都是金属防护的例子。

①为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
②图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的
③以上两种方法中,
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下列事实中,与电化学腐蚀无关的是________
A.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀
B.金属钠置于空气中表面变暗
C.镀银的铁制品,镀层部分受损后,露出的铁表面更易被腐蚀
D.黄铜(铜锌合金)制作的铜锣不易产生铜绿
E.生铁比软铁芯(几乎是纯铁)容易生锈
F.铁制器件附有铜制配件,在接触处易生铁锈
A.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀
B.金属钠置于空气中表面变暗
C.镀银的铁制品,镀层部分受损后,露出的铁表面更易被腐蚀
D.黄铜(铜锌合金)制作的铜锣不易产生铜绿
E.生铁比软铁芯(几乎是纯铁)容易生锈
F.铁制器件附有铜制配件,在接触处易生铁锈
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】日常生产、生活中用到许多金属制品,从实用美观角度考虑选择下列合适的金属材料或保护(防腐蚀)方法,将序号填入下表相应空格中。
①不锈钢 ②白铁(镀锌铁皮) ③铝合金 ④镀铬铁管 ⑤涂漆 ⑥镶嵌锌块 ⑦与直流电源负极相连(阴极保护法)
①不锈钢 ②白铁(镀锌铁皮) ③铝合金 ④镀铬铁管 ⑤涂漆 ⑥镶嵌锌块 ⑦与直流电源负极相连(阴极保护法)
| 用途 | 选用材料或保护方法 |
| 菜刀 | |
| 楼梯扶手或阳台护栏 | |
| 水桶 | |
| 航海轮船 | |
| 水闸 | |
| 吊车塔架 | |
| 房门窗框 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】如图所示为在直流电源的作用下电解CuSO4溶液的装置,其中A、B为石墨电极,a、b为电源的两极,当接通电源,通电一段时间后,将B电极取出,洗干净并干燥后称量,其质量增加了3.2g,则:
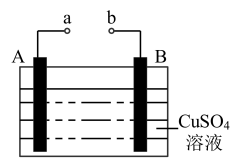
(1)a电极为电源的___ 极。
(2)写出电极反应式:A极___ ,B极__ 。
(3)若要使反应后的溶液恢复到原来状态,则应该加入__ ,加入__ g。

(1)a电极为电源的
(2)写出电极反应式:A极
(3)若要使反应后的溶液恢复到原来状态,则应该加入
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)。污染跟冬季燃煤密切相关,SO2.CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式_________________ 。
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g) CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
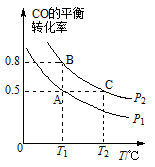
①下列说法不能判断该反应达到化学平衡状态的是____ (填字母)。
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA____ PB(填“>”“<”或“=”)。
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=________ L。
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图: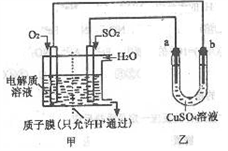
①该电池的负极反应:___________________ ;
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重____ g。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g)
 CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①下列说法不能判断该反应达到化学平衡状态的是
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重
您最近一年使用:0次