化合物X是一种黄色晶体(含结晶水),无水X由四种元素组成,X晶体的摩尔质量在400~500 。取12.66gX晶体完成如图实验,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B溶液保存时需加酸和F,C盐溶液的焰色反应是紫色,H是能使湿润的红色石蕊试纸变蓝的气体。(气体体积已转化为标准状况下的体积)
。取12.66gX晶体完成如图实验,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B溶液保存时需加酸和F,C盐溶液的焰色反应是紫色,H是能使湿润的红色石蕊试纸变蓝的气体。(气体体积已转化为标准状况下的体积)
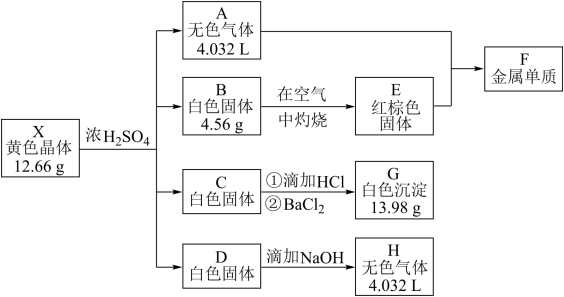
请回答:
(1)组成无水X的四种元素是_______ (填元素符号),X晶体的化学式是_______ 。
(2)X晶体与浓硫酸反应的化学方程式为_______ 。
(3)无水X可被 氧化成一种红色晶体Y,X与Y的组成元素相同,其反应的化学方程式为
氧化成一种红色晶体Y,X与Y的组成元素相同,其反应的化学方程式为_______ 。
(4)可利用X来鉴别 和
和 ,原因是
,原因是_______ 。
(5)设计实验方案检验B在空气中灼烧的产物:_______ 。
 。取12.66gX晶体完成如图实验,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B溶液保存时需加酸和F,C盐溶液的焰色反应是紫色,H是能使湿润的红色石蕊试纸变蓝的气体。(气体体积已转化为标准状况下的体积)
。取12.66gX晶体完成如图实验,其中A为无色有毒气体,B、C、D是三种酸根相同的盐,B溶液保存时需加酸和F,C盐溶液的焰色反应是紫色,H是能使湿润的红色石蕊试纸变蓝的气体。(气体体积已转化为标准状况下的体积)
请回答:
(1)组成无水X的四种元素是
(2)X晶体与浓硫酸反应的化学方程式为
(3)无水X可被
 氧化成一种红色晶体Y,X与Y的组成元素相同,其反应的化学方程式为
氧化成一种红色晶体Y,X与Y的组成元素相同,其反应的化学方程式为(4)可利用X来鉴别
 和
和 ,原因是
,原因是(5)设计实验方案检验B在空气中灼烧的产物:
2021·浙江·模拟预测 查看更多[4]
(已下线)浙江省“超级全能生”2021年3月高考选考科目联考(B卷)化学试题(已下线)【浙江新东方】高中化学20210621-008【2021】【高三下】(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)
更新时间:2021-04-20 15:18:13
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】X是一种由4种短周期元素组成含结晶水的盐。某兴趣小组按如下流程进行实验(所用试剂均足量):
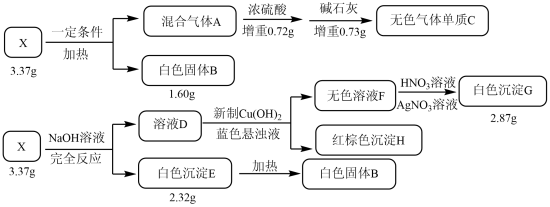
其中:X微溶于水。溶液D中仅有一种溶质。红棕色沉淀H是一种钠盐。请回答:
(1)组成X的元素有_______ ,X的化学式为_______ 。
(2)无色溶液F中的溶质是(用化学式表示):_______ 。
(3)上图生红棕色沉淀H时,溶液D中的溶质与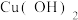 的物质的量之比为1:2,则其离子反应方程式是
的物质的量之比为1:2,则其离子反应方程式是_______ 。
(4)设计实验验证溶液D中的阴离子_______ 。

其中:X微溶于水。溶液D中仅有一种溶质。红棕色沉淀H是一种钠盐。请回答:
(1)组成X的元素有
(2)无色溶液F中的溶质是(用化学式表示):
(3)上图生红棕色沉淀H时,溶液D中的溶质与
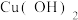 的物质的量之比为1:2,则其离子反应方程式是
的物质的量之比为1:2,则其离子反应方程式是(4)设计实验验证溶液D中的阴离子
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】中学化学中几种常见物质的转化关系如下:
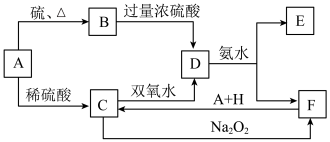
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:___________________________________ 。
(2)写出B的化学式:B________ 。
(3)①H2O2分子的电子式:__________________________________ 。
②写出C的酸性溶液与双氧水反应的离子方程式:_________________________ 。
(4)写出鉴定E中阳离子的实验方法和现象:____________________________ 。
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:______________________________________________________ 。

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:
(2)写出B的化学式:B
(3)①H2O2分子的电子式:
②写出C的酸性溶液与双氧水反应的离子方程式:
(4)写出鉴定E中阳离子的实验方法和现象:
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】某固体样品中含有的离子由 中的若干种组成,取适量该固体进行如下实验:
中的若干种组成,取适量该固体进行如下实验:

实验中气体均全部逸出,固体A、D、E均为纯净物。回答下列问题:
(1)固体E中所含物质的化学式为___________ 。
(2)可用___________ 检验气体C,现象是___________ 。
(3)1.97gBaCO3在空气中高温充分灼烧得到1.69g固体,经检验没有产生有毒气体,写出高温灼烧时发生反应的化学方程式:___________ 。
(4)100mL无色溶液A中 =
=___________ ,固体样品中 =
=___________ 。
(5)当m>___________ 时,100mL无色溶液A中会含有Cl-,此时c(Cl-)=___________ (用含m的代数式表示)。
 中的若干种组成,取适量该固体进行如下实验:
中的若干种组成,取适量该固体进行如下实验:
实验中气体均全部逸出,固体A、D、E均为纯净物。回答下列问题:
(1)固体E中所含物质的化学式为
(2)可用
(3)1.97gBaCO3在空气中高温充分灼烧得到1.69g固体,经检验没有产生有毒气体,写出高温灼烧时发生反应的化学方程式:
(4)100mL无色溶液A中
 =
= =
=(5)当m>
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
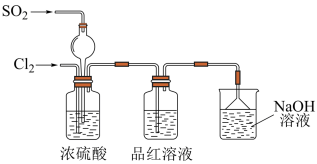
【推荐1】某学习小组设计了如图装置用于制取SO2并验证其性质。

(1)仪器a的名称为_______ ,实验时装置E中反应的离子方程式为_______ 。
(2)若装置B中溶液无明显现象,装置C中溶液红色褪去,则使品红的水溶液褪色的含硫微粒一定不是_______ (填化学式)。
(3)该实验小组的甲、乙两位同学为了进一步探究SO2的漂白性,按下图装置继续进行实验并记录相关实验现象。请根据下表中实验现象做出合理解释。
(4)该实验小组的学生丙预测装置D中没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。为进一步探究产生沉淀的原因,分别用煮沸和未煮沸过的蒸馏水配制的Ba(NO3)2和BaCl2溶液,进行如图实验:
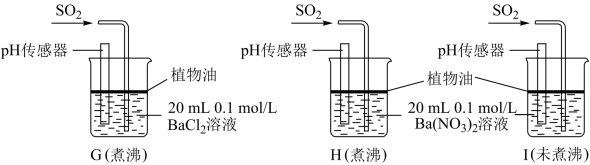
实验中G、H、I烧杯中观察到的现象如表:
①据G中现象推测D中产生的白色沉淀的化学式是_______ 。
②据I中出现白色沉淀的速率比H中快很多 的现象,推测其根本原因可能是_______ 。
(5)该实验小组的学生丁用200ml0.1mol·L-1酸性KMnO4溶液测定空气中SO2含量,若气体流速为acm3·min-1,当时间为tmin时酸性KMnO4溶液恰好褪色,则空气中SO2的含量为_______ (g·cm-3)。

(1)仪器a的名称为
(2)若装置B中溶液无明显现象,装置C中溶液红色褪去,则使品红的水溶液褪色的含硫微粒一定不是
(3)该实验小组的甲、乙两位同学为了进一步探究SO2的漂白性,按下图装置继续进行实验并记录相关实验现象。请根据下表中实验现象做出合理解释。

| 组别 | 实验现象 | 合理解释 |
| 甲 | 品红溶液几乎不褪色 | 反应离子方程式为 |
| 乙 | 品红溶液随时间的推移变得越来越浅 | 原因可能是 |
(4)该实验小组的学生丙预测装置D中没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。为进一步探究产生沉淀的原因,分别用煮沸和未煮沸过的蒸馏水配制的Ba(NO3)2和BaCl2溶液,进行如图实验:

实验中G、H、I烧杯中观察到的现象如表:
| 烧杯 | 实验现象 |
| G | 无白色沉淀产生,pH传感器测的溶液pH=5.3 |
| H | 有白色沉淀产生 |
| I | 有白色沉淀产生,I中出现白色沉淀比H中快很多 |
②据I中出现白色沉淀的速率比H中
(5)该实验小组的学生丁用200ml0.1mol·L-1酸性KMnO4溶液测定空气中SO2含量,若气体流速为acm3·min-1,当时间为tmin时酸性KMnO4溶液恰好褪色,则空气中SO2的含量为
您最近一年使用:0次
【推荐2】X是由四种短周期元素组成的纯净物,合结晶水,相对分子量范围: 105~230,它是工业上重要的还原性漂白剂,也是重要的食品抗氧化剂,现将X按如图流程实验,气体A到气体B质量减轻7.2 g。气体B能使品红溶液褪色,固体B中含两种固体(两种固体所含元素相同),溶液D焰色反应呈黄色。(气体体积均为标况下体积)。
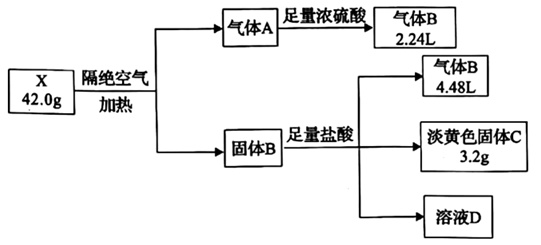
(1)X中含有的非金属元素有_______ (填写元素符号)。
(2)写出x隔绝空气加热的化学方程式_______ 。
(3)X溶液暴露于空气中易吸收氧气而被氧化成一种酸式盐,请写出离子方程式_______ 。
(4)关于气体B使品红水溶液褪色的原因,一般认为B不能使品红褪色,而是B与水反应的生成物使品红褪色。请设计实验证明_______ 。

(1)X中含有的非金属元素有
(2)写出x隔绝空气加热的化学方程式
(3)X溶液暴露于空气中易吸收氧气而被氧化成一种酸式盐,请写出离子方程式
(4)关于气体B使品红水溶液褪色的原因,一般认为B不能使品红褪色,而是B与水反应的生成物使品红褪色。请设计实验证明
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
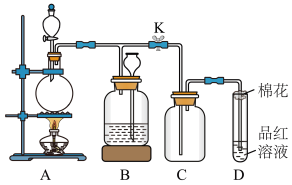
【推荐3】某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行相关实验。
请回答:
(1)装置 A 中发生的化学反应方程式为________________________ 。
(2)装置 D 中试管口放置的棉花中可以浸上NaOH溶液, 其作用是_____________ 。
(3)装置 B 的作用是贮存多余的气体。当 D 处有明显的现象后,关闭旋塞 K 并移去酒精灯。B 中应放置的液体是(填字母)____ 。
a.水 b.酸性 KMnO4溶液 c.饱和 NaHSO3溶液 d.浓溴水
(4)实验中,取一定质量的铜片和一定体积 18 mol·L—1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。有一定量的余酸但未能使铜片完全溶解,你认为可能的原因是____________ 。

请回答:
(1)装置 A 中发生的化学反应方程式为
(2)装置 D 中试管口放置的棉花中可以浸上NaOH溶液, 其作用是
(3)装置 B 的作用是贮存多余的气体。当 D 处有明显的现象后,关闭旋塞 K 并移去酒精灯。B 中应放置的液体是(填字母)
a.水 b.酸性 KMnO4溶液 c.饱和 NaHSO3溶液 d.浓溴水
(4)实验中,取一定质量的铜片和一定体积 18 mol·L—1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。有一定量的余酸但未能使铜片完全溶解,你认为可能的原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________ 、B___________ 、C____________ 、
F___________ 、H___________ 、乙____________ 。
(2)写出下列反应离子方程式:
反应①______________________
反应⑥_____________________

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
F
(2)写出下列反应离子方程式:
反应①
反应⑥
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知A、B、C、D、E、F、G为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,G为红褐色固体。常温下甲、乙、丙为单质气体,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如图所示(有的反应部分产物已经略去)
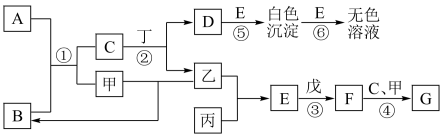
(1)试写出C与丁反应的离子方程式___________
(2)①到⑥的反应中属于氧化还原反应的是___________ 、反应①中每生成标况下22.4L的甲气体时,转移的电子数为___________
(3)检验溶液中是否含有F物质的阳离子的实验操作是___________
(4)试写出D与少量的E反应的离子方程式___________
(5)利用NaClO在碱性条件的强氧化性将G氧化可以用来制备高效净水剂 ,其中NaClO被还原为
,其中NaClO被还原为 ,现制取
,现制取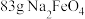 ,消耗NaClO
,消耗NaClO___________ mol

(1)试写出C与丁反应的离子方程式
(2)①到⑥的反应中属于氧化还原反应的是
(3)检验溶液中是否含有F物质的阳离子的实验操作是
(4)试写出D与少量的E反应的离子方程式
(5)利用NaClO在碱性条件的强氧化性将G氧化可以用来制备高效净水剂
 ,其中NaClO被还原为
,其中NaClO被还原为 ,现制取
,现制取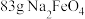 ,消耗NaClO
,消耗NaClO
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】下图是元素周期表的一部分。
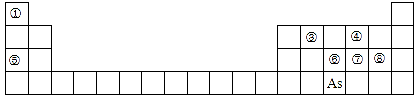
Ⅰ.(1)④、⑤、⑧的离子半径由大到小的顺序为_________ (用离子符号表示)。
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______ 。(用化学式表示)
(3) 由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂,
由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂, 可与
可与 的水溶液反应,产物有
的水溶液反应,产物有 的最高价含氧酸,该反应的化学方程式为
的最高价含氧酸,该反应的化学方程式为_______________ 。
Ⅱ.以下框图中的物质均为中学中常见的化合物或单质(部分产物略去),已知化合物 为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
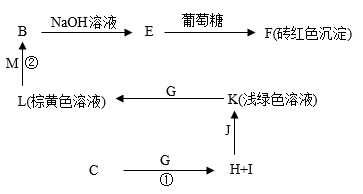
(1)化合物 的电子式为
的电子式为______________ , 的化学式为
的化学式为____________ 。
(2)写出反应①和反应②的离子方程式
①________________________________________ 。
②________________________________________ 。

Ⅰ.(1)④、⑤、⑧的离子半径由大到小的顺序为
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)
 由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂,
由④⑤⑧三种元素组成,它的水溶液是生活中常见的消毒剂, 可与
可与 的水溶液反应,产物有
的水溶液反应,产物有 的最高价含氧酸,该反应的化学方程式为
的最高价含氧酸,该反应的化学方程式为Ⅱ.以下框图中的物质均为中学中常见的化合物或单质(部分产物略去),已知化合物
 为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
为由以上①④两种元素组成的人类生命活动不可缺少的常见液态物质,试回答
(1)化合物
 的电子式为
的电子式为 的化学式为
的化学式为(2)写出反应①和反应②的离子方程式
①
②
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】菱铁矿 主要成分是
主要成分是 是炼铁的原料.已知
是炼铁的原料.已知 为白色固体,不溶于水,在干燥空气中稳定,潮湿环境中需较长时间被氧化为
为白色固体,不溶于水,在干燥空气中稳定,潮湿环境中需较长时间被氧化为 .
.
I. 甲同学取一定量碳酸亚铁固体于烧杯中,加入足量水,将烧杯放置在天平左盘上,向右盘放入砝码至天平平衡.放置较长时间后
甲同学取一定量碳酸亚铁固体于烧杯中,加入足量水,将烧杯放置在天平左盘上,向右盘放入砝码至天平平衡.放置较长时间后 不考虑水分蒸发
不考虑水分蒸发 ,观察到天平的指针会
,观察到天平的指针会______  填“偏左”、“偏右”、“不发生偏转”
填“偏左”、“偏右”、“不发生偏转” ;放置过程中还可观察到的实验现象为
;放置过程中还可观察到的实验现象为______ .
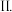 乙同学设计图1所示的装置制备
乙同学设计图1所示的装置制备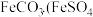 和
和 溶液均用经煮沸后冷却的蒸馏水配制,并在
溶液均用经煮沸后冷却的蒸馏水配制,并在 溶液中加入少量铁粉
溶液中加入少量铁粉 滴加
滴加 溶液后观察到试管中出现白色沉淀,同时有大量无色气体生成.
溶液后观察到试管中出现白色沉淀,同时有大量无色气体生成.

 产生的气体是
产生的气体是______  填分子式
填分子式 .
.
 丙同学对白色沉淀的成分提出异议,并做出如下假设,请补充完成假设3:
丙同学对白色沉淀的成分提出异议,并做出如下假设,请补充完成假设3:
假设1:白色沉淀是 ;
;
假设2:白色沉淀是 ;
;
假设3:白色沉淀是______ .
 若假设1成立,写出有关反应的化学方程式:
若假设1成立,写出有关反应的化学方程式:______ .
 若假设2成立,说明用经煮沸后冷却的蒸馏水配制
若假设2成立,说明用经煮沸后冷却的蒸馏水配制 和
和 溶液的目的是
溶液的目的是______ .请设计一个实验方案验证假设2成立,写出实验步骤、预期现象和结论,实验所需仪器和药品自选. ______ .
 现取
现取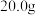 菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图2所示.
菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图2所示. 假设菱铁矿中杂质不参加反应,且难溶于水.
假设菱铁矿中杂质不参加反应,且难溶于水.
 菱铁矿中
菱铁矿中 的质量分数为
的质量分数为______
 若将稀硫酸改成1mol
若将稀硫酸改成1mol  ,则该反应的离子方程式为
,则该反应的离子方程式为______  将反应逸出的气体与一定量的
将反应逸出的气体与一定量的 混合循环通入反应液中,目的是
混合循环通入反应液中,目的是______ .
 某铁锈成分为
某铁锈成分为 和
和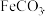 为确定其组成,兴趣小组称取此铁锈样品
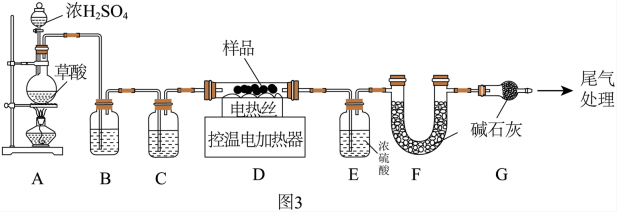
为确定其组成,兴趣小组称取此铁锈样品 ,在科研人员的指导下用图3装置进行实验.
,在科研人员的指导下用图3装置进行实验.
【查阅资料】
① 失去结晶水温度为
失去结晶水温度为 ,
, 在
在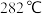 分解为FeO和
分解为FeO和 .
.
②温度高于 时铁的氧化物才能被CO还原.
时铁的氧化物才能被CO还原.
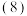 装配好实验装置后,首先要
装配好实验装置后,首先要______ .
 装置A中的反应为:
装置A中的反应为:
 草酸)
草酸) 
 通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放
通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放______  选填序号
选填序号 .
.
 浓硫酸
浓硫酸 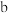 澄清的石灰水
澄清的石灰水  氢氧化钠溶液
氢氧化钠溶液
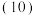 现控制D装置中的温度为
现控制D装置中的温度为 对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重
对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重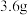 ,装置F增重
,装置F增重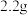 .则样品中
.则样品中 的质量
的质量
______ g,
______ .
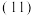 若缺少G装置,测得的
若缺少G装置,测得的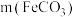
______  选填“偏大”、“偏小”、“不变”,下同
选填“偏大”、“偏小”、“不变”,下同 ,x的值会
,x的值会______ .
 主要成分是
主要成分是 是炼铁的原料.已知
是炼铁的原料.已知 为白色固体,不溶于水,在干燥空气中稳定,潮湿环境中需较长时间被氧化为
为白色固体,不溶于水,在干燥空气中稳定,潮湿环境中需较长时间被氧化为 .
.I.
 甲同学取一定量碳酸亚铁固体于烧杯中,加入足量水,将烧杯放置在天平左盘上,向右盘放入砝码至天平平衡.放置较长时间后
甲同学取一定量碳酸亚铁固体于烧杯中,加入足量水,将烧杯放置在天平左盘上,向右盘放入砝码至天平平衡.放置较长时间后 不考虑水分蒸发
不考虑水分蒸发 ,观察到天平的指针会
,观察到天平的指针会 填“偏左”、“偏右”、“不发生偏转”
填“偏左”、“偏右”、“不发生偏转” ;放置过程中还可观察到的实验现象为
;放置过程中还可观察到的实验现象为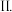 乙同学设计图1所示的装置制备
乙同学设计图1所示的装置制备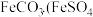 和
和 溶液均用经煮沸后冷却的蒸馏水配制,并在
溶液均用经煮沸后冷却的蒸馏水配制,并在 溶液中加入少量铁粉
溶液中加入少量铁粉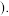 滴加
滴加 溶液后观察到试管中出现白色沉淀,同时有大量无色气体生成.
溶液后观察到试管中出现白色沉淀,同时有大量无色气体生成.
 产生的气体是
产生的气体是 填分子式
填分子式 .
. 丙同学对白色沉淀的成分提出异议,并做出如下假设,请补充完成假设3:
丙同学对白色沉淀的成分提出异议,并做出如下假设,请补充完成假设3:假设1:白色沉淀是
 ;
;假设2:白色沉淀是
 ;
;假设3:白色沉淀是
 若假设1成立,写出有关反应的化学方程式:
若假设1成立,写出有关反应的化学方程式: 若假设2成立,说明用经煮沸后冷却的蒸馏水配制
若假设2成立,说明用经煮沸后冷却的蒸馏水配制 和
和 溶液的目的是
溶液的目的是 现取
现取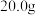 菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图2所示.
菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图2所示. 假设菱铁矿中杂质不参加反应,且难溶于水.
假设菱铁矿中杂质不参加反应,且难溶于水.
 菱铁矿中
菱铁矿中 的质量分数为
的质量分数为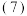 若将稀硫酸改成1mol
若将稀硫酸改成1mol  ,则该反应的离子方程式为
,则该反应的离子方程式为 将反应逸出的气体与一定量的
将反应逸出的气体与一定量的 混合循环通入反应液中,目的是
混合循环通入反应液中,目的是 某铁锈成分为
某铁锈成分为 和
和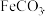 为确定其组成,兴趣小组称取此铁锈样品
为确定其组成,兴趣小组称取此铁锈样品 ,在科研人员的指导下用图3装置进行实验.
,在科研人员的指导下用图3装置进行实验.
【查阅资料】
①
 失去结晶水温度为
失去结晶水温度为 ,
, 在
在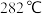 分解为FeO和
分解为FeO和 .
.②温度高于
 时铁的氧化物才能被CO还原.
时铁的氧化物才能被CO还原.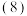 装配好实验装置后,首先要
装配好实验装置后,首先要 装置A中的反应为:
装置A中的反应为:
 草酸)
草酸) 
 通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放
通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放 选填序号
选填序号 .
. 浓硫酸
浓硫酸 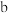 澄清的石灰水
澄清的石灰水  氢氧化钠溶液
氢氧化钠溶液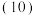 现控制D装置中的温度为
现控制D装置中的温度为 对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重
对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重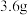 ,装置F增重
,装置F增重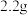 .则样品中
.则样品中 的质量
的质量

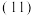 若缺少G装置,测得的
若缺少G装置,测得的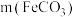
 选填“偏大”、“偏小”、“不变”,下同
选填“偏大”、“偏小”、“不变”,下同 ,x的值会
,x的值会
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】高铁酸钾 为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在
为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在 浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备
浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:

(1)装置A中发生反应的方程式_______ 。
(2)装置B中盛装的液体是_______ 。
(3)先向装置C的三口烧瓶中通入一段时间的 制备
制备 ,再滴加
,再滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_______ 。
(4)向装置C中通入的 不能过量,原因是
不能过量,原因是_______ 。
(5)若无装置D,可能产生的危害是_______ 。
(6)装置C中反应结束后,过滤,然后向滤液中加入饱和KOH溶液,低温析出 晶体。由此可知低温时溶解度:
晶体。由此可知低温时溶解度:
_______ (填“大于”、“小于”或“等于”) 。
。
(7)高铁酸钾 是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成
是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成 胶体,高铁酸钾能用于净水的原理是
胶体,高铁酸钾能用于净水的原理是_______ 。
(8)固体化合物X由3种元素组成。某学习小组进行了如下实验:

X的化学式_______ ,混合物Y的组成_______ 。
 为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在
为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在 浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备
浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
(1)装置A中发生反应的方程式
(2)装置B中盛装的液体是
(3)先向装置C的三口烧瓶中通入一段时间的
 制备
制备 ,再滴加
,再滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(4)向装置C中通入的
 不能过量,原因是
不能过量,原因是(5)若无装置D,可能产生的危害是
(6)装置C中反应结束后,过滤,然后向滤液中加入饱和KOH溶液,低温析出
 晶体。由此可知低温时溶解度:
晶体。由此可知低温时溶解度:
 。
。(7)高铁酸钾
 是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成
是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成 胶体,高铁酸钾能用于净水的原理是
胶体,高铁酸钾能用于净水的原理是(8)固体化合物X由3种元素组成。某学习小组进行了如下实验:

X的化学式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】某化学兴趣小组欲测量碳铁合金的含碳量,提出了如下三种实验方案。
方案Ⅰ:含碳铁合金粉末与浓硫酸在一定条件下反应,用下列装置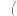 加持装置省略
加持装置省略 既可检验产物中除
既可检验产物中除 外混合气体的成分,又可通过测量
外混合气体的成分,又可通过测量 的质量来计算合金的含碳量。
的质量来计算合金的含碳量。
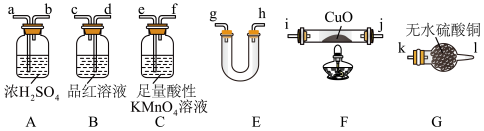
(1)合金与浓硫酸在一定条件下生成 的反应中,做还原剂的物质时
的反应中,做还原剂的物质时____ (填化学式)。
(2)为实现实验目的,上述仪器正确的连接顺序 按气流方向
按气流方向 为:混合气体→
为:混合气体→____ →____ →______ →(a)(b)→_____ →_______ →(k)(l)。
(3)装置E中所装药品为______  填字母序号
填字母序号 ;在本实验中的作用是
;在本实验中的作用是 ______ 。
A 碱石灰 B 无水氯化钙 C 浓硫酸
(4)若能观察到______ 的现象,则证明原混合气体中一定含有 。
。
(5)实验后最终测量的含碳量偏低,某同学猜测混合气体中有可能含有CO,在G后增加一个装置即可验证他的猜测,请简要说明验证这个猜测所需装置及药品和具体实验现象______ 。
方案Ⅱ:称取粉末状样品 ,加入某浓度的稀硫酸100mL,充分反应后,收集到标准状况下气体
,加入某浓度的稀硫酸100mL,充分反应后,收集到标准状况下气体 ,然后继续往样品中加入同浓度的稀硫酸100mL,充分反应后又收集到标准状况下气体1.12L。则合金中碳的质量分数为
,然后继续往样品中加入同浓度的稀硫酸100mL,充分反应后又收集到标准状况下气体1.12L。则合金中碳的质量分数为 ______ (保留三位有效数字)。
方案Ⅲ:利用灼烧法使合金中的碳转化为二氧化碳,合金质量会减轻从而计算含碳量,但是他们将一定量的样品灼烧后,发现质量反而增加了,其原因是______ 。
方案Ⅰ:含碳铁合金粉末与浓硫酸在一定条件下反应,用下列装置
 加持装置省略
加持装置省略 既可检验产物中除
既可检验产物中除 外混合气体的成分,又可通过测量
外混合气体的成分,又可通过测量 的质量来计算合金的含碳量。
的质量来计算合金的含碳量。
(1)合金与浓硫酸在一定条件下生成
 的反应中,做还原剂的物质时
的反应中,做还原剂的物质时(2)为实现实验目的,上述仪器正确的连接顺序
 按气流方向
按气流方向 为:混合气体→
为:混合气体→(3)装置E中所装药品为
 填字母序号
填字母序号 ;在本实验中的作用是
;在本实验中的作用是 A 碱石灰 B 无水氯化钙 C 浓硫酸
(4)若能观察到
 。
。(5)实验后最终测量的含碳量偏低,某同学猜测混合气体中有可能含有CO,在G后增加一个装置即可验证他的猜测,请简要说明验证这个猜测所需装置及药品和具体实验现象
方案Ⅱ:称取粉末状样品
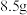 ,加入某浓度的稀硫酸100mL,充分反应后,收集到标准状况下气体
,加入某浓度的稀硫酸100mL,充分反应后,收集到标准状况下气体 ,然后继续往样品中加入同浓度的稀硫酸100mL,充分反应后又收集到标准状况下气体1.12L。则合金中碳的质量分数为
,然后继续往样品中加入同浓度的稀硫酸100mL,充分反应后又收集到标准状况下气体1.12L。则合金中碳的质量分数为 方案Ⅲ:利用灼烧法使合金中的碳转化为二氧化碳,合金质量会减轻从而计算含碳量,但是他们将一定量的样品灼烧后,发现质量反而增加了,其原因是
您最近一年使用:0次



