按要求填空
(1)浓硫酸具有如下的性质:A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________
②碳投入热的浓硫酸中溶解___________
③浓硫酸与氧化铜反应___________
④浓硫酸干燥氢气___________
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________
②常温下可用铝或者铁遇浓硝酸钝化___________
(3)二氧化硫气体在下列反应中表现的性质填写在横线上。
A.氧化性B.漂白性C.还原性D.酸性氧化物的性质
①SO2+2OH-= +H2O
+H2O___________
②SO2+2H2S=3S↓+2H2O___________
③SO2+Ca(OH)2=CaSO3↓+H2O___________
④SO2+Cl2+2H2O=2HCl+H2SO4___________
(1)浓硫酸具有如下的性质:A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑
②碳投入热的浓硫酸中溶解
③浓硫酸与氧化铜反应
④浓硫酸干燥氢气
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存
②常温下可用铝或者铁遇浓硝酸钝化
(3)二氧化硫气体在下列反应中表现的性质填写在横线上。
A.氧化性B.漂白性C.还原性D.酸性氧化物的性质
①SO2+2OH-=
 +H2O
+H2O②SO2+2H2S=3S↓+2H2O
③SO2+Ca(OH)2=CaSO3↓+H2O
④SO2+Cl2+2H2O=2HCl+H2SO4
更新时间:2021-04-27 11:06:27
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:

回答下列问题:
(1)下列说法不正确的是_______
(2)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,用化学方程式解释其原因_______
(3)利用反应6NO2 + 8NH3 ═ 7N2 + 12H2O构成电池,能实现有效消除氮氧化物的排放,减轻环境污染,装置如图所示。

电极B为_______ (正极/负极),电极A的电极反应式为_______

回答下列问题:
(1)下列说法不正确的是_______
| A.SO2、NO2均能形成酸雨 |
| B.雾和霾的分散剂不相同 |
| C.雾霾的形成与过度使用氮肥有关 |
| D.工厂中燃料脱硫、开发新能源有利于减少雾霾 |
(3)利用反应6NO2 + 8NH3 ═ 7N2 + 12H2O构成电池,能实现有效消除氮氧化物的排放,减轻环境污染,装置如图所示。

电极B为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氮是地球上含量丰富的元素。氮及其化合物在一定条件下的转化关系如图:
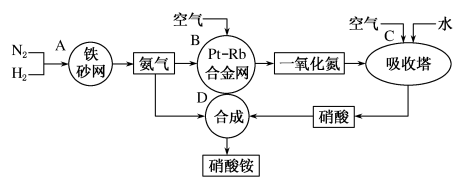
(1)容器B中的合金网采用网状结构的目的是_______ ,该处发生反应的化学方程式为_______ 。
(2)同温同压下,理论上容器B和容器C消耗的空气体积之比为_______ 。
(3)实验室中浓硝酸一般保存在棕色试剂瓶中,并放置于阴凉处,请解释原因:_______ 。
(4)常温下,Zn与稀硝酸反应生成硝酸铵的离子方程式为_______ ,该反应中稀硝酸表现出的性质是_______ 。
(5)工业制硝酸时尾气中含有的 (NO、
(NO、 )常用碱液吸收。
)常用碱液吸收。
①写出 与NaOH溶液反应生成两种氮的含氧酸盐的化学方程式:
与NaOH溶液反应生成两种氮的含氧酸盐的化学方程式:_______ 。
②将硝酸尾气中的NO,通入过量的NaOH溶液中充分反应后无气体剩余,则 中的x的取值范围是
中的x的取值范围是_______ (用含x的式子表示,已知: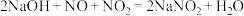 )。
)。

(1)容器B中的合金网采用网状结构的目的是
(2)同温同压下,理论上容器B和容器C消耗的空气体积之比为
(3)实验室中浓硝酸一般保存在棕色试剂瓶中,并放置于阴凉处,请解释原因:
(4)常温下,Zn与稀硝酸反应生成硝酸铵的离子方程式为
(5)工业制硝酸时尾气中含有的
 (NO、
(NO、 )常用碱液吸收。
)常用碱液吸收。①写出
 与NaOH溶液反应生成两种氮的含氧酸盐的化学方程式:
与NaOH溶液反应生成两种氮的含氧酸盐的化学方程式:②将硝酸尾气中的NO,通入过量的NaOH溶液中充分反应后无气体剩余,则
 中的x的取值范围是
中的x的取值范围是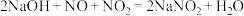 )。
)。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】硫、氮元素是高中化学学习的两种重要非金属元素,其价类二维图分别如图所示:
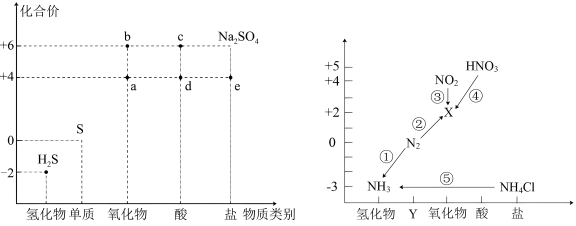
(1)c物质的浓溶液与金属铜发生反应的化学方程式为:_____ 。
(2)a与H2S发生反应的化学方程式:_____ 。
(3)实验室用⑤途径制备NH3的化学方程式为:_____ 。
(4)氨气是工业制硝酸的重要原料,写出①反应的化学方程式_____ 。
(5)关于氮及其化合物的说法错误的是_____ 。

(1)c物质的浓溶液与金属铜发生反应的化学方程式为:
(2)a与H2S发生反应的化学方程式:
(3)实验室用⑤途径制备NH3的化学方程式为:
(4)氨气是工业制硝酸的重要原料,写出①反应的化学方程式
(5)关于氮及其化合物的说法错误的是
| A.氮气分子结构稳定,常做保护气,不支持任何物质燃烧 |
| B.NO、NO2均为大气污染气体,在大气中均可稳定存在 |
| C.可用浓盐酸检测输送NH3的管道是否发生泄漏 |
| D.HNO3具有强氧化性,可溶解铜、银等不活泼金属 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】混合物的分离与提纯在化学实验中占有重要的位置。如图表示从固体混合物中分离X的方案,请回答有关问题。
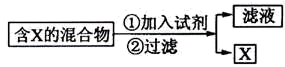
若按照如图图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是___ ,有关反应的化学方程式为____ ;过滤所用到的玻璃仪器有:___ 。

若按照如图图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下:

请回答下列问题:
(1)在炉气制造中,黄铁矿粉碎的目的是____________ ,生成二氧化硫的化学方程式是_____________ 。
(2)炉气精制的目的是__________________________________ 。
(3)二氧化硫催化氧化的化学方程式是________________________ 。
(4)浓硫酸是不是可以用水代替:__________ ,原因是__________________________________ 。
(5)尾气的主要成分是__________ ,若将尾气通入氢氧化钙浊液中,最后能得到的副产品是________ 。

请回答下列问题:
(1)在炉气制造中,黄铁矿粉碎的目的是
(2)炉气精制的目的是
(3)二氧化硫催化氧化的化学方程式是
(4)浓硫酸是不是可以用水代替:
(5)尾气的主要成分是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求回答下列问题:
(1)写出铁红的化学式___________ ;
(2)CO2分子的空间结构是___________ (用文字描述);
(3)写出灼热的木炭与浓硫酸反应的化学方程式___________ ;
(4)反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,该反应的氧化剂是
MnCl2+Cl2↑+2H2O,该反应的氧化剂是___________ ;
(5)写出硫酸钠的电离方程式___________ ;
(6)铝条表面的氧化膜与NaOH溶液反应的离子方程式是___________ ;
(7)把2.0mol/LCuSO4溶液和1.0mol/LFe2(SO4)3溶液等体积混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量铁粉经过足够长的时间后,铁粉有剩余。此时溶液中Fe2+的物质的量浓度为___________ 。
(1)写出铁红的化学式
(2)CO2分子的空间结构是
(3)写出灼热的木炭与浓硫酸反应的化学方程式
(4)反应MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,该反应的氧化剂是
MnCl2+Cl2↑+2H2O,该反应的氧化剂是(5)写出硫酸钠的电离方程式
(6)铝条表面的氧化膜与NaOH溶液反应的离子方程式是
(7)把2.0mol/LCuSO4溶液和1.0mol/LFe2(SO4)3溶液等体积混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量铁粉经过足够长的时间后,铁粉有剩余。此时溶液中Fe2+的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】二氧化硫的化学性质
(1)SO2具有酸性氧化物的通性
①写出下列反应的化学方程式:
a.和水反应:____ 。
b.和澄清石灰水反应:___ 。
c.和CaO反应:____ 。
②可逆反应:在____ 条件下,既能向____ 方向进行,____ 又能向____ 方向进行的反应。在可逆反应的化学方程式中用“ ”代替“=”。
”代替“=”。
(2)从元素化合价变化角度分析SO2性质
①强还原性
与氯水反应:____ 。
与O2反应:____ 。
②弱氧化性
与H2S反应:____ 。
(3)SO2的特性——漂白性
它能与某些有色物质(如品红溶液)生成不稳定的无色物质。这些无色物质容易分解而使有色物质恢复原来的颜色。
(1)SO2具有酸性氧化物的通性
①写出下列反应的化学方程式:
a.和水反应:
b.和澄清石灰水反应:
c.和CaO反应:
②可逆反应:在
 ”代替“=”。
”代替“=”。(2)从元素化合价变化角度分析SO2性质
①强还原性
与氯水反应:
与O2反应:
②弱氧化性
与H2S反应:
(3)SO2的特性——漂白性
它能与某些有色物质(如品红溶液)生成不稳定的无色物质。这些无色物质容易分解而使有色物质恢复原来的颜色。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O)
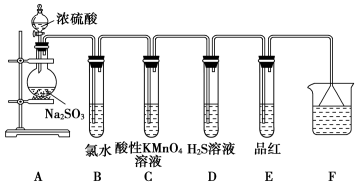
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是_______ 。
(2)反应后,装置B中发生反应的离子方程式为_______ ,装置C中的现象是_______ ,表现了SO2的_______ ;装置D中现象是_______ ,发生反应的化学方程式为_______ 。
(3)F装置的作用是_______ ,漏斗的作用是_______ 。

请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是
(2)反应后,装置B中发生反应的离子方程式为
(3)F装置的作用是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】如图所示的装置是带有可上下移动的活塞的密闭容器,其中盛有饱和 H2S 溶液,并与 H2S 气体建立溶解平衡。
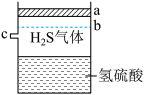
(1)饱和 H2S 溶液中存在_______ 种微粒。
(2)关闭 c 口,若容器中活塞由 a 压到 b 位置,则H2S 溶液中,_______ 离子浓度增大,而_______ 离子浓度减小。
(3)在压强不变时,由 c 处通入一定量N2,则溶液中 H+浓度将_______ 。(填变大,变小,不变)
(4)若从 c 处通入 SO2气体充分反应,并达到饱和,溶液中 H+浓度将_______。
(5)将等浓度等体积的氢硫酸和氢氧化钠溶液混合,写出反应的离子方程式_______ 所得溶液中阴离子浓度由大到小的次序为_______

(1)饱和 H2S 溶液中存在
(2)关闭 c 口,若容器中活塞由 a 压到 b 位置,则H2S 溶液中,
(3)在压强不变时,由 c 处通入一定量N2,则溶液中 H+浓度将
(4)若从 c 处通入 SO2气体充分反应,并达到饱和,溶液中 H+浓度将_______。
| A.不断增大 | B.先减小,后增大到某值 |
| C.不变 | D.先增大,后减小到某值 |
您最近一年使用:0次

 CO2↑+ 2SO2↑+2H2O,在该反应中,浓硫酸表现出
CO2↑+ 2SO2↑+2H2O,在该反应中,浓硫酸表现出

