如图所示的装置是带有可上下移动的活塞的密闭容器,其中盛有饱和 H2S 溶液,并与 H2S 气体建立溶解平衡。
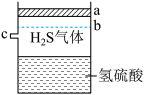
(1)饱和 H2S 溶液中存在_______ 种微粒。
(2)关闭 c 口,若容器中活塞由 a 压到 b 位置,则H2S 溶液中,_______ 离子浓度增大,而_______ 离子浓度减小。
(3)在压强不变时,由 c 处通入一定量N2,则溶液中 H+浓度将_______ 。(填变大,变小,不变)
(4)若从 c 处通入 SO2气体充分反应,并达到饱和,溶液中 H+浓度将_______。
(5)将等浓度等体积的氢硫酸和氢氧化钠溶液混合,写出反应的离子方程式_______ 所得溶液中阴离子浓度由大到小的次序为_______

(1)饱和 H2S 溶液中存在
(2)关闭 c 口,若容器中活塞由 a 压到 b 位置,则H2S 溶液中,
(3)在压强不变时,由 c 处通入一定量N2,则溶液中 H+浓度将
(4)若从 c 处通入 SO2气体充分反应,并达到饱和,溶液中 H+浓度将_______。
| A.不断增大 | B.先减小,后增大到某值 |
| C.不变 | D.先增大,后减小到某值 |
更新时间:2023-03-10 13:14:56
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】如图是硫元素价态与含硫元素物质类别的二维坐标图。

请回答下列问题
(1)硫元素在周期表中的位置为____ 。
(2)氧元素比硫元素的非金属性___ (填“强”或“弱”),不能说明该非金属性强弱的事实是___ 。
A.热稳定性H2O比H2S强
B.H2S水溶液在空气中变浑浊
C.H2O比H2S的沸点高
D.在一定条件下,O2与Cu反应生成CuO,S与Cu反应生成Cu2S
(3)写出b与j混合,发生反应的化学方程式为_______ 。
(4)已知硒(Se)与硫是相邻周期同主族元素,画出硒原子结构示意图_______ 。

请回答下列问题
(1)硫元素在周期表中的位置为
(2)氧元素比硫元素的非金属性
A.热稳定性H2O比H2S强
B.H2S水溶液在空气中变浑浊
C.H2O比H2S的沸点高
D.在一定条件下,O2与Cu反应生成CuO,S与Cu反应生成Cu2S
(3)写出b与j混合,发生反应的化学方程式为
(4)已知硒(Se)与硫是相邻周期同主族元素,画出硒原子结构示意图
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。___________ 。
(2)X与Y反应的化学方程式___________ ,其中还原剂与氧化剂的物质的量之比为___________ 。
(3) 和氯水都有漂白性,有人为增强漂白效果,将
和氯水都有漂白性,有人为增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,其原因是
混合使用,结果适得其反,几乎没有漂白效果,其原因是___________ (用化学方程式表示)。
(4)下列四种有色溶液与 作用均能褪色:
作用均能褪色:
①酸性 溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液
溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液
体现 漂白性的是
漂白性的是___________ (用序号填空)。体现 还原性的是
还原性的是___________ (用序号填空)。写出 通入酸性
通入酸性 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(5)硝酸是用途广泛的化工原料。铜与浓稀硝酸均能反应,写出铜和稀硝酸反应的离子方程式是___________ 。若64.0gCu与一定量的 溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和
溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和 ),则消耗的
),则消耗的 溶液中溶质的物质的量为
溶液中溶质的物质的量为___________ 。
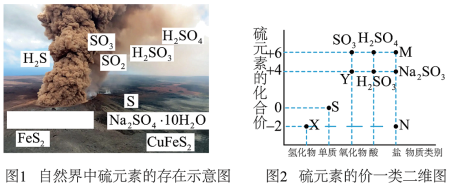
(2)X与Y反应的化学方程式
(3)
 和氯水都有漂白性,有人为增强漂白效果,将
和氯水都有漂白性,有人为增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,其原因是
混合使用,结果适得其反,几乎没有漂白效果,其原因是(4)下列四种有色溶液与
 作用均能褪色:
作用均能褪色:①酸性
 溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液
溶液 ②品红溶液 ③淀粉—碘溶液 ④滴有酚酞的NaOH溶液体现
 漂白性的是
漂白性的是 还原性的是
还原性的是 通入酸性
通入酸性 溶液反应的离子方程式
溶液反应的离子方程式(5)硝酸是用途广泛的化工原料。铜与浓稀硝酸均能反应,写出铜和稀硝酸反应的离子方程式是
 溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和
溶液反应,当Cu反应完时,共产生标准状况下的4.48L气体(NO和 ),则消耗的
),则消耗的 溶液中溶质的物质的量为
溶液中溶质的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】 是危害环境的气体,生产中可用多种方法减少烟气中
是危害环境的气体,生产中可用多种方法减少烟气中 排放,并实现资源再利用。
排放,并实现资源再利用。
(1)软锰矿(主要成分 )可用于脱除烟气中的
)可用于脱除烟气中的 ,其主要化学反应原理是:
,其主要化学反应原理是:
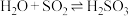

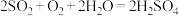
①脱除时需将软锰矿进行粉碎,配成软锰矿浆,其目的是_______ 。上述反应中,MnO2是_______ (填“氧化剂”、“还原剂”或“催化剂”)。
②吸收大量的 后,软锰矿浆的pH将
后,软锰矿浆的pH将_______ 。
A.增大 B.减小 C.不变 D.无法确定
③软锰矿浆吸收 时,温度常控制在室温。若温度过高,烟气脱硫效率将下降,其可能的原因是
时,温度常控制在室温。若温度过高,烟气脱硫效率将下降,其可能的原因是_______ 。
④实验室常用软锰矿制取氯气,写出发生的化学方程式:_______ 。
(2)工业上利用 尾气、硫黄、液氯为原料,在活性炭为催化剂、200~250℃条件下制备氯化亚砜(SOCl2),反应的化学方程式为
尾气、硫黄、液氯为原料,在活性炭为催化剂、200~250℃条件下制备氯化亚砜(SOCl2),反应的化学方程式为_______ 。
 是危害环境的气体,生产中可用多种方法减少烟气中
是危害环境的气体,生产中可用多种方法减少烟气中 排放,并实现资源再利用。
排放,并实现资源再利用。(1)软锰矿(主要成分
 )可用于脱除烟气中的
)可用于脱除烟气中的 ,其主要化学反应原理是:
,其主要化学反应原理是: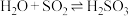

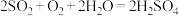
①脱除时需将软锰矿进行粉碎,配成软锰矿浆,其目的是
②吸收大量的
 后,软锰矿浆的pH将
后,软锰矿浆的pH将A.增大 B.减小 C.不变 D.无法确定
③软锰矿浆吸收
 时,温度常控制在室温。若温度过高,烟气脱硫效率将下降,其可能的原因是
时,温度常控制在室温。若温度过高,烟气脱硫效率将下降,其可能的原因是④实验室常用软锰矿制取氯气,写出发生的化学方程式:
(2)工业上利用
 尾气、硫黄、液氯为原料,在活性炭为催化剂、200~250℃条件下制备氯化亚砜(SOCl2),反应的化学方程式为
尾气、硫黄、液氯为原料,在活性炭为催化剂、200~250℃条件下制备氯化亚砜(SOCl2),反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】常温下,某水溶液M中存在的离子有:Na+ 、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式_______ 。
(2)实验测得NaHA溶液的pH>7,请分析NaHA溶液显碱性的原因_______ 。
(1)写出酸H2A的电离方程式
(2)实验测得NaHA溶液的pH>7,请分析NaHA溶液显碱性的原因
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】同体积、pH=2的盐酸(A)和pH=2醋酸溶液(B)各1L 。分别加入等质量的锌片,充分反应后:(填>、<、=)
(1)若Zn均剩余,开始时生成氢气的速率:υ(H2):A____ B, 一会儿后υ(H2)A___ B。最终生成H2总量A ____ B; 所得溶液的质量增重A ____ B。
(2)若Zn均耗尽,最终生成H2总量A____ B,所用时间A____ B;剩余溶液PH:A _____ B。
(3)若有一溶液中剩Zn,此溶液是_____ (填A或B) ,最终生成H2总量A_____ B。
(4)若二溶液不加锌,而改为加水稀至pH=4,所加水量A____ B;加水后对水电离的抑制程度A ___ B;水的电离转化率A____ B。
(1)若Zn均剩余,开始时生成氢气的速率:υ(H2):A
(2)若Zn均耗尽,最终生成H2总量A
(3)若有一溶液中剩Zn,此溶液是
(4)若二溶液不加锌,而改为加水稀至pH=4,所加水量A
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某酸HA是一元弱酸,25℃时的电离平衡常数Ka=4.0×10-8。
(1)写出该酸的电离方程式____ ,其电离平衡常数表达式Ka=____ 。
(2)25℃时,向1mol•L-1HA溶液中加入1mol•L-1盐酸,会____ (“抑制”或“促进”)HA的电离,c(H+)____ (填“增大”、“减小”或“不变”),电离平衡常数Ka____ (填“增大”、“减小”或“不变”)。
(3)常温条件下,某浓度的盐酸溶液的pH=3,则其中c(H+)=____ mol/L,c(OH-)=____ mol/L。
(4)常温下等体积混合0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液后,溶液pH=____ 。
(1)写出该酸的电离方程式
(2)25℃时,向1mol•L-1HA溶液中加入1mol•L-1盐酸,会
(3)常温条件下,某浓度的盐酸溶液的pH=3,则其中c(H+)=
(4)常温下等体积混合0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液后,溶液pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】25℃时,三种酸的电离平衡常数如表所示。
回答下列问题:
(1)浓度均为0.1mol/L的CH3COOH,HClO,H3PO3溶液中,c(H+)最小的是___ 。
(2)亚磷酸(H3PO3)为二元酸,具有较强的还原性Na2HPO3是___ (填“酸式盐”“碱式盐”或“正盐”)。H3PO3的第二级电离方程式为___ 。此时的电离平衡常数表达式K=___ 。
(3)常温下,0.1mol/L的CH3COOH溶液加水稀释的过程中,下列表达式的数值变大的是___ (填字母)。
A.c(H+) B. C.c(CH3COO-) D.c(CH3COOH)
C.c(CH3COO-) D.c(CH3COOH)
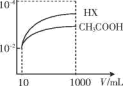
(4)体积均为10mL、c(H+)均为10-2mol/L的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中c(H+)的变化如图所示测HX的电离平衡常数___ (填“大于”、“小于”或“等于”)醋酸的电离平衡常数,理由是___ 。
| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数 | 1.8×10-5 | 3.0×10-8 | Ki=8.3×10-3 K2=5.6×10-6 |
回答下列问题:
(1)浓度均为0.1mol/L的CH3COOH,HClO,H3PO3溶液中,c(H+)最小的是
(2)亚磷酸(H3PO3)为二元酸,具有较强的还原性Na2HPO3是
(3)常温下,0.1mol/L的CH3COOH溶液加水稀释的过程中,下列表达式的数值变大的是
A.c(H+) B.
 C.c(CH3COO-) D.c(CH3COOH)
C.c(CH3COO-) D.c(CH3COOH)(4)体积均为10mL、c(H+)均为10-2mol/L的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中c(H+)的变化如图所示测HX的电离平衡常数

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】物质A~E都是由下表中的离子组成的,常温下将各物质的溶液从1mL稀释到1000mL,pH的变化关系如图甲所示,其中A与D反应得到E。请回答下列问题。

(1)根据pH的变化关系,写出物质的化学式:B___________ ,C___________ 。
(2)写出D的电离方程式:___________
(3)写出A与C反应的离子方程式:___________ 。
| 阳离子 |  、H+、Na+ 、H+、Na+ |
| 阴离子 | OH-、CH3COO-、Cl- |

(1)根据pH的变化关系,写出物质的化学式:B
(2)写出D的电离方程式:
(3)写出A与C反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
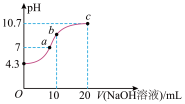
①写出H2N2O2在水溶液中的电离方程式:__ 。
②c点时溶液中各离子浓度由大到小的顺序为__ 。
③b点时溶液中c(H2N2O2)__ c(N2O22-)。(填“>”“<”或“=”,下同)
④a点时溶液中c(Na+)__ c(HN2O)+c(N2O22-)。
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中 =
=__ 。[已知Ksp(Ag2N2O2)=4.2×10-9,Ksp(Ag2SO4)=1.4×10-5]
(3)有时我们将NaHCO3溶液中的平衡表示为:2HCO3- H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理
H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理___ (填序号)
A.适当浓度的盐酸
B.适当浓度Ba(OH)2溶液
C.适当浓度BaCl2溶液
(1)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:
②c点时溶液中各离子浓度由大到小的顺序为
③b点时溶液中c(H2N2O2)
④a点时溶液中c(Na+)
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中
 =
=(3)有时我们将NaHCO3溶液中的平衡表示为:2HCO3-
 H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理
H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理A.适当浓度的盐酸
B.适当浓度Ba(OH)2溶液
C.适当浓度BaCl2溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是_________________________
向其中加入少量KOH溶液时,发生反应的离子方程是___________________________
(2)现将0.04 mol·L-1HA溶液和0.02 mol·L-1NaOH 溶液等体积混合,得到缓冲溶液。
①若HA为HCN,该溶液显碱性,则溶液中c(Na+)_______ c(CN−)(填“<”“=”“>”)
②若HA为CH3COOH ,该溶液显酸性。溶液中所有的离子按浓度由大到小排列的顺序是_____________________________________________ 。
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是
向其中加入少量KOH溶液时,发生反应的离子方程是
(2)现将0.04 mol·L-1HA溶液和0.02 mol·L-1NaOH 溶液等体积混合,得到缓冲溶液。
①若HA为HCN,该溶液显碱性,则溶液中c(Na+)
②若HA为CH3COOH ,该溶液显酸性。溶液中所有的离子按浓度由大到小排列的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问题。
(1)生活中明矾常作净水剂,其净水的原理是_____ (用离子方程式表示)。
(2)常温下,取0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合,测得混合后溶液的pH=5,则pH=13的MOH溶液的浓度____ 0.1mol/L(填<、>或=)。
(3)氢叠氮酸(HN3)是常用原料。氢叠氮酸易溶于水,25℃时,该酸的电离常数为Ka=1.0×10-5。
①氢叠氮酸在水溶液中的电离方程式为____ 。
②0.2mol/L的HN3溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,溶液呈酸性,则混合溶液中各离子浓度由大到小的顺序为____ 。
(4)含Cr2O 的废水毒性较大,某工厂废水中含5.0×10−3mol/L的Cr2O
的废水毒性较大,某工厂废水中含5.0×10−3mol/L的Cr2O 。为了使废水的排放达标,进行如图处理:
。为了使废水的排放达标,进行如图处理:

绿矾为FeSO4•7H2O。反应(I)中Cr2O 与FeSO4的物质的量之比为
与FeSO4的物质的量之比为____ 。常温下若处理后的废水中c(Cr3+)=6.0×10−7mol/L,则处理后的废水的pH=____ 。(Ksp[Cr(OH)3]=6.0×10-31)
(1)生活中明矾常作净水剂,其净水的原理是
(2)常温下,取0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合,测得混合后溶液的pH=5,则pH=13的MOH溶液的浓度
(3)氢叠氮酸(HN3)是常用原料。氢叠氮酸易溶于水,25℃时,该酸的电离常数为Ka=1.0×10-5。
①氢叠氮酸在水溶液中的电离方程式为
②0.2mol/L的HN3溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,溶液呈酸性,则混合溶液中各离子浓度由大到小的顺序为
(4)含Cr2O
 的废水毒性较大,某工厂废水中含5.0×10−3mol/L的Cr2O
的废水毒性较大,某工厂废水中含5.0×10−3mol/L的Cr2O 。为了使废水的排放达标,进行如图处理:
。为了使废水的排放达标,进行如图处理:
绿矾为FeSO4•7H2O。反应(I)中Cr2O
 与FeSO4的物质的量之比为
与FeSO4的物质的量之比为
您最近一年使用:0次

 的原因
的原因

