已知化合物X由3种元素组成,某学习小组进行了如下实验:
①取适量X,加水完全溶解有无色气体和蓝色沉淀产生;取反应后溶液进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色:
②取2.95gX溶于水,加入含H2SO40.025mol的硫酸恰好反应,生成标准状况下0.056L无色气体;反应后的溶液可与0.015molSiO2反应,得到无色刺激性气体,该气体易潮解,在潮湿空气中可产生浓烟雾。
请回答:
(1)X中3种元素是___________ (用元素符号表示)。
(2)X与硫酸反应的化学方程式是___________ 。
(3)向①反应后溶液滴加少量酸或少量碱溶液时,溶液pH值并不会发生明显变化,试用离子方程式解释:___________ 。
①取适量X,加水完全溶解有无色气体和蓝色沉淀产生;取反应后溶液进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色:
②取2.95gX溶于水,加入含H2SO40.025mol的硫酸恰好反应,生成标准状况下0.056L无色气体;反应后的溶液可与0.015molSiO2反应,得到无色刺激性气体,该气体易潮解,在潮湿空气中可产生浓烟雾。
请回答:
(1)X中3种元素是
(2)X与硫酸反应的化学方程式是
(3)向①反应后溶液滴加少量酸或少量碱溶液时,溶液pH值并不会发生明显变化,试用离子方程式解释:
20-21高二下·浙江·阶段练习 查看更多[1]
(已下线)【浙江新东方】高中化学20210429—002【2021】【高二下】
更新时间:2021-05-07 18:53:17
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】近年来,“氮排放”逐渐引起人们的重视。氮及其化合物与生产生活及环境息息相关,请回答下列问题:
(1)下列环境问题与氮的氧化物排放无关的是___________。
(2)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式___________ 。
(3)硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
①工业生产中为了盛装大量浓硝酸,可选择___________ 作为罐体材料。
A.Mg B.Al C.Fe D.Cu
②为避免硝酸生产尾气中的NO2污染环境,可以使用具有碱性的碳酸钠溶液吸收,发生反应的离子方程式为___________ 。
③硝酸与金属反应会产生氮氧化物。在含有agHNO3的稀硝酸中,加入bg铁粉充分反应, 铁全部溶解并生成NO,有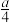 gHNO3被还原,则a:b可能为
gHNO3被还原,则a:b可能为___________ 。
A.2:1 B.3:1 C.4:1 D.8:3
(4)氮化硅(Si3N4)陶瓷材料可用于高温工程的部件、冶金工业等方面的高级耐火材料,可由石英与焦炭在高温的氮气流中制备,反应的化学方程式为___________ 。
(5)氮的同族元素锑(Sb)可形成比纯硫酸更强的酸——氟锑酸(HSbF6),称为超酸。为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为:CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为___________ 。
(1)下列环境问题与氮的氧化物排放无关的是___________。
| A.酸雨 | B.光化学烟雾 | C.臭氧层空洞 | D.白色污染 |
(3)硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
①工业生产中为了盛装大量浓硝酸,可选择
A.Mg B.Al C.Fe D.Cu
②为避免硝酸生产尾气中的NO2污染环境,可以使用具有碱性的碳酸钠溶液吸收,发生反应的离子方程式为
③硝酸与金属反应会产生氮氧化物。在含有agHNO3的稀硝酸中,加入bg铁粉充分反应, 铁全部溶解并生成NO,有
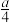 gHNO3被还原,则a:b可能为
gHNO3被还原,则a:b可能为A.2:1 B.3:1 C.4:1 D.8:3
(4)氮化硅(Si3N4)陶瓷材料可用于高温工程的部件、冶金工业等方面的高级耐火材料,可由石英与焦炭在高温的氮气流中制备,反应的化学方程式为
(5)氮的同族元素锑(Sb)可形成比纯硫酸更强的酸——氟锑酸(HSbF6),称为超酸。为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为:CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为探究不含结晶水的白色正盐X(仅含三种元素)的组成和性质,设计并完成如下实验:
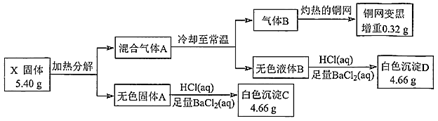
已知:M(X)=270g·mol-1,灼烧X并透过蓝色钴玻璃片可看到紫色火焰。请回答:
(1)无色液体B的化学式是____ 。
(2)固体X加热分解的化学方程式是____ 。
(3)将X加入MnSO4溶液中,溶液变成紫红色,该反应的离子方程式为____ 。

已知:M(X)=270g·mol-1,灼烧X并透过蓝色钴玻璃片可看到紫色火焰。请回答:
(1)无色液体B的化学式是
(2)固体X加热分解的化学方程式是
(3)将X加入MnSO4溶液中,溶液变成紫红色,该反应的离子方程式为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】现有一种碱金属的碳酸盐(M2CO3)和碳酸氢钠组成的混合物,取其1.896g加热至质量不再变化,把放出的气体通入足量的澄清石灰水中,得到白色沉淀0.800g。将加热后残留的固体与足量稀硫酸充分反应,生成的气体经充分干燥后通过足量的过氧化钠粉末,结果过氧化钠粉末增重0.336 g。
(1)试通过计算确定M2CO3的M为___________ 元素。
(2)有同学提出,通过简单的定性实验,也可以确定该样品中的M为何种碱金属元素。你认为该实验方案是_________________
(1)试通过计算确定M2CO3的M为
(2)有同学提出,通过简单的定性实验,也可以确定该样品中的M为何种碱金属元素。你认为该实验方案是
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】A.将一定质量的Mg和Al混合物投入400 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
计算:
(1)Mg和Al的总质量为________ g;
(2)硫酸的物质的量浓度为________ ;
(3)生成H2的物质的量为________ 。

B.将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL ,4mol/L的稀硫酸中,生成标准状况下6.72L气体。向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:
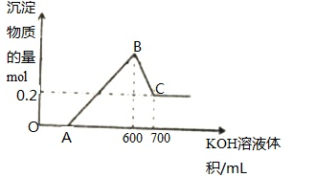
(1)OA对应反应的离子方程式为_________ ,BC对应反应的离子方程式为____________ ;
(2)c(KOH)=_________ mol/L,混合物中氧化铝的物质的量为_____ mol;
(3)A点对应的数值为_______ ;
(4)在中学阶段,实验室里检验B点对应的溶液中的阳离子时,所观察到的现象是___________ 。
(5)向C点对应的溶液中通入足量的CO2所发生反应的离子方程式为_____________ 。
计算:
(1)Mg和Al的总质量为
(2)硫酸的物质的量浓度为
(3)生成H2的物质的量为

B.将一定量的铝粉、氧化铝、氧化镁的混合物加入到300mL ,4mol/L的稀硫酸中,生成标准状况下6.72L气体。向反应后的溶液中滴加一定物质的量浓度的KOH溶液时,所得沉淀的物质的量(mol)与滴加KOH溶液的体积(mL)之间的关系如图所示:

(1)OA对应反应的离子方程式为
(2)c(KOH)=
(3)A点对应的数值为
(4)在中学阶段,实验室里检验B点对应的溶液中的阳离子时,所观察到的现象是
(5)向C点对应的溶液中通入足量的CO2所发生反应的离子方程式为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】聚合硫酸铝铁[AlaFeb(OH)n(SO4)m·xH2O]是一种新型高效净水剂,广泛应用于工业污染水的处理。
(1)聚合硫酸铝铁能够净水的原因是________________________
(2)AlaFeb(OH)m(SO4)n•xH2O中a、b、m、n的代数关系式为_______________________ 。
(3)为了测定聚合硫酸铝铁的组成,进行如下实验:
步骤一:准确称取8.810g样品溶于150mL 0.100mol•L-1稀硫酸,恰好完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体10.485g;
步骤二:另取相同质量的样品,溶于过量的氢碘酸,以磁力搅拌机搅拌,充分反应后,以0.500mol•L-1Na2S2O3溶液滴定至浅黄色,滴入几滴淀粉溶液,再滴定至终点,消耗Na2S2O3溶液20.00mL.(已知:I2+2Na2S2O3=2NaI+Na2S4O6)
①步骤二中使用磁力搅拌器进行搅拌的目的是________________________ 。
②通过计算确定聚合硫酸铝铁的化学式(写出计算过程)。________________________
(1)聚合硫酸铝铁能够净水的原因是
(2)AlaFeb(OH)m(SO4)n•xH2O中a、b、m、n的代数关系式为
(3)为了测定聚合硫酸铝铁的组成,进行如下实验:
步骤一:准确称取8.810g样品溶于150mL 0.100mol•L-1稀硫酸,恰好完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体10.485g;
步骤二:另取相同质量的样品,溶于过量的氢碘酸,以磁力搅拌机搅拌,充分反应后,以0.500mol•L-1Na2S2O3溶液滴定至浅黄色,滴入几滴淀粉溶液,再滴定至终点,消耗Na2S2O3溶液20.00mL.(已知:I2+2Na2S2O3=2NaI+Na2S4O6)
①步骤二中使用磁力搅拌器进行搅拌的目的是
②通过计算确定聚合硫酸铝铁的化学式(写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】I.有一碳酸钠和碳酸氢钠混合物,取mg固体样品进行加热,完全分解产生CO2112mL;另取mg固体样品溶于水,向所得溶液中逐滴加入150mL稀盐酸时产生CO2112mL,盐酸过量时共产生CO2448mL(气体体积均在标准状况下测定)。
(1)碳酸氢钠与碳酸钠的物质的量之比为____ 。
(2)盐酸的浓度c(HCl)=____ (保留两位有效数字)。
II.用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
①2NO2+2NaOH=NaNO2+NaNO3+H2O
②NO+NO2+2NaOH=2NaNO2+H2O
现有VL某NaOH溶液,能完全吸收由nmolNO2和mmolNO组成的大气污染物:
(1)混合气体中NO2和NO若能完全被NaOH溶液吸收,则n与m的关系是:n___ m(用<、=、>、≥、≤表示)
(2)若所得溶液中c(NO ):c(NO
):c(NO )=1:9,则原混合气体中NO2和NO的物质的量之比n:m=
)=1:9,则原混合气体中NO2和NO的物质的量之比n:m=____ 。(写出计算过程)
(1)碳酸氢钠与碳酸钠的物质的量之比为
(2)盐酸的浓度c(HCl)=
II.用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
①2NO2+2NaOH=NaNO2+NaNO3+H2O
②NO+NO2+2NaOH=2NaNO2+H2O
现有VL某NaOH溶液,能完全吸收由nmolNO2和mmolNO组成的大气污染物:
(1)混合气体中NO2和NO若能完全被NaOH溶液吸收,则n与m的关系是:n
(2)若所得溶液中c(NO
 ):c(NO
):c(NO )=1:9,则原混合气体中NO2和NO的物质的量之比n:m=
)=1:9,则原混合气体中NO2和NO的物质的量之比n:m=
您最近一年使用:0次

 Si+2CO↑;Si+C
Si+2CO↑;Si+C


