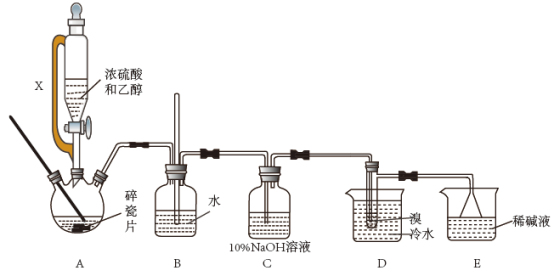
实验室用乙醇和浓硫酸反应制备乙烯,乙烯再与溴反应制备1,2—二溴乙烷。装置如图所示(加热及夹持装置省略):
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。
有关数据列表如下:
回答下列问题:
(1)该装置中盛放浓硫酸和乙醇的仪器名称___ ;装置B的作用__ 。
(2)装置C中10%NaOH溶液的作用___ 。
(3)在A中发生的化学反应方程式为___ 。
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是___ 。
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在__ (填“上”或“下”)层。
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是__ 。
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。

有关数据列表如下:
| 物质 | 乙醇 | 1,2—二溴乙烷 | 溴 |
| 密度g·cm-3 | 0.79 | 2.2 | 3.12 |
| 沸点/℃ | 78.5 | 132 | 59 |
(1)该装置中盛放浓硫酸和乙醇的仪器名称
(2)装置C中10%NaOH溶液的作用
(3)在A中发生的化学反应方程式为
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
更新时间:2021-05-07 13:59:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下面是实验室制乙烯并检验其性质的装置图,请回答:
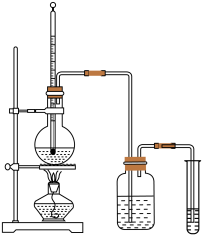
(1)写出圆底烧瓶中反应的方程式______________________________ ;
(2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式:____________________________________________ ;
(3)为了检验乙烯的生成及乙烯的不饱和性,试管中应盛放_________ ,现象为___________ ;
(4)洗瓶中盛放的试剂为____________________ ,作用__________________ .

(1)写出圆底烧瓶中反应的方程式
(2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式:
(3)为了检验乙烯的生成及乙烯的不饱和性,试管中应盛放
(4)洗瓶中盛放的试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ. 实验室制得气体中常含有杂质,影响其性质检验。
下图A为除杂装置,B为性质检验装置,完成下列表格:

Ⅱ. 为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同 时间,观察到如下现象。
(1)试管①中反应的化学方程式是________________________ ;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是______________ ;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因_____________ 。
下图A为除杂装置,B为性质检验装置,完成下列表格:

| 序号 | 气体 | 反应原理 | A中试剂 |
| ① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | |
| ② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是 | |
| ③ | 乙炔 | 电石与饱和食盐水反应 |
Ⅱ. 为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热
| 编号 | ① | ② | ③ |
| 实验操作 |  |  |  |
| 实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管①中反应的化学方程式是
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是
(3)试用化学平衡移动原理解释试管②中酯层消失的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学设计实验探究工业制乙烯的原理和乙烯主要的化学性质,实验装置如图所示。

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34 C8H18+甲,甲
C8H18+甲,甲 4乙,乙的结构简式为
4乙,乙的结构简式为___________ 。
(2)写出B中发生的化学反应方程式___________ 。
(3)C装置中的实验现象是___________ ,其中发生反应的反应类型是___________ 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置___________ (填序号)中的实验现象可判断该资料是否真实。
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是___________ (填序号,下同);除去甲烷中乙烯的方法是___________ 。
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。例如,石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34
 C8H18+甲,甲
C8H18+甲,甲 4乙,乙的结构简式为
4乙,乙的结构简式为(2)写出B中发生的化学反应方程式
(3)C装置中的实验现象是
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
(5)通过题述实验探究可知,检验甲烷和乙烯的方法是
A.气体通入水中 B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH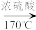 CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
已知:①乙醇在浓硫酸存在下在140℃脱水生成乙醚2CH3CH2OH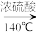 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量SO2和CO2,用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示:

有关数据列表如下:
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是________ 。要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是________ 。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是____________ 。
(3)在装置C中应加入NaOH溶液,其目的是_________ 。
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是_______ 。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在__________ 层(填“上”或“下”)。若产物中有少量未反应的Br2,最好用______ 洗涤除去;若产物中有少量副产物乙醚,可用_____ (填操作方法名称)的方法除去。
(6)若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为___________ 。
CH3CH2OH
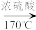 CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br
CH2=CH2+H2O CH2=CH2+Br2→BrCH2CH2Br已知:①乙醇在浓硫酸存在下在140℃脱水生成乙醚2CH3CH2OH
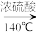 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O②实验中常因温度过高而使乙醇和浓硫酸反应生成少量SO2和CO2,用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示:

有关数据列表如下:
类别 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是
(3)在装置C中应加入NaOH溶液,其目的是
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
(6)若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用加热l-丁醇、溴化钠和浓H2SO4的混合物的方法来制备1-溴丁烷时,还会有烯、醚等副产物生成。反应结束后将反应混合物蒸馏,分离得到1-溴丁烷,已知相关有机物的性质如下:
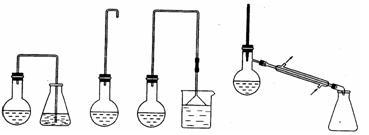
A B C D
⑴制备1-溴丁烷的装置应选用上图中的_______ (填序号)。反应加热时的温度不宜超过100℃,理由是______ 。
⑵制备操作中,加入的浓硫酸必需进行稀释,其目的是_____ 。(填字母)
A.减少副产物烯和醚的生成
b.减少Br2的生成
c.减少HBr的挥发
d.水是反应的催化剂
⑶反应结束后,将反应混合物中1-溴丁烷分离出来,应选用的装置是______ 。该操作应控制的温度(t)范围是_______ 。
⑷欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是______ 。(填字母)
A.NaI b.NaOH c.NaHSO3 d.KCl
| 熔点/℃ | 沸点/℃ | |
| 1-丁醇 | -89.53 | 117.25 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |

A B C D
⑴制备1-溴丁烷的装置应选用上图中的
⑵制备操作中,加入的浓硫酸必需进行稀释,其目的是
A.减少副产物烯和醚的生成
b.减少Br2的生成
c.减少HBr的挥发
d.水是反应的催化剂
⑶反应结束后,将反应混合物中1-溴丁烷分离出来,应选用的装置是
⑷欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是
A.NaI b.NaOH c.NaHSO3 d.KCl
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36g•cm-3.实验室制备少量1-溴丙烷的主要步骤如下:
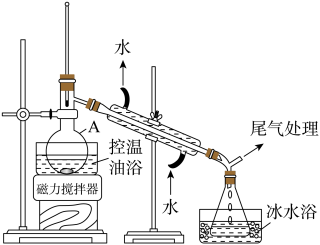
步骤1:在仪器A中加入搅拌磁子、12g正丙醇及20mL水,冰水冷却下缓慢加入28mL浓H2SO4;冷却至室温,搅拌下加入24gNaBr。
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12mLH2O、12mL5%Na2CO3溶液和12mLH2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
(1)步骤1发生反应的方程式为______
(2)仪器A的名称是______ ;加入搅拌磁子的目的是搅拌和______ 。
(3)反应时生成的主要有机副产物有______ 。
(4)反应过程中可以观察到A的上方出现红棕色气体,其电子式为______ 。
(5)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是______ 。同时可以观察到的现象是______ 。
(6)步骤4中三次洗涤分别洗去的主要杂质是①______ ②______ ③______ 。
(5)步骤4中②的Na2CO3溶液还可以用下列哪个试剂代替______
A. NaOH溶液 B. NaI溶液 C. Na2SO3溶液 D. CCl4

步骤1:在仪器A中加入搅拌磁子、12g正丙醇及20mL水,冰水冷却下缓慢加入28mL浓H2SO4;冷却至室温,搅拌下加入24gNaBr。
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12mLH2O、12mL5%Na2CO3溶液和12mLH2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
(1)步骤1发生反应的方程式为
(2)仪器A的名称是
(3)反应时生成的主要有机副产物有
(4)反应过程中可以观察到A的上方出现红棕色气体,其电子式为
(5)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是
(6)步骤4中三次洗涤分别洗去的主要杂质是①
(5)步骤4中②的Na2CO3溶液还可以用下列哪个试剂代替
A. NaOH溶液 B. NaI溶液 C. Na2SO3溶液 D. CCl4
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】1,2-二氯乙烷是杀菌剂稻瘟灵和植物生长调节剂矮壮素的中间体。它不溶于水,易溶于有机溶剂,沸点83.6℃;在光照下易分解:碱性条件下易水解。化学家们提出了“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如图。
已知:C2H5OH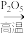 CH2=CH2↑+H2O;甘油的沸点为290℃。
CH2=CH2↑+H2O;甘油的沸点为290℃。

请回答以下问题:
(1)仪器A的名称是______ ,装置Ⅵ中水的作用是______ 。
(2)①装置Ⅳ中多孔球泡的作用是______ 。
②Ⅳ中反应前先加入少量1,2-二氯乙烷液体,其作用是______ (填序号)。
a.溶解Cl2和乙烯 b.作催化剂 c.促进气体反应物间的接触
③写出装置Ⅳ中发生的化学反应方程式______ ,反应类型为______ 。
(3)Ⅶ装置中采用甘油浴加热,该加热方式的优点是______ 。
(4)已知C4H8液相直接氯化法可生成1,2-二氯乙烷的同系物C4H8Cl2,满足分子式C4H8Cl2的同分异构体有______ 种,写出其中符合以下条件的同分异构体的结构简式______ 。
①核磁共振氢谱图有3组峰;②峰面积之比为1∶3∶4
已知:C2H5OH
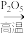 CH2=CH2↑+H2O;甘油的沸点为290℃。
CH2=CH2↑+H2O;甘油的沸点为290℃。
请回答以下问题:
(1)仪器A的名称是
(2)①装置Ⅳ中多孔球泡的作用是
②Ⅳ中反应前先加入少量1,2-二氯乙烷液体,其作用是
a.溶解Cl2和乙烯 b.作催化剂 c.促进气体反应物间的接触
③写出装置Ⅳ中发生的化学反应方程式
(3)Ⅶ装置中采用甘油浴加热,该加热方式的优点是
(4)已知C4H8液相直接氯化法可生成1,2-二氯乙烷的同系物C4H8Cl2,满足分子式C4H8Cl2的同分异构体有
①核磁共振氢谱图有3组峰;②峰面积之比为1∶3∶4
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】苯甲酸乙酯为无色透明液体,稍有水果气味,微溶于热水,易溶于很多有机物,用于配制香水、香精和人造精油。某同学利用如图装置制取并提纯苯甲酸乙酯。
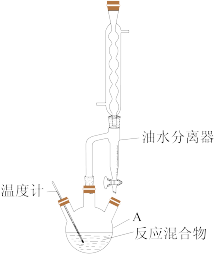
实验操作如下:
Ⅰ.合成反应:向仪器A中加入12.2 g苯甲酸、20 mL无水乙醇、25 mL环己烷和2片碎瓷片,搅拌后再加入2 mL浓硫酸。按图组装好仪器后,水浴加热回流1.5 h,已知:环己烷、乙醇和水可形成共沸物,混合物沸点为62.1℃。
Ⅱ.分离提纯:继续水浴加热蒸出多余的乙醇和环己烷,经油水分离器放出。剩余物质倒入盛有60 mL冷水的烧杯中,依次用饱和碳酸钠溶液、无水氯化钙处理后,再蒸馏纯化,收集213℃的馏分,得产品8.8 g。
已知部分实验数据如表所示:
回答下列问题:
(1)仪器A的名称为___________ 。
(2)实验中加入过量乙醇的目的是___________ ,分离提纯时加入饱和碳酸钠溶液的目的是___________ 。
(3)从平衡角度考虑,合成反应中油水分离器的作用是___________ 。
(4)制取苯甲酸乙酯的化学方程式为___________ 。
(5)该实验过程中苯甲酸乙酯的产率约为___________ %(结果保留小数点后一位)。

实验操作如下:
Ⅰ.合成反应:向仪器A中加入12.2 g苯甲酸、20 mL无水乙醇、25 mL环己烷和2片碎瓷片,搅拌后再加入2 mL浓硫酸。按图组装好仪器后,水浴加热回流1.5 h,已知:环己烷、乙醇和水可形成共沸物,混合物沸点为62.1℃。
Ⅱ.分离提纯:继续水浴加热蒸出多余的乙醇和环己烷,经油水分离器放出。剩余物质倒入盛有60 mL冷水的烧杯中,依次用饱和碳酸钠溶液、无水氯化钙处理后,再蒸馏纯化,收集213℃的馏分,得产品8.8 g。
已知部分实验数据如表所示:
| 相对分子质量 | 密度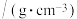 | 沸点 | 水中溶解性 | |
| 苯甲酸 | 122 | 1.266 | 249 | 微溶 |
| 乙醇 | 46 | 0.789 | 78.3 | 易溶 |
| 苯甲酸乙酯 | 150 | 1.045 | 213 | 难溶 |
| 环己烷 | 84 | 0.779 | 80.8 | 难溶 |
(1)仪器A的名称为
(2)实验中加入过量乙醇的目的是
(3)从平衡角度考虑,合成反应中油水分离器的作用是
(4)制取苯甲酸乙酯的化学方程式为
(5)该实验过程中苯甲酸乙酯的产率约为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】以环己醇( )为原料制取己二酸
)为原料制取己二酸 的实验流程如图:
的实验流程如图:
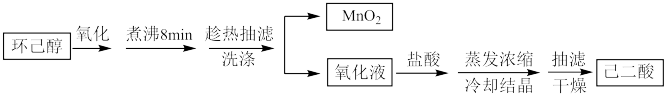
其中“氧化”的实验过程为:在 三颈烧瓶中加入
三颈烧瓶中加入 水和
水和 碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入
碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入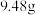 (约
(约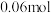 )高锰酸钾,按图示1组装好装置,打开磁力搅拌器,加热至35℃,滴加
)高锰酸钾,按图示1组装好装置,打开磁力搅拌器,加热至35℃,滴加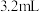 (约
(约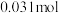 )环己醇,发生的主要反应为:
)环己醇,发生的主要反应为:


(1)图1中 的名称为
的名称为________ 。
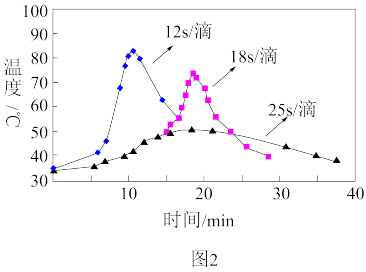
(2)“氧化”过程,不同环己醇滴加速度下,溶液温度随时间变化曲线如图2,为保证产品纯度,应选择的滴速为_________ 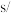 滴(“
滴(“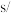 滴”指两滴间的间隔时间),选择的理由是
滴”指两滴间的间隔时间),选择的理由是_________ 。
(3)为证明“氧化”反应已结束,在滤纸上点1滴反应混合物,若观察到_________ ,则表明反应已经完成。
(4)“趁热抽滤”后,洗涤沉淀的操作为:__________ 。
(5)室温下,相关物质溶解度(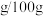 水)为:己二酸
水)为:己二酸 ,
, ,
,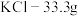 。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至
。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至_________ (填标号)。
A. B.
B. C.
C.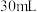 D.
D.
(6)称取己二酸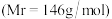 样品
样品 ,用新煮沸的
,用新煮沸的 热水溶解,滴入2滴酚酞试液,用
热水溶解,滴入2滴酚酞试液,用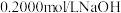 溶液滴定至终点,进行平行实验及空白实验后,消耗
溶液滴定至终点,进行平行实验及空白实验后,消耗 的平均体积为
的平均体积为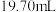 ,己二酸样品的纯度为
,己二酸样品的纯度为_________ 。
 )为原料制取己二酸
)为原料制取己二酸 的实验流程如图:
的实验流程如图:
其中“氧化”的实验过程为:在
 三颈烧瓶中加入
三颈烧瓶中加入 水和
水和 碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入
碳酸钠,低速搅拌至碳酸钠溶解,缓慢加入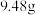 (约
(约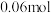 )高锰酸钾,按图示1组装好装置,打开磁力搅拌器,加热至35℃,滴加
)高锰酸钾,按图示1组装好装置,打开磁力搅拌器,加热至35℃,滴加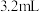 (约
(约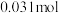 )环己醇,发生的主要反应为:
)环己醇,发生的主要反应为:


(1)图1中
 的名称为
的名称为(2)“氧化”过程,不同环己醇滴加速度下,溶液温度随时间变化曲线如图2,为保证产品纯度,应选择的滴速为
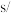 滴(“
滴(“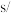 滴”指两滴间的间隔时间),选择的理由是
滴”指两滴间的间隔时间),选择的理由是(3)为证明“氧化”反应已结束,在滤纸上点1滴反应混合物,若观察到
(4)“趁热抽滤”后,洗涤沉淀的操作为:
(5)室温下,相关物质溶解度(
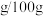 水)为:己二酸
水)为:己二酸 ,
, ,
,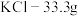 。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至
。“蒸发浓缩”过程中,为保证产品纯度及产量,应浓缩溶液体积至A.
 B.
B. C.
C.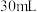 D.
D.
(6)称取己二酸
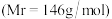 样品
样品 ,用新煮沸的
,用新煮沸的 热水溶解,滴入2滴酚酞试液,用
热水溶解,滴入2滴酚酞试液,用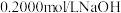 溶液滴定至终点,进行平行实验及空白实验后,消耗
溶液滴定至终点,进行平行实验及空白实验后,消耗 的平均体积为
的平均体积为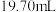 ,己二酸样品的纯度为
,己二酸样品的纯度为
您最近一年使用:0次



