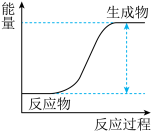
人们曾认为的N2+3H2 2NH3化学反应速率小,原料利用率低,不可能用于工业化生产,化学家们不断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。合成氨为放热反应,下列说法正确的是
2NH3化学反应速率小,原料利用率低,不可能用于工业化生产,化学家们不断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。合成氨为放热反应,下列说法正确的是
 2NH3化学反应速率小,原料利用率低,不可能用于工业化生产,化学家们不断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。合成氨为放热反应,下列说法正确的是
2NH3化学反应速率小,原料利用率低,不可能用于工业化生产,化学家们不断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。合成氨为放热反应,下列说法正确的是| A.断开H—H键放出能量 |
| B.反应物的总能量大于生成物的总能量 |
| C.形成N—H键吸收能量 |
| D.反应物的总能量小于生成物的总能量 |
20-21高一下·江苏苏州·期中 查看更多[2]
更新时间:2021-05-09 15:23:21
|
相似题推荐
单选题
|
容易
(0.94)
名校
【推荐1】已知C(石墨,s) = C(金刚石,s) △H>0,P(白磷,s) = P(红磷,s) △H<0。根据上述信息推论正确的是
| A.前者为放热反应 | B.红磷的能量比白磷低 |
| C.金刚石比石墨稳定 | D.上述变化都为物理变化 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列关于化学反应与能量的说法不正确 的是
| A.乙醇的燃烧是放热反应 |
| B.Mg与盐酸的反应是吸热反应 |
| C.反应物化学键的断裂要吸收能量 |
| D.化学反应伴随有能量的变化 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】氢气在氯气中燃烧为放热反应,下列说法正确的是
| A.断开H-H键放出能量 | B.形成H-Cl键吸收能量 |
| C.燃烧都是放热反应 | D.反应物的总能量小于生成物的总能量 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列说法中不正确的是
| A.物质发生化学变化都伴有能量的变化 |
| B.利用盖斯定律可间接计算通过实验难测定的反应的反应热 |
| C.吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量 |
| D.NH4NO3固体溶于水时吸热,属于吸热反应 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】下列反应中,属于吸热反应的是
| A.Na 与水反应 | B.甲烷的燃烧反应 |
| C.CaCO3 受热分解 | D.锌与盐酸反应 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列反应属于吸热反应的是
| A.KOH +HF = KF + H2O |
B.C + O2 CO2 CO2 |
| C.CaO + H2O = Ca(OH)2 |
D.NH4Cl + NaOH NH3↑ + H2O +NaCl NH3↑ + H2O +NaCl |
您最近一年使用:0次


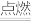 2HCl
2HCl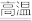 CaO+CO2↑
CaO+CO2↑

