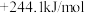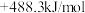下列说法中不正确的是
| A.物质发生化学变化都伴有能量的变化 |
| B.利用盖斯定律可间接计算通过实验难测定的反应的反应热 |
| C.吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量 |
| D.NH4NO3固体溶于水时吸热,属于吸热反应 |
更新时间:2023-09-23 21:09:35
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】下列关于化学反应与能量的说法不正确 的是
| A.乙醇的燃烧是放热反应 |
| B.Mg与盐酸的反应是吸热反应 |
| C.反应物化学键的断裂要吸收能量 |
| D.化学反应伴随有能量的变化 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】已知断裂 1 mol 共价键所需要吸收的能量分别为 H-H 键:436 kJ;I-I 键:153 kJ;H-I 键:299 kJ。下列对反应 H2(g)+I2(g)⇌2HI(g)的判断中,错误的是
| A.该反应是放出能量的反应 | B.该反应是吸收能量的反应 |
| C.该反应是氧化还原反应 | D.I2 与 H2 具有的总能量大于生成的 HI 具有的总能量 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐1】已知肼(N2H4)是一种用于火箭或燃料电池的原料,已知①2H2O(l)+O2(g)=2H2O2(l) △H1=+108.3kJ/mol②N2H4(l)+O2(g)=N2(g)+2H2O(l) △H2=-534.0kJ/mol。则有反应:N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)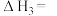 ,则ΔH3为
,则ΔH3为
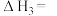 ,则ΔH3为
,则ΔH3为| A.+425.7kJ·mol-1 | B.-425.7kJ·mol-1 | C.+642.3kJ·mol-1 | D.-642.3kJ·mol-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】已知:2NO2(g) N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母) ( )
N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母) ( )
 N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母) ( )
N2O4(l) ΔH2,下列能量变化示意图中,正确的是(选填字母) ( )A.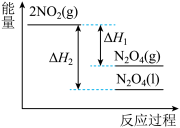 | B.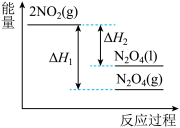 |
C.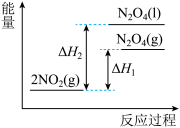 | D.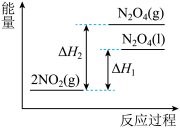 |
您最近一年使用:0次


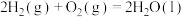
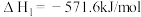

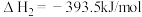
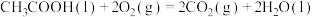
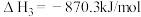
 的反应热
的反应热 为
为