A、B、C、D、E五种短周期元素,A是周期表中原子半径最小的元素,其中B、C同周期,B、D同主族,原子半径E>D>B>C>A.D原子核内质子数等于B、C原子电子数之和,D原子最外层电子数是E原子最外层电子数的4倍。试回答:
(1)B、C、D的最简单氢化物的稳定性由强到弱的顺序是___________ (填化学式);
(2)B与C形成的三原子分子甲的结构式是___________ ,C与E形成的原子个数比为1∶1的化合物乙的电子式是___________ ,乙物质中含有的共价键是___________ (填“极性”或“非极性”)
(3)B的简单氢化物与氯气的第一步反应的方程式为___________ ;
(4)A和B形成的化合物之一丙是一种重要的基本化工原料,其产量可以用来衡量一个国家的石油化工发展水平,写出由丙制得高聚物的反应方程式___________ ,该反应类型是___________ 。
(1)B、C、D的最简单氢化物的稳定性由强到弱的顺序是
(2)B与C形成的三原子分子甲的结构式是
(3)B的简单氢化物与氯气的第一步反应的方程式为
(4)A和B形成的化合物之一丙是一种重要的基本化工原料,其产量可以用来衡量一个国家的石油化工发展水平,写出由丙制得高聚物的反应方程式
更新时间:2021-05-11 11:52:59
|
相似题推荐
【推荐1】丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料,可以用乙烯、丙烯等石油化工产品为原料进行合成:
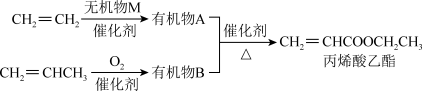
(1)乙烯是石油化学工业重要的基本原料,它的电子式为___________ 。
(2)无机物M的化学式为________ ;由乙烯生成有机物A的化学反应的类型是_______ 。
(3)有机物B中含有的官能团是___________ (填名称)。
(4)A与B反应生成丙烯酸乙酯的化学方程式是________ ,该反应的类型是_______ 。
(5)久置的丙烯酸乙酯自身会发生聚合反应,所得聚合物具有较好的弹性,可用于生产织物和皮革处理剂。请用化学方程式表示上述聚合过程_______ 。

(1)乙烯是石油化学工业重要的基本原料,它的电子式为
(2)无机物M的化学式为
(3)有机物B中含有的官能团是
(4)A与B反应生成丙烯酸乙酯的化学方程式是
(5)久置的丙烯酸乙酯自身会发生聚合反应,所得聚合物具有较好的弹性,可用于生产织物和皮革处理剂。请用化学方程式表示上述聚合过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】乙烯氧化法是生产氯乙烯的主要方法,其过程如图所示。

(1)下列关于乙烯、氯乙烯、乙烷的说法正确的是___________ (填字母)。
A.都能在氧气中燃烧
B.都能发生加成反应而使溴水褪色
C.都能使酸性高锰酸钾溶液褪色
(2)由乙烯生成乙醇的化学方程式为___________ 。
(3)反应①的反应类型是___________ 。
(4)聚氯乙烯的结构简式为___________ ,氯乙烯中所有原子___________ (填“在”或“不在”)同一平面。
(5)写出1,2-二氯乙烷同分异构体的结构简式:___________ 。

(1)下列关于乙烯、氯乙烯、乙烷的说法正确的是
A.都能在氧气中燃烧
B.都能发生加成反应而使溴水褪色
C.都能使酸性高锰酸钾溶液褪色
(2)由乙烯生成乙醇的化学方程式为
(3)反应①的反应类型是
(4)聚氯乙烯的结构简式为
(5)写出1,2-二氯乙烷同分异构体的结构简式:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】烃A的相对分子质量为28,B是一种高分子化合物。由A和D为原料合成F(丙烯酸乙酯)的转化关系如图:
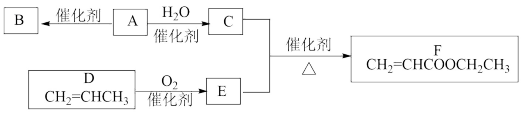
请回答:
(1)B的结构简式是_______ 。
(2)F中所含官能团的名称是碳碳双键和_______ 。
(3)C与E反应生成F的化学方程式是_______ 。
(4)下列说法正确的是_______。

请回答:
(1)B的结构简式是
(2)F中所含官能团的名称是碳碳双键和
(3)C与E反应生成F的化学方程式是
(4)下列说法正确的是_______。
| A.等质量的A和B完全燃烧消耗氧气的质量不相等 |
| B.仅用水无法鉴别C和F |
| C.在催化剂作用下D可发生加聚反应 |
| D.丙烯酸乙酯具有香味,能使酸性KMnO4溶液褪色 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D、E五种元素,它们的原子序数按E、C、D、A、B依次增大,E原子最外层有4个电子,A-和B+的核外电子排布相同,D的氢化物的化学式为H2D,D的最高价氧化物中D的质量分数为40%,且D原子核内质子数和中子数相等,C的原子序数比D少9,比B少12,其气态氢化物中氢的质量分数为17.65%。
(1)写出这五种元素的元素符号:
A___________ 、B___________ 、C___________ 、D___________ 、E___________ 。
(2)画出A-、B+的结构示意图___________ 、___________
(3)写出E的最高价氧化物与过量的B的最高价氧化物对应水化物反应的离子方程式:______ 。
(1)写出这五种元素的元素符号:
A
(2)画出A-、B+的结构示意图
(3)写出E的最高价氧化物与过量的B的最高价氧化物对应水化物反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D四种元素。其中A为第四周期元素,与D可行成1∶1和1∶2原子比的化合物。B为第四周期d区元素,最高化合价为7。C和B是同周期的元素,具有相同的最高化合价。D为所有元素中电负性第二大的元素。
(1)试写出四种元素的元素符号:A____ B____ C____ D____
(2)按电负性由大到小排列:________________ 。
(1)试写出四种元素的元素符号:A
(2)按电负性由大到小排列:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X; D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4倍;C与E同主族。请回答下列问题:
(1)依次写出A、B、C、D、E五种元素的名称_____ _____ _____ _____ _____ 。
(2)X的名称为_________ ,A、C、D构成的化合物中含有的化学键有_____________ 。
(3)下列各项中,能说明元素C比E非金属性强的事实有____________ (填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
④C与E组成化合物,C显负价
(4)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(ⅰ)浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ)NaOH溶液与BC2反应的化学方程式为:
2NaOH+2BC2 ====== NaBC2+NaBC3+ H2O, NaOH溶液与BC气体不反应。
装置①、②、③中盛放的药品依次是_________ 、_________ 、 ___________ 。
(5)通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是___________ (填一种气体的化学式)。
(1)依次写出A、B、C、D、E五种元素的名称
(2)X的名称为
(3)下列各项中,能说明元素C比E非金属性强的事实有
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
④C与E组成化合物,C显负价
(4)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(ⅰ)浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ)NaOH溶液与BC2反应的化学方程式为:
2NaOH+2BC2 ====== NaBC2+NaBC3+ H2O, NaOH溶液与BC气体不反应。
装置①、②、③中盛放的药品依次是
(5)通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E五种短周期元素,原子序数依次增大。A元素的单质是自然界最轻的气体,E单质须保存在煤油中。A与B、C分别构成电子数相等的化合物M、N,且M是一种能产生温室效应的最简单的有机气体物质;D元素最外层电子数是次外层电子数的3倍;回答下列问题:
(1)N的电子式为___________ ;M分子中含有______ (填“极性”或“非极性”)键
(2)D与E以1:1形成的化合物与水反应的化学反应方程式________________________
(3)A、B、C、D可形成阳离子和阴离子个数比是1∶1的离子化合物X;A、D、E可形成化合物Y;X与Y以物质的量之比1∶2加热反应,写出反应的化学方程式_____________________________
反应后水溶液显_____ (填“酸”“碱”或“中”)性,原因是___________________ (用离子方程式表示)
(4)由N与D的单质、KOH溶液构成原电池,负极会产生C的单质。则其负极反应为____________________ ;一段时间后,溶液pH________ (填“增大”“减小”或“不变”)。
(5)在一定温度下,将4 mol C单质和12 mol A单质通入到体积为2L的密闭容器中,发生反应,2 min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为________ ;该温度下的平衡常数为K=___________ 。
从化学平衡移动的角度分析,提高A单质的转化率可以采取的措施是________ (选填序号字母)。
a、及时分离出生成物 b、平衡后再加入6molA物质 c、增大压强 d、使用催化剂 e、平衡后再加入2molC物质
(1)N的电子式为
(2)D与E以1:1形成的化合物与水反应的化学反应方程式
(3)A、B、C、D可形成阳离子和阴离子个数比是1∶1的离子化合物X;A、D、E可形成化合物Y;X与Y以物质的量之比1∶2加热反应,写出反应的化学方程式
反应后水溶液显
(4)由N与D的单质、KOH溶液构成原电池,负极会产生C的单质。则其负极反应为
(5)在一定温度下,将4 mol C单质和12 mol A单质通入到体积为2L的密闭容器中,发生反应,2 min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为
从化学平衡移动的角度分析,提高A单质的转化率可以采取的措施是
a、及时分离出生成物 b、平衡后再加入6molA物质 c、增大压强 d、使用催化剂 e、平衡后再加入2molC物质
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】x、y、z、w、n为五种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:

请回答下列问题:
(1)w位于周期表中第__________ 周期,第__________ 族。
(2)n、z、w、三种元素最高价氧化物水化物的酸性由弱到强的顺序为:__________ (用化学式表示)。
(3)下列事实能说明y元素的非金属性比z元素的非金属性强的是____
(4)y和氢元素形成的10电子微粒中常见 价阳离子为
价阳离子为__________ (填化学式);z和氢元素形成的18电子微粒中常见 价阴离子的电子式为
价阴离子的电子式为__________ 。
(5)化合物nyz存在于天然气中,可以用NaOH溶液洗涤除去。化合物nyz的电子式为__________ ,其与NaOH溶液反应除生成两种正盐外,还有水生成,其化学方程式为__________ 。
(6)m元素的原子序数为__________ ,它是一种__________ 。(填“金属”或“非金属”)

请回答下列问题:
(1)w位于周期表中第
(2)n、z、w、三种元素最高价氧化物水化物的酸性由弱到强的顺序为:
(3)下列事实能说明y元素的非金属性比z元素的非金属性强的是____
| A.y单质与z的气态氢化物水溶液反应,溶液变浑浊 |
| B.在氧化还原反应中,1moly单质比1molz得电子多 |
| C.y和z两元素的简单氢化物受热分解,前者的分解温度高 |
| D.y元素最高价氧化物水化物酸性比z元素最高价氧化物水化物酸性强 |
 价阳离子为
价阳离子为 价阴离子的电子式为
价阴离子的电子式为(5)化合物nyz存在于天然气中,可以用NaOH溶液洗涤除去。化合物nyz的电子式为
(6)m元素的原子序数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期元素A、B、C、D、E的原子序数依次增大。A原子是元素周期表中原子半径最小的原子;B可以与A形成常温下常见的液态物质;C原子的最外层电子数为比最内层电子数少1;D单质在空气中点燃发出耀眼的白光;E是第3周期非金属性最强的元素。
(1)A、B形成的具有强氧化性的18电子的物质__ 。(填化学式)
(2)C、D最高价氧化物的水化物的碱性__ >__ 。(填化学式)
(3)B、C形成的简单离子半径大小__ >__ 。(填具体离子符号)
(4)E的最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式__ 。
(5)化合物CA与水反应生成A单质的化学方程式__ 。
(1)A、B形成的具有强氧化性的18电子的物质
(2)C、D最高价氧化物的水化物的碱性
(3)B、C形成的简单离子半径大小
(4)E的最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式
(5)化合物CA与水反应生成A单质的化学方程式
您最近一年使用:0次



