单斜硫和正交硫是硫的两种同素异形体,下列说法不正确的是


| A.正交硫比单斜硫稳定 |
| B.S(s,单间) =S(s,正交) △H3=-0.33 kJ/mol |
| C.相同物质的量的正交硫比单斜疏所含的能量高 |
| D.由②可知断裂l molO2和1 mol正交硫中的共价键所吸收的能量比形成1 mol SO2中的共价键所放出的能量多296.83 kJ |
更新时间:2021-05-28 11:08:25
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】单斜硫和正交硫是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)=SO2(g) ΔH1=-297.16kJ·mol-1
②S(正交,s)+O2(g)=SO2(g) ΔH2=-296.83kJ·mol-1
下列说法正确的是
已知:①S(单斜,s)+O2(g)=SO2(g) ΔH1=-297.16kJ·mol-1
②S(正交,s)+O2(g)=SO2(g) ΔH2=-296.83kJ·mol-1
下列说法正确的是
| A.S(单斜,s)=S(正交,s) ΔH3=+0.33kJ·mol-1 |
| B.正交硫比单斜硫稳定 |
| C.相同物质的量的正交硫比单斜硫所含有的能量低 |
| D.①式表示断裂1molO2中的化学键所吸收的能量比形成1molSO2中的化学键所放出的能量多297.16kJ |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列说法或表示方法不正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的能量少 |
| B.由H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ·mol -1可知,若将含 1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量大于57.3 kJ |
| C.由C(石墨)=C(金刚石)△H=+1.9 kJ·mol -1可知,石墨比金刚石稳定 |
| D.在100 kPa时,1 g H2完全燃烧生成液态水,放出285. 8 kJ热量,则H2燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ·mol -1 |
您最近一年使用:0次
【推荐3】下列示意图表示正确的是
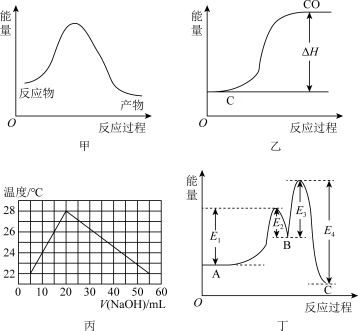

| A.甲图表示2Fe(s)+3CO2(g)=Fe2O3(s)+3CO(g) ΔH=-26.7kJ·mol-1反应的能量变化 |
| B.乙图表示碳的燃烧热 |
| C.丙图表示实验的环境温度为20℃,将物质的量浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,混合液的最高温度随V(NaOH)的变化(已知V1+V2=60mL) |
| D.已知稳定性顺序:B<A<C,某反应由两步反应A→B→C构成,反应过程中的能量变化曲线如丁图 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】已经298K、101kPa时,下列说法不正确的是
反应1:4Fe(s)+3O2(g) = 2Fe2O3 (s) ΔH1= -1648 kJ/mol
反应2:C(s) + O2 (g) = CO2 (g) ΔH2= -393 kJ/mol
反应3:2Fe(s)+2C(s) +3O2(g) = 2FeCO3(s) ΔH3= -1480 kJ/mol
反应4:2FeCO3(s) +1/2O2(g) =2CO2(g) +Fe2O3(s) ΔH4
反应1:4Fe(s)+3O2(g) = 2Fe2O3 (s) ΔH1= -1648 kJ/mol
反应2:C(s) + O2 (g) = CO2 (g) ΔH2= -393 kJ/mol
反应3:2Fe(s)+2C(s) +3O2(g) = 2FeCO3(s) ΔH3= -1480 kJ/mol
反应4:2FeCO3(s) +1/2O2(g) =2CO2(g) +Fe2O3(s) ΔH4
| A.上述反应1、2、3、4在热力学上自发趋势都很大 |
| B.反应1和3在较低温度下能自发反应,反应4是熵增反应 |
| C.自发反应代表反应一定能发生,可以判断过程的方向,但不能确定过程发生的速率 |
| D.反应1表示铁在氧气中燃烧的热化学方程式 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】氢能是清洁的绿色能源。现有一种太阳能两步法甲烷蒸气重整制氢工艺,反应原理为
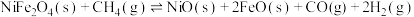

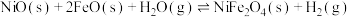

第Ⅰ、Ⅱ步反应的 关系如图所示。下列有关说法正确的是
关系如图所示。下列有关说法正确的是


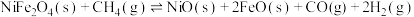

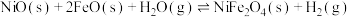

第Ⅰ、Ⅱ步反应的
 关系如图所示。下列有关说法正确的是
关系如图所示。下列有关说法正确的是

A.  |
B.1000℃时,反应 平衡常数 平衡常数 |
C.1000℃时,只考虑反应I时,第Ⅰ步反应平衡时 的平衡分压 的平衡分压 ,则第Ⅰ步反应平衡时混合气体中 ,则第Ⅰ步反应平衡时混合气体中 的体积分数为58.8% 的体积分数为58.8% |
D. 改变反应历程,降低了反应活化能,提升了反应物的平衡转化率 改变反应历程,降低了反应活化能,提升了反应物的平衡转化率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】以下反应中,Q1 >Q2的是
A.S(s)+O2(g) → SO2(g)+ Q1 kJ; S(g)+O2(g) → SO2(g)+ Q1 kJ; S(g)+O2(g) → SO2(g)+ Q2kJ → SO2(g)+ Q2kJ |
B.2H2(g)+O2(g) → 2H2O(l)+Q1 kJ ;2H2(g)+O2(g) → 2H2O(g)+Q2 kJ → 2H2O(l)+Q1 kJ ;2H2(g)+O2(g) → 2H2O(g)+Q2 kJ |
C.NaOH(aq)+HCl(aq) → NaCl(aq)+H2O(l)+Q1 kJ NaOH(aq)+CH3COOH(aq) →CH3COONa(aq)+H2O(l)+Q2 kJ → NaCl(aq)+H2O(l)+Q1 kJ NaOH(aq)+CH3COOH(aq) →CH3COONa(aq)+H2O(l)+Q2 kJ |
D.H2(g)+Cl2(g) → 2HCl(g)+Q1 kJ, H2(g)+F2(g) → 2HCl(g)+Q1 kJ, H2(g)+F2(g) → 2HF(g)+Q2 kJ → 2HF(g)+Q2 kJ |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】 的氯化、溴化反应势能图及产物选择性如下图,下列叙述错误的是
的氯化、溴化反应势能图及产物选择性如下图,下列叙述错误的是
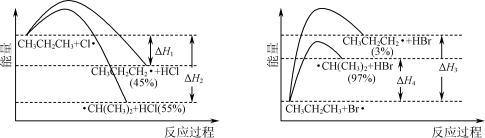
 的氯化、溴化反应势能图及产物选择性如下图,下列叙述错误的是
的氯化、溴化反应势能图及产物选择性如下图,下列叙述错误的是
A.丙烷中仲氢 比伯氢 比伯氢 活性强 活性强 |
B.升高温度 与 与 反应速率加快、与 反应速率加快、与 反应速率减慢 反应速率减慢 |
C.以 为原料合成2-丙醇时,溴化反应比氯化反应产率更高 为原料合成2-丙醇时,溴化反应比氯化反应产率更高 |
D. 和 和 的键能差=△H1-△H3 的键能差=△H1-△H3 |
您最近一年使用:0次
【推荐2】已知: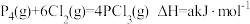 ,
,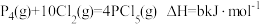 已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为
已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为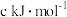 ,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是
,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是
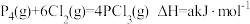 ,
,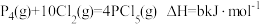 已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为
已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为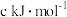 ,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是
,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是| A.P-P键的键能大于P-Cl键的键能 |
B.可求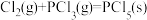 的反应热△H 的反应热△H |
C.P-P键的键能为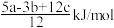 |
D.Cl-Cl键的键能为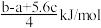 |
您最近一年使用:0次