硼氢化钠(NaBH4)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33℃)。工业上可用硼镁矿(主要成分为Mg2B2O5·H2O,含少量杂质Fe3O4)制取NaBH4,其工艺流程如下:
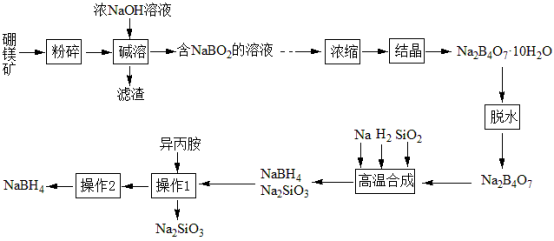
回答下列问题:
(1)NaBH4的电子式为___________ 。
(2)碱溶时Mg2B2O5发生反应的化学方程式是___________ 。
(3)滤渣的成分是___________ 。
(4)高温合成中,加料之前需将反应器加热至100℃以上并通入氩气,该操作的目的是___________ ,实验室取用少量金属钠用到的实验用品有___________ 、滤纸、玻璃片和小刀。
(5)操作2的名称为___________ 。流程中可循环利用的物质是___________ 。
(6)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1gNaBH4的还原能力相当于___________ gH2的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同,结果保留两位小数)。

回答下列问题:
(1)NaBH4的电子式为
(2)碱溶时Mg2B2O5发生反应的化学方程式是
(3)滤渣的成分是
(4)高温合成中,加料之前需将反应器加热至100℃以上并通入氩气,该操作的目的是
(5)操作2的名称为
(6)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1gNaBH4的还原能力相当于
更新时间:2021-06-04 07:22:01
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】若以X、Y和Z代表三种不同周期的短周期元素,其原子序数依次增大。且知:X与Y可形成原子个数比分别为1∶1的共价化合物甲和2∶1的共价化合物乙;Y与Z可形成原子个数比分别为1∶1的离子化合物丙和2∶1的离子化合物丁。请回答:
(1)元素Y在周期表中的位置为:第_______ 周期、第____ 族。
(2)化合物甲的结构式是______________________ 。
(3)化合物丙中的化学键类型有__________________________ 。
(4)Y的阴离子半径与Z的阳离子半径大小关系为:r(Yn-)________ r(Zm+)。
(1)元素Y在周期表中的位置为:第
(2)化合物甲的结构式是
(3)化合物丙中的化学键类型有
(4)Y的阴离子半径与Z的阳离子半径大小关系为:r(Yn-)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表为八种短周期主族元素的部分性质(已知铍的原子半径为0.89×10-10m):
(1)元素M在元素周期表中的位置为_________________________ 。
(2)写出X、Y、J三种元素形成的化合物电子式_________ 。用电子式表示X元素与Z元素形成化合物的过程:_______________________ 。
(3)写出Y与Q两种元素形成的化合物与J的最高价氧化物的水化物反应的离子方程式_____ 。
(4)R与T相比,非金属性较强的是_____ (用元素符号表示),下列事实能证明这一结论的是_______ (填字母)。
A.常温下T的单质呈固态,R的单质呈气态
B.R的氢化物比T的氢化物稳定
C.R的氢化物水溶液酸性比T的氧化物对应水化物酸性强
D.R与T形成的化合物中T呈正价
(5)J与Q相比,金属性较强的是____ (用元素符号表示),能证明这一结论的依据是______ 。
(6)根据表中数据推测,M的原子半径的最小范围是____________________ 。
| 元素代号 | X | Y | Z | M | R | J | Q | T |
| 原子半径/10-10m | 0.74 | 0.75 | 0.99 | 1.86 | 1.43 | 1.10 | ||
| 主要化合价 | -2 | +5、-3 | +4、-4 | +7、-1 | +1 | +3 | +5、-3 | |
| 其它 | 原子核内无中子 | 无机非金属材料主角 | 有两种氧化物 |
(2)写出X、Y、J三种元素形成的化合物电子式
(3)写出Y与Q两种元素形成的化合物与J的最高价氧化物的水化物反应的离子方程式
(4)R与T相比,非金属性较强的是
A.常温下T的单质呈固态,R的单质呈气态
B.R的氢化物比T的氢化物稳定
C.R的氢化物水溶液酸性比T的氧化物对应水化物酸性强
D.R与T形成的化合物中T呈正价
(5)J与Q相比,金属性较强的是
(6)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。回答下列问题:

(1)组成单质Y的元素在周期表中的位置是___________ ;M中存在的化学键类型为___________ ;R的化学式是___________ 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为___________ 。
(3)写出A和D的稀溶液反应生成G的离子方程式:___________ 。
(4)向含4mol D的稀溶液中,逐渐加入X粉末至过量。假设生成的气体只有一种,则n(X2+)的最大值为___________ 。

(1)组成单质Y的元素在周期表中的位置是
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为
(3)写出A和D的稀溶液反应生成G的离子方程式:
(4)向含4mol D的稀溶液中,逐渐加入X粉末至过量。假设生成的气体只有一种,则n(X2+)的最大值为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒,已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。(已知:淀粉遇I2变蓝色)
(1)上述反应的氧化剂是_____ ,氧化产物是____
(2)用双线桥标出上述反应电子转移的方向与数目:______
2NaNO2+4HI=2NO↑+I2+2NaI+2H2O
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,实验可选用的物质有:
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤食醋,下列合适的组合是_____ (填字母)。
A.③⑤ B.①②④ C.①②⑤ D.①②③⑤
(4)①某厂废切削液中,含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为________
该反应中的还原剂是________ ,氧化产物是_____ ,还原产物是______
②取200.00mL该厂废切削液,加入适量HI溶液,充分反应后,滴加一定浓度的Na2S2O3溶液,恰好完全反应时,消耗0.12mol Na2S2O3,计算所取废切削液中含NaNO2的质量。
(已知: ,写出计算过程,保留两位小数)
,写出计算过程,保留两位小数)
(1)上述反应的氧化剂是
(2)用双线桥标出上述反应电子转移的方向与数目:
2NaNO2+4HI=2NO↑+I2+2NaI+2H2O
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,实验可选用的物质有:
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤食醋,下列合适的组合是
A.③⑤ B.①②④ C.①②⑤ D.①②③⑤
(4)①某厂废切削液中,含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为
该反应中的还原剂是
②取200.00mL该厂废切削液,加入适量HI溶液,充分反应后,滴加一定浓度的Na2S2O3溶液,恰好完全反应时,消耗0.12mol Na2S2O3,计算所取废切削液中含NaNO2的质量。
(已知:
 ,写出计算过程,保留两位小数)
,写出计算过程,保留两位小数)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】金属铝在酸性或碱性溶液中均可与NO 发生氧化还原反应,转化关系如图:
发生氧化还原反应,转化关系如图:
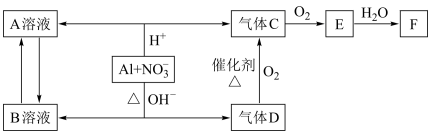
请回答下列问题:
(1)气体D和F反应可生成盐,该盐的化学式为___ 。
(2)将A转化为B,可选择的试剂是___ (填序号)。
a.CO2 b.NaOH c.CH3COOH d.NH3 e.HCl
(3)除去气体C中的杂质气体E的化学方法:将混合气体通入___ 中。
(4)Al与NO 在酸性条件下反应,Al与被还原的NO
在酸性条件下反应,Al与被还原的NO 的物质的量之比是
的物质的量之比是___ 。
(5)Al与NO 在碱性条件下反应的离子方程式为
在碱性条件下反应的离子方程式为___ 。
(6)含Al的化合物明矾[KAl(SO4)2•12H2O]常常用来净水,往明矾溶液中逐滴加入Ba(OH)2溶液,若使SO 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为___ 。
(7)1L1mol/L的F稀溶液中加入足量铁粉,充分反应后过滤,向滤液中至少再加入___ molH2SO4才能使反应后的溶液加入铁氰化钾不出现蓝色。
 发生氧化还原反应,转化关系如图:
发生氧化还原反应,转化关系如图:
请回答下列问题:
(1)气体D和F反应可生成盐,该盐的化学式为
(2)将A转化为B,可选择的试剂是
a.CO2 b.NaOH c.CH3COOH d.NH3 e.HCl
(3)除去气体C中的杂质气体E的化学方法:将混合气体通入
(4)Al与NO
 在酸性条件下反应,Al与被还原的NO
在酸性条件下反应,Al与被还原的NO 的物质的量之比是
的物质的量之比是(5)Al与NO
 在碱性条件下反应的离子方程式为
在碱性条件下反应的离子方程式为(6)含Al的化合物明矾[KAl(SO4)2•12H2O]常常用来净水,往明矾溶液中逐滴加入Ba(OH)2溶液,若使SO
 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为(7)1L1mol/L的F稀溶液中加入足量铁粉,充分反应后过滤,向滤液中至少再加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和NaClO。
和NaClO。

回答下列问题:
(1)a中的试剂为_______ 。
(2)b中反应的氧化剂和还原剂的质量比为_______ ,c中化学反应的离子方程式是_______ ,采用冰水浴冷却的目的是_______ 。
(3)d的作用是_______ ,可选用的最佳试剂为_______ (填标号)。
A. 溶液 B.饱和食盐水 C.KI溶液 D.浓
溶液 B.饱和食盐水 C.KI溶液 D.浓
(4)反应结束后,取出b中试管,经冷却结晶,_______ ,_______ ,干燥,得到 晶体。
晶体。
 和NaClO。
和NaClO。
回答下列问题:
(1)a中的试剂为
(2)b中反应的氧化剂和还原剂的质量比为
(3)d的作用是
A.
 溶液 B.饱和食盐水 C.KI溶液 D.浓
溶液 B.饱和食盐水 C.KI溶液 D.浓
(4)反应结束后,取出b中试管,经冷却结晶,
 晶体。
晶体。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】探究钠及其化合物的性质,请按要求填空:
(1)金属钠的性质活泼,应放在___________ 中保存。将等质量的钠分别在常温和加热条件下与氧气反应,反应过程中转移电子数之比为___________ 。
(2)将稀盐酸逐滴滴入碳酸钠溶液中,发生反应的离子方程式为___________ 、___________ 。
(3)某兴趣小组对久置于空气中的过氧化钠样品M进行实验探究。
实验Ⅰ:甲同学设计下图所示装置探究样品M的变质情况。
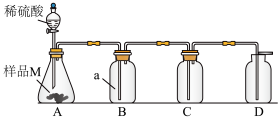
装置B中的溶液a为___________ (填化学式),若B中出现浑浊,D中收集到的气体能使带火星的木条复燃,则样品M部分变质。
实验Ⅱ:乙同学用氯化钡溶液作为检验试剂进行实验。
(4)根据产生白色沉淀,乙同学认为样品M已变质,该反应的离子方程式为___________ 。
资料显示,H2O2与BaCl2、NaOH溶液反应生成白色不溶物BaO2∙8H2O。据此,丙同学对乙同学的检验结果提出质疑并进行实验。
实验Ⅲ:取少量纯净的过氧化钠固体溶于蒸馏水,先加入过量稀硫酸,再滴入KMnO4溶液。实验证明Na2O2与水反应有H2O2生成。
(5)滴入KMnO4溶液后观察到的现象是溶液紫色褪去,冒出大量气泡,此反应的离子方程式为___________ 。
(1)金属钠的性质活泼,应放在
(2)将稀盐酸逐滴滴入碳酸钠溶液中,发生反应的离子方程式为
(3)某兴趣小组对久置于空气中的过氧化钠样品M进行实验探究。
实验Ⅰ:甲同学设计下图所示装置探究样品M的变质情况。

装置B中的溶液a为
实验Ⅱ:乙同学用氯化钡溶液作为检验试剂进行实验。
(4)根据产生白色沉淀,乙同学认为样品M已变质,该反应的离子方程式为
资料显示,H2O2与BaCl2、NaOH溶液反应生成白色不溶物BaO2∙8H2O。据此,丙同学对乙同学的检验结果提出质疑并进行实验。
实验Ⅲ:取少量纯净的过氧化钠固体溶于蒸馏水,先加入过量稀硫酸,再滴入KMnO4溶液。实验证明Na2O2与水反应有H2O2生成。
(5)滴入KMnO4溶液后观察到的现象是溶液紫色褪去,冒出大量气泡,此反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】有人设计出一种让Na与CuSO4,溶液反应的方法.实验时,往100mL大试管中先加40mL煤油,取3粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加煤油入CuSO4溶液使煤油的液面至胶塞,并夹紧弹簧夹(如图)仔细观察,回答下列问题:

(1)从试剂瓶中取用金属钠需要_______ (填所用工具或耗材名称)。剩余的Na____________ (能/不能)放回原试剂瓶。
(2)有关钠反应的现象是____________
(3)大试管的溶液中出现的现象:____________
(4)装置中液面的变化____________
(5)写出钠与硫酸铜溶液反应的化学方程式:____________

(1)从试剂瓶中取用金属钠需要
(2)有关钠反应的现象是
(3)大试管的溶液中出现的现象:
(4)装置中液面的变化
(5)写出钠与硫酸铜溶液反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某课外活动小组为了探究钠与MgSO4溶液的反应,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒金属钠,再从U形管左端加入MgSO4溶液,一段时间后加热铜丝。回答下列问题:
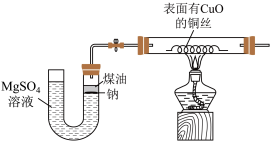
(1)实验室的钠保存在________ 中,从试剂瓶取出后剩余的Na能否放回原试剂瓶? ________ (填“能”或“否”)。
(2)U形管中出现的现象是________(填字母)。
(3)写出钠与MgSO4溶液反应的化学方程式:_____________________ (可分步写)。
(4)铜丝的变化现象是________ ,写出该化学反应方程式____________ 。

(1)实验室的钠保存在
(2)U形管中出现的现象是________(填字母)。
| A.有气泡生成,钠熔化成小球 |
| B.钠在煤油面上四处游动 |
| C.溶液中有银白色金属生成 |
| D.溶液变浑浊 |
(4)铜丝的变化现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】已知某工业废水中含有大量FeSO4,较多的Cu2+,极少量的Na+ 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。

(1)步骤1的主要操作是___ ,需用到的玻璃仪器除烧杯外还有___ 。
(2)固体混合物是____ (填化学式)
(3)步骤3中发生反应的化学方程式为___ 。
(4)步骤4中涉及的操作是:蒸发浓缩、___ 、过滤、洗涤、干燥。
(5)火法制得的粗铜中常混有少量氧化亚铜(Cu2O),氧化亚铜溶于稀硫酸溶液变蓝。试写出该反应的离子方程式___ 。

(1)步骤1的主要操作是
(2)固体混合物是
(3)步骤3中发生反应的化学方程式为
(4)步骤4中涉及的操作是:蒸发浓缩、
(5)火法制得的粗铜中常混有少量氧化亚铜(Cu2O),氧化亚铜溶于稀硫酸溶液变蓝。试写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氧化钴(Co2O3)粉体材料在工业、电子、电讯等领域都有着广阔的应用前景。某铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等。由该矿石制备Co2O3的部分工艺流程如下:
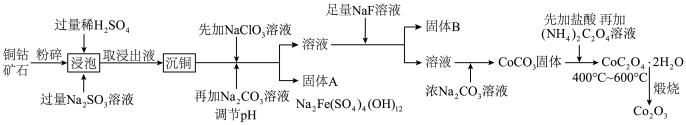
请回答下列问题:
(1)“浸泡”过程中,CoO(OH)可转化为CoSO4,请将该反应的化学方程式补充完整:
2CoO(OH)+2H2SO4+□_______=□CoSO4+□_______+□_______,_____________
(2)固体B的成分是______________________ (填化学式)。
(3)向“沉铜”后的滤液中加入NaClO3溶液的主要目的是___________________ ;若上述流程中固、液分离均采用过滤操作,则共有________________ 处使用该操作。
(4)根据图1、图2分析:
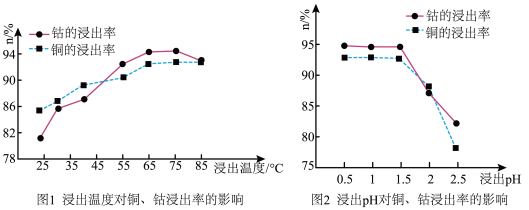
①矿石粉末浸泡的适宜条件应是________________________________ 。
②图2中铜、钴浸出率下降的可能原因是___________________________________ 。
(5)CoC2O4·2H2O在空气中高温煅烧得到Co2O3的化学方程式是_____________ 。
(6)LiCoO2可用于电动汽车的电池,其工作原理如右图所示,且电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为:LixC6+Li1-xCoO2 C6 +LiCoO2
C6 +LiCoO2

①放电时,Li+移动的方向为_________ →___________ 。(填“ 左”或“ 右”)
②放电时正极的电极反应式为______________________________________ 。

请回答下列问题:
(1)“浸泡”过程中,CoO(OH)可转化为CoSO4,请将该反应的化学方程式补充完整:
2CoO(OH)+2H2SO4+□_______=□CoSO4+□_______+□_______,
(2)固体B的成分是
(3)向“沉铜”后的滤液中加入NaClO3溶液的主要目的是
(4)根据图1、图2分析:

①矿石粉末浸泡的适宜条件应是
②图2中铜、钴浸出率下降的可能原因是
(5)CoC2O4·2H2O在空气中高温煅烧得到Co2O3的化学方程式是
(6)LiCoO2可用于电动汽车的电池,其工作原理如右图所示,且电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为:LixC6+Li1-xCoO2
 C6 +LiCoO2
C6 +LiCoO2
①放电时,Li+移动的方向为
②放电时正极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】以含锂电解铝废渣(主要成分为LiF、AlF3、NaF,少量CaO等)为原料,生产碳酸锂的工艺流程如下:(已知:常温下,LiOH可溶于水,Li2CO3微溶于水)

(1)含锂电解铝废渣与浓硫酸在200~400 ℃条件下反应2 h,加水浸取后过滤,得到的滤渣主要成分是________ (填化学式)。
(2)流程中浸取后的过滤操作需要趁热在恒温装置中进行,否则会导致Li2SO4的收率下降,原因是________________ 。(已知部分物质的溶解度数据见下表)
(3)40℃下进行碱解反应,得到粗碳酸锂与氢氧化铝的混合滤渣,生成氢氧化铝的离子方程式为_______________________ 。
(4)苛化过程中加入的氧化钙将不溶性的碳酸锂转化成氢氧化锂溶液。若氧化钙过量,则可能会造成_____________________ 。
(5)碳化反应中,CO2的吸收采用了气、液逆流的方式,这样做的优点是________ 。整个工艺流程中可以循环利用的物质有________ 。

(1)含锂电解铝废渣与浓硫酸在200~400 ℃条件下反应2 h,加水浸取后过滤,得到的滤渣主要成分是
(2)流程中浸取后的过滤操作需要趁热在恒温装置中进行,否则会导致Li2SO4的收率下降,原因是
温度/℃ | Li2SO4/g | Al2(SO4)3/g | Na2SO4/g |
0 | 36.1 | 31.2 | 4.9 |
(4)苛化过程中加入的氧化钙将不溶性的碳酸锂转化成氢氧化锂溶液。若氧化钙过量,则可能会造成
(5)碳化反应中,CO2的吸收采用了气、液逆流的方式,这样做的优点是
您最近一年使用:0次



