I.通常将一定量的有机物充分燃烧转化为简单的无机物,根据产物的质量确定有机物的组成。如图所示是用燃烧法确定有机物分子式的常用装置,将含有C、H、O的有机物3.24 g装入元素分析装置,通入足量的O2使之完全燃烧,实验过程中CaCl2管(B)增加了2.16 g和NaOH(A)管增加了9.24 g,试回答。
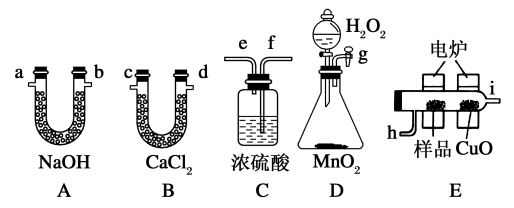
(1)使产生的O2按从左到右的方向流动,则所选装置中各导管的正确连接顺序是________ 。
(2)装置C中浓硫酸的作用是________ ,燃烧管中CuO的作用是__________ 。
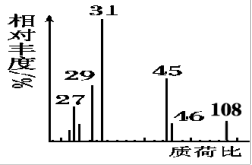
(3)已知质谱仪分析如图,则该有机物的分子式为________________ 。
II.实验室通过苯与浓硫酸和浓硝酸的混合液在50~60 ℃的水浴中加热制备硝基苯。
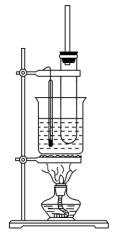
已知苯与硝基苯的某些物理性质如表所示。
(1)添加药品时的操作是________________________ 。
(2)用水浴加热的优点是____________ ;
(3)大试管上安装一长导管的作用是:________________________ 。
(4)简述获得纯净的溴苯应进行的实验操作:________________________ 。
III.认真观察下列装置,回答下列问题:
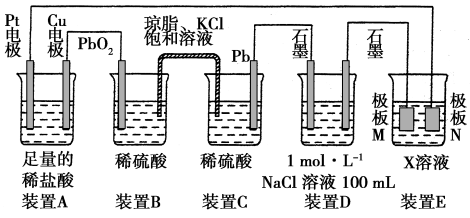
(1)装置B中PbO2上发生的电极反应方程式为_________________________ 。
(2)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为________ L(标准状况下)

(1)使产生的O2按从左到右的方向流动,则所选装置中各导管的正确连接顺序是
(2)装置C中浓硫酸的作用是
(3)已知质谱仪分析如图,则该有机物的分子式为

II.实验室通过苯与浓硫酸和浓硝酸的混合液在50~60 ℃的水浴中加热制备硝基苯。

已知苯与硝基苯的某些物理性质如表所示。
| 熔点/℃ | 沸点/℃ | 状态 | |
| 苯 | 5.5 | 80.1 | 液体 |
| 硝基苯 | 5.7 | 210.9 | 液体 |
(2)用水浴加热的优点是
(3)大试管上安装一长导管的作用是:
(4)简述获得纯净的溴苯应进行的实验操作:
III.认真观察下列装置,回答下列问题:

(1)装置B中PbO2上发生的电极反应方程式为
(2)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为
更新时间:2021-05-23 10:46:43
|
相似题推荐
【推荐1】二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.请回答下列问题:
(1)煤的气化的主要化学反应方程式为:______ .
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)⇌CH3OH(g)△H=-90.8kJ•mol-1
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41.3kJ•mol-1
写出水煤气直接合成二甲醚同时生成CO2的热化学反应方程式______ .
(3)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是______ .
a.高温低压
b.低温高压
c.减少CO2的浓度
d.增加CO的浓度
e.分离出二甲醚
f.加入催化剂
(4)已知反应②2CH3OH(g)⇌CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
比较此时正、逆反应速率的大小:v正______ v逆(填“>”、“<”或“=”),若上述情况达到平衡,此时c(CH3OH)= ______
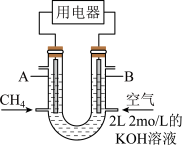
(5)将CH4设计成燃料电池,其装置示意如图(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL.
①0<V≤44.8L时,电池总反应方程式为______ ;
②44.8L<V≤89.6L时,负极电极反应为______ ;
③V=67.2L时,溶液中阴离子浓度大小关系为______ .

(1)煤的气化的主要化学反应方程式为:
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)⇌CH3OH(g)△H=-90.8kJ•mol-1
②2CH3OH(g)⇌CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41.3kJ•mol-1
写出水煤气直接合成二甲醚同时生成CO2的热化学反应方程式
(3)一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
a.高温低压
b.低温高压
c.减少CO2的浓度
d.增加CO的浓度
e.分离出二甲醚
f.加入催化剂
(4)已知反应②2CH3OH(g)⇌CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
比较此时正、逆反应速率的大小:v正
(5)将CH4设计成燃料电池,其装置示意如图(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL.
①0<V≤44.8L时,电池总反应方程式为
②44.8L<V≤89.6L时,负极电极反应为
③V=67.2L时,溶液中阴离子浓度大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)电池是一种将化学能直接转化为电能的装置,它的出现极大方便了人们的生活。如图为三种电池的示意图:
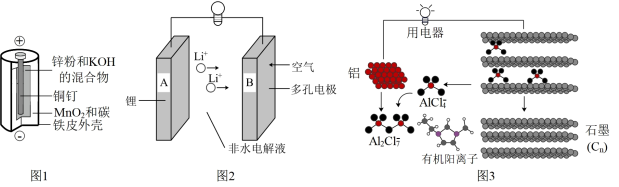
图1中碱性锌锰电池正极反应方程式是_____ 。
(2)锂-空气电池的理论能量密度高,是未来电动汽车续航里程的关键。锂-空气电池的反应原理可表示为:2Li+O2 Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或
Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或_____ 。
结论:H2O降低锂-空气电池放电、充电循环性能。
(3)铝离子电池高效耐用、超快充电、高安全性、可折叠、材料成本低等优势。已知图3的正极反应物为CnAlCl4,请写出负极的电极反应式:_____ 。
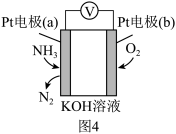
(4)图4所示装置为电化学气敏传感器,通过电压表示数可测量环境中NH3的含量。电极a上发生的电极反应为_____ 。
(1)电池是一种将化学能直接转化为电能的装置,它的出现极大方便了人们的生活。如图为三种电池的示意图:

图1中碱性锌锰电池正极反应方程式是
(2)锂-空气电池的理论能量密度高,是未来电动汽车续航里程的关键。锂-空气电池的反应原理可表示为:2Li+O2
 Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或
Li2O2。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质:A极产物:LiOH;B极产物:Li2O2、LiOH,B电极产生LiOH的电极反应方程式是2Li2O2+2H2O=4LiOH+O2↑或结论:H2O降低锂-空气电池放电、充电循环性能。
(3)铝离子电池高效耐用、超快充电、高安全性、可折叠、材料成本低等优势。已知图3的正极反应物为CnAlCl4,请写出负极的电极反应式:
(4)图4所示装置为电化学气敏传感器,通过电压表示数可测量环境中NH3的含量。电极a上发生的电极反应为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,只在c、d两极上共收集到336 mL(标准况)气体。回答:
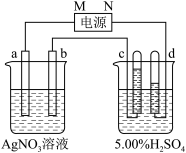
(1)直流电源中,M为_______ 极。
(2)Pt电极上生成的物质是_______ ,其质量为_______ g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为2:_______ :_______ :_______ 。
(4)AgNO3溶液的浓度_______ ,(填“增大”、“减小”或“不变”,下同),AgNO3溶液的pH_______ ,H2SO4溶液的浓度_______ 。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为_______ g。

(1)直流电源中,M为
(2)Pt电极上生成的物质是
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为2:
(4)AgNO3溶液的浓度
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】中国科学家首次实现了二氧化碳到淀粉的从头合成,相关成果由国际知名学术期刊《科学》在线发表,因此CO2的捕集及其资源化利用成为科学家研究的重要课题。
I.二氧化碳合成“合成气”
(1)捕获的高浓度CO2能与CH4制备合成气(CO、H2),该过程主要涉及以下反应:
①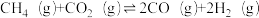 ;△H1
;△H1
②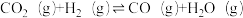 ;△H2
;△H2
③ ;△H3
;△H3
④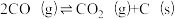 ;△H4
;△H4
根据盖斯定律,反应①的△H1=_____________ (写出代数式即可)。
Ⅱ.二氧化碳合成低碳烯烃
(2)用可再生能源电还原CO2时,采用高浓度的K+抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图1所示。阴极发生的反应为____________ ;
每转移1mol电子,阳极生成____________ L气体(标准状况)。
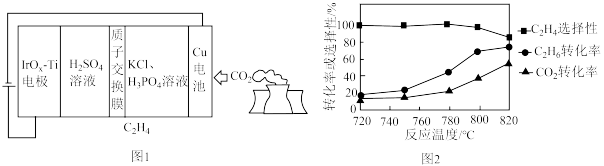
(3)以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
A.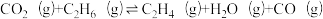 ;
; (主反应)
(主反应)
B.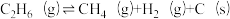 ;
;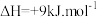 (副反应)
(副反应)
其中,反应A的反应历程可分为如下两步:
A. ;△H1(反应速率较快)
;△H1(反应速率较快)
B. ;
;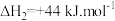 (反应速率较慢)
(反应速率较慢)
相比于提高c(C2H6),则提高c(CO2)对反应A速率影响更大,原因是____________ 。
向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂KFeMn/Si2性能的影响如图2所示,工业生产综合各方面的因素,反应选择800℃的原因是____________ 。
Ⅲ.二氧化碳合成甲醇
主反应: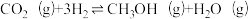 ;
;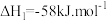
副反应: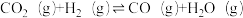 ;
;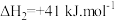
某一刚性容器中充入1molCO2和3molH2,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图3所示。已知:CH3OH选择性=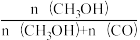
(4)240℃平衡时,生成的CH3OH的物质的量是____________ 。

Ⅳ、新型二氧化碳固定法
(5)某课题组设计一种新型的固定CO2方法,如图4所示。若原料用 ,则产物为
,则产物为____________ 。
I.二氧化碳合成“合成气”
(1)捕获的高浓度CO2能与CH4制备合成气(CO、H2),该过程主要涉及以下反应:
①
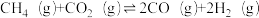 ;△H1
;△H1②
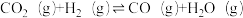 ;△H2
;△H2③
 ;△H3
;△H3④
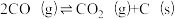 ;△H4
;△H4根据盖斯定律,反应①的△H1=
Ⅱ.二氧化碳合成低碳烯烃
(2)用可再生能源电还原CO2时,采用高浓度的K+抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图1所示。阴极发生的反应为
每转移1mol电子,阳极生成
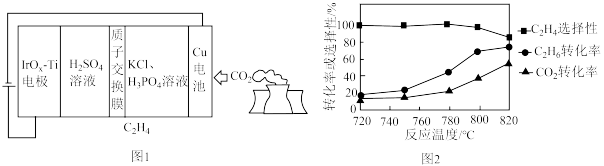
(3)以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
A.
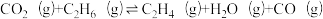 ;
; (主反应)
(主反应)B.
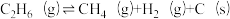 ;
;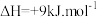 (副反应)
(副反应)其中,反应A的反应历程可分为如下两步:
A.
 ;△H1(反应速率较快)
;△H1(反应速率较快)B.
 ;
;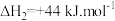 (反应速率较慢)
(反应速率较慢)相比于提高c(C2H6),则提高c(CO2)对反应A速率影响更大,原因是
向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂KFeMn/Si2性能的影响如图2所示,工业生产综合各方面的因素,反应选择800℃的原因是
Ⅲ.二氧化碳合成甲醇
主反应:
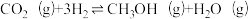 ;
;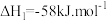
副反应:
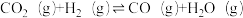 ;
;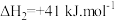
某一刚性容器中充入1molCO2和3molH2,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图3所示。已知:CH3OH选择性=
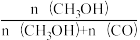
(4)240℃平衡时,生成的CH3OH的物质的量是

Ⅳ、新型二氧化碳固定法
(5)某课题组设计一种新型的固定CO2方法,如图4所示。若原料用
 ,则产物为
,则产物为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】十九大报告中提出要“打赢蓝天保卫战”,意味着对污染防治比过去要求更高. 和
和 是主要大气污染物,科学处理这些污染物对改善人们的生存环境具有重要的现实意义。
是主要大气污染物,科学处理这些污染物对改善人们的生存环境具有重要的现实意义。
Ⅰ.甲科研小组设计如图装置吸收 ,实现了“制硫酸、发电、环保”三位一体的结合。
,实现了“制硫酸、发电、环保”三位一体的结合。
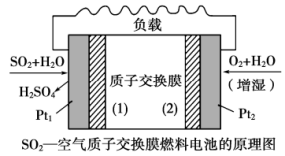
(1)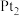 电极为
电极为_______ 极, 电极反应式为
电极反应式为_______ 。
(2)若负载通过 电子时,可以吸收
电子时,可以吸收 的体积为
的体积为_______ L(标准状况)。
Ⅱ.乙科研小组设计如图装置可以同时吸收 和
和 ,提高了吸收效率。
,提高了吸收效率。
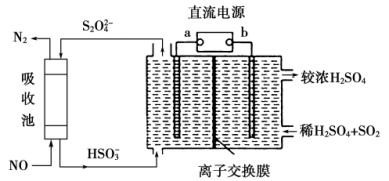
(3)a为直流电源的_______ 极,与a相连的电极反应式为_______ 。
(4)离子交换膜选择_______ (填“阳离子交换膜”或“阴离子交换膜”)。
(5)吸收池中发生反应的离子方程式为_______ 。
 和
和 是主要大气污染物,科学处理这些污染物对改善人们的生存环境具有重要的现实意义。
是主要大气污染物,科学处理这些污染物对改善人们的生存环境具有重要的现实意义。Ⅰ.甲科研小组设计如图装置吸收
 ,实现了“制硫酸、发电、环保”三位一体的结合。
,实现了“制硫酸、发电、环保”三位一体的结合。
(1)
 电极为
电极为 电极反应式为
电极反应式为(2)若负载通过
 电子时,可以吸收
电子时,可以吸收 的体积为
的体积为Ⅱ.乙科研小组设计如图装置可以同时吸收
 和
和 ,提高了吸收效率。
,提高了吸收效率。
(3)a为直流电源的
(4)离子交换膜选择
(5)吸收池中发生反应的离子方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】第1小题:下表所示的是关于有机物A、B的信息:
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的产物的名称为______________ 。
(2) B具有的性质是________ (填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤能使酸性KMnO4溶液和溴水褪色 ⑥任何条件下均不与氢气反应 ⑦与溴水混合后液体分层且上层呈橙红色
(3) A的同系物用通式CnHm表示,B的同系物用通式CxHy表示,当CnHm、CxHy分别出现同分异构体时,碳原子数的最小值n=________ ,x=________ 。
第2小题:有如下图所示某有机物,根据该有机物的结构回答: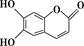
①该物质中的含氧官能团有________ 、________ (写名称,下同),此外还含有的官能团是________ 。
②该物质既可以与溴水发生________ 反应和________ 反应,也可以与酸性KMnO4溶液因发生______ 反应而使其褪色,当遇到FeCl3溶液时发生显色反应而呈________ 色。
③若1 mol该物质与足量H2反应,消耗H2的物质的量为________ ,若与足量溴水反应,消耗Br2的物质的量为________ ,若与足量氢氧化钠溶液反应,消耗NaOH的物质的量为________ 。
| A | B |
| ①能使溴的四氯化碳溶液褪色 ②分子比例模型为  ③能与水在一定条件下反应 | ①由C、H两种元素组成 ②分子球棍模型为 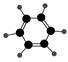 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的产物的名称为
(2) B具有的性质是
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤能使酸性KMnO4溶液和溴水褪色 ⑥任何条件下均不与氢气反应 ⑦与溴水混合后液体分层且上层呈橙红色
(3) A的同系物用通式CnHm表示,B的同系物用通式CxHy表示,当CnHm、CxHy分别出现同分异构体时,碳原子数的最小值n=
第2小题:有如下图所示某有机物,根据该有机物的结构回答:

①该物质中的含氧官能团有
②该物质既可以与溴水发生
③若1 mol该物质与足量H2反应,消耗H2的物质的量为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为___________ 。
(2)A与溴的四氯化碳溶液反应的化学方程式为___________ ,反应类型是___________ 。
(3)已知: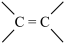

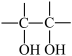 。
。
请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式:___________ 。
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式:___________ 。
(5)在一定条件下,由A得到的高分子化合物的结构简式为___________ 。
(6)已知 有10种二氯取代物,则其六氯取代物有___________。
有10种二氯取代物,则其六氯取代物有___________。
(7)下图是立方烷的球棍模型,下列有关说法不正确的是___________。
(1)A的分子式为
(2)A与溴的四氯化碳溶液反应的化学方程式为
(3)已知:
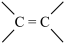

 。
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式:
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式:
(5)在一定条件下,由A得到的高分子化合物的结构简式为
(6)已知
 有10种二氯取代物,则其六氯取代物有___________。
有10种二氯取代物,则其六氯取代物有___________。| A.6种 | B.8种 | C.10种 | D.12种 |
(7)下图是立方烷的球棍模型,下列有关说法不正确的是___________。

| A.它的一氯代物只有一种 |
| B.它的二氯代物有两种 |
| C.它的核磁共振氢谱图上只有一种峰 |
| D.它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】纳豆是一种减肥食品,从其中分离出一种由C、H、O三种元素组成的有机物A,为确定其结构现进行如下实验:
①相同条件下,测得A的蒸气密度是H2密度的60倍;
②6gA在一定条件下完全燃烧,生成3.36L二氧化碳(标况)和1.8g水;
③1mol物质A发生酯化反应,转化完全时消耗乙醇92g,等量的A能与足量的金属钠反应放出33.6L氢气(标况)。
(1)A的相对分子质量为_______ ;
(2)A的分子式为_________ ;
(3)A的结构简式________ 。
①相同条件下,测得A的蒸气密度是H2密度的60倍;
②6gA在一定条件下完全燃烧,生成3.36L二氧化碳(标况)和1.8g水;
③1mol物质A发生酯化反应,转化完全时消耗乙醇92g,等量的A能与足量的金属钠反应放出33.6L氢气(标况)。
(1)A的相对分子质量为
(2)A的分子式为
(3)A的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】有四种烃:①乙烷;②乙烯;③乙炔;④苯。
(1)这四种烃分子中的碳碳键键长由长到短的顺序为_______ (用数字表示)
(2)实验室制取②乙烯的原理方程式为_______ 。将反应得到的气体直接通入酸性高锰酸钾溶液中,发现溶液紫红色褪色,则_______ (填“能”或“不能”)证明乙烯发生了氧化反应。
(3)工业上用乙炔合成聚氯乙烯的反应方程式为_______ 、_______ 。
(4)苯是常用的有机原料。若按照下图装置用苯制备硝基苯,存在的错误是_______ 、_______ 。反应一段时间后混合液明显分层,其中硝基苯在_______ (填“上”或“下”)层。若所得硝基苯呈黄色,则除去其中杂质可用的试剂是_______ ,所需主要玻璃仪器的名称是_______ 。

(1)这四种烃分子中的碳碳键键长由长到短的顺序为
(2)实验室制取②乙烯的原理方程式为
(3)工业上用乙炔合成聚氯乙烯的反应方程式为
(4)苯是常用的有机原料。若按照下图装置用苯制备硝基苯,存在的错误是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室以浓硫酸(50.00mL)、浓硝酸(39.00mL,密度1.40g/mL)、苯(39.00mL,密度0.88g/mL)为原料,制备并提纯一定量的硝基苯(密度1.205g/mL)流程如图。
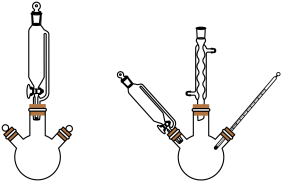
配置混酸→制硝基苯→精制硝基苯
请回答下列问题:
(1)配制混酸时,将250mL三颈烧瓶置于冰水浴中,加入搅拌磁子,先向其中先加入______ ,开启磁力搅拌器,然后再______ 。
(2)制取硝基苯的反应过程中经历了如下反应:
①HNO3+2H2SO4 H3O++NO
H3O++NO +2HSO
+2HSO
②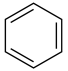 +NO
+NO →
→
③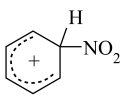 +HSO
+HSO →
→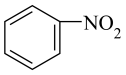 +H2SO4
+H2SO4
则生成硝基苯的总反应方程式为______ 。
(3)上述制取硝基苯的反应为放热反应,温度为100~110℃时生成间二硝基苯。为减少副反应的发生,除水浴加热外,还采用______ ,将反应温度控制在50~60℃。
(4)粗硝基苯精制实验操作中,依次进行的操作顺序为水洗、_____ 蒸馏。(操作可以重复,填序号)
①稀NaOH溶液洗 ②水洗 ③分液 ④向产品中加入CaCl2 ⑤过滤
(5)上述“水洗”实验室里常在______ (填序号)仪器中进行。
(6)若最终得到33.68mL精制产品,则该次实验硝基苯的产率是______ (保留三位有效数字)。
(7)实验结束后的产品处理方式为______ 。试对制硝基苯装置进行评价______ 。

配置混酸→制硝基苯→精制硝基苯
请回答下列问题:
(1)配制混酸时,将250mL三颈烧瓶置于冰水浴中,加入搅拌磁子,先向其中先加入
(2)制取硝基苯的反应过程中经历了如下反应:
①HNO3+2H2SO4
 H3O++NO
H3O++NO +2HSO
+2HSO
②
 +NO
+NO →
→
③
 +HSO
+HSO →
→ +H2SO4
+H2SO4则生成硝基苯的总反应方程式为
(3)上述制取硝基苯的反应为放热反应,温度为100~110℃时生成间二硝基苯。为减少副反应的发生,除水浴加热外,还采用
(4)粗硝基苯精制实验操作中,依次进行的操作顺序为水洗、
①稀NaOH溶液洗 ②水洗 ③分液 ④向产品中加入CaCl2 ⑤过滤
(5)上述“水洗”实验室里常在
A. | B.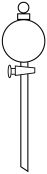 | C. | D.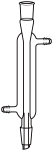 |
(6)若最终得到33.68mL精制产品,则该次实验硝基苯的产率是
(7)实验结束后的产品处理方式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】对乙酰氨苯酚(M)是常用的消炎解热镇痛药。其合成路线如下:
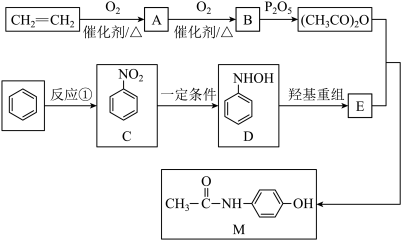
完成下列填空:
(1)A的结构简式为____________ 。C→D的反应类型为___________________ 。
(2)实验室中进行反应①的实验时添加试剂的顺序为________________________ 。
(3)下列有关E的说法正确的是____________ 。(选填编号)
a.分子式为C6H6NO b.能与溴水发生加成反应
c.遇到FeCl3溶液能发生显色反应 d.既能和氢氧化钠溶液反应,又能和盐酸反应
(4)已知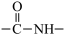 与
与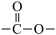 的性质相似,写出一定条件下M与NaOH溶液反应的化学方程式。
的性质相似,写出一定条件下M与NaOH溶液反应的化学方程式。______________________
(5)满足下列条件的M的同分异构体有_____________ 种。
①苯环上只有两种不同环境的氢原子;②苯环上连有-NH2;③属于酯类物质。
(6)N-邻苯二甲酰甘氨酸(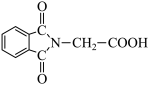 )是重要的化工中间体,工业上以邻二甲苯和甘氨酸(NH2-CH2-COOH)为原料通过一系列的反应制取该化合物,请参照上述流程的相关信息,写出最后一步反应的化学方程式。
)是重要的化工中间体,工业上以邻二甲苯和甘氨酸(NH2-CH2-COOH)为原料通过一系列的反应制取该化合物,请参照上述流程的相关信息,写出最后一步反应的化学方程式。_____________________

完成下列填空:
(1)A的结构简式为
(2)实验室中进行反应①的实验时添加试剂的顺序为
(3)下列有关E的说法正确的是
a.分子式为C6H6NO b.能与溴水发生加成反应
c.遇到FeCl3溶液能发生显色反应 d.既能和氢氧化钠溶液反应,又能和盐酸反应
(4)已知
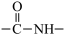 与
与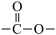 的性质相似,写出一定条件下M与NaOH溶液反应的化学方程式。
的性质相似,写出一定条件下M与NaOH溶液反应的化学方程式。(5)满足下列条件的M的同分异构体有
①苯环上只有两种不同环境的氢原子;②苯环上连有-NH2;③属于酯类物质。
(6)N-邻苯二甲酰甘氨酸(
 )是重要的化工中间体,工业上以邻二甲苯和甘氨酸(NH2-CH2-COOH)为原料通过一系列的反应制取该化合物,请参照上述流程的相关信息,写出最后一步反应的化学方程式。
)是重要的化工中间体,工业上以邻二甲苯和甘氨酸(NH2-CH2-COOH)为原料通过一系列的反应制取该化合物,请参照上述流程的相关信息,写出最后一步反应的化学方程式。
您最近一年使用:0次



