二氧化硫是一种应用广泛的化工原料。在接触法制硫酸的工业中,二氧化硫制取三氧化硫的反应为2SO2(g)+O2(g) = 2SO3(g) ∆H= -196 kJ•mol-1.实验室用亚硫酸钠固体与70%的硫酸制取少量的二氧化硫。下列有关用二氧化硫制取三氧化硫的说法正确的是
| A.反应的∆S > 0 |
| B.2 mol SO2与足量O2反应,放出的热量为196 kJ |
| C.工业上用通入足量的空气来提高SO2的转化率 |
| D.反应中每消耗1 mol SO2转移的电子数目约等于4×6.02×1023 |
更新时间:2021-05-22 22:53:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】科研人员提出CeO2催化合成DMC需经历三步反应,示意图如图:
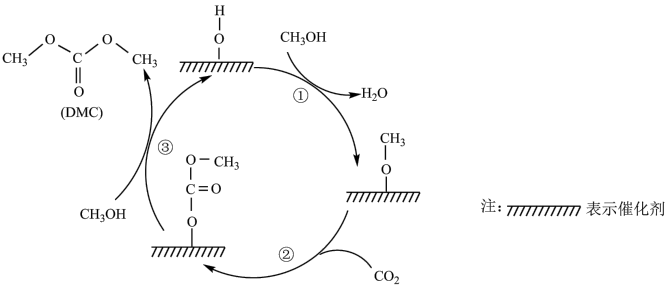
下列说法正确的是( )

下列说法正确的是( )
| A.DMC与过量NaOH溶液反应生成CO32-和甲醇 |
| B.CeO2可有效提高反应物的平衡转化率 |
| C.①、②、③中均有O—H的断裂 |
| D.生成DMC总反应的原子利用率为100% |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】消除天然气中H2S是能源领域的热点,利用CuFe2O4表面吸附H2S时,华中科技大学李钰等研究表明有两种机理途径,如图所示。
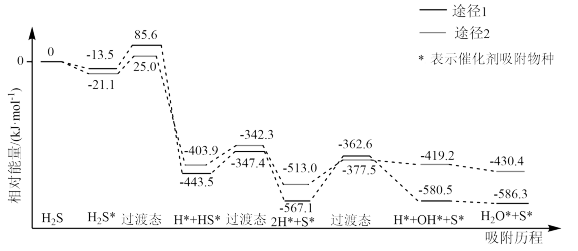
下列说法错误的是

下列说法错误的是
| A.该吸附过程释放能量 |
| B.途径1历程中最大活化能为204.5kJ·mol-1 |
| C.H2S*=HS*+H*的速率:途径1>途径2 |
| D.CuFe2O4在吸附过程中提供了O原子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】关于下列图象说法正确的是
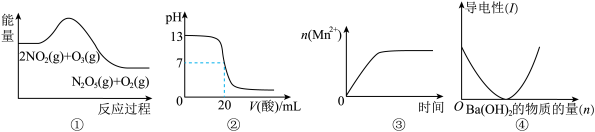

| A.①表示化学反应2NO2(g) + O3(g) = N2O5(g) + O2(g) ΔH > 0 |
| B.②表示25℃时,用0.1 mol/L CH3COOH溶液滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化 |
| C.③表示10 mL 0.01 mol/L酸性KMnO4溶液与过量的0.1 mol/L H2C2O4溶液混合时, n (Mn2+) 随时间的变化 |
| D.④可表示向稀硫酸溶液中滴加氢氧化钡溶液,溶液导电性随氢氧化钡物质的量的变化 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是
A.工业制硫酸的接触室中发生反应: 。该反应在500℃和催化剂存在下进行,原因是该反应为吸热反应 。该反应在500℃和催化剂存在下进行,原因是该反应为吸热反应 |
| B.对于可逆反应N2+3H2⇌2NH3,增大氮气浓度可增加活化分子百分数,从而使反应速率加快 |
| C.将AlCl3溶液和Al2(SO4)3溶液分别蒸干后再灼烧,所得固体产物均为Al2O3 |
| D.恒容密闭容器中进行的反应3A(g)⇌B(g)+C(g),在其他条件不变的情况下,再充入一定量的A气体,A的转化率将增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
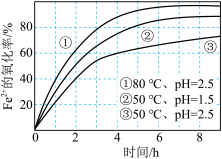
【推荐2】在不同条件下,用 氧化一定浓度
氧化一定浓度 溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
 氧化一定浓度
氧化一定浓度 溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
A.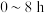 内, 内, 的氧化率随时间延长而逐渐增大 的氧化率随时间延长而逐渐增大 |
B.由曲线②和③可知,pH越大, 的氧化速率越快 的氧化速率越快 |
C.由曲线①和③可知,温度越高, 的氧化速率越快 的氧化速率越快 |
D.氧化过程的离子方程式为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】空气中的硫酸盐会加剧雾霾的形成,我国科学家用下列实验研究其成因:反应室底部盛有不同吸收液。将SO2和NO按一定比例混合,以N2或空气为载气通入反应室,相同时间后,检测吸收液中SO42-的含量.数据如下表所示,下列说法正确的是
| 反应室 | 载气 | 吸收液 | SO42-含量 | 数据分析 |
| ① | n2 | 蒸馏水 | a | i.b≈d>a≈c ii.若起始不通入NO2,则最终测不到SO42- |
| ② | 3%氨水 | b | ||
| ③ | 空气 | 蒸馏水 | c | |
| ④ | 3%氨水 | d |
| A.实验表明;酸性环境下,更有利于硫酸盐的形成 |
| B.反应室①中可能发生反应:SO2+2NO2+2H2O = H2SO4+2HNO2 |
| C.本研究表明:硫酸盐的形成主要与空气中的O2有关 |
| D.燃煤产生的气体盲目排放只会引起酸雨而不会加剧雾霾形成 |
您最近半年使用:0次



