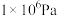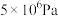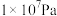空气中的硫酸盐会加剧雾霾的形成,我国科学家用下列实验研究其成因:反应室底部盛有不同吸收液。将SO2和NO按一定比例混合,以N2或空气为载气通入反应室,相同时间后,检测吸收液中SO42-的含量.数据如下表所示,下列说法正确的是
| 反应室 | 载气 | 吸收液 | SO42-含量 | 数据分析 |
| ① | n2 | 蒸馏水 | a | i.b≈d>a≈c ii.若起始不通入NO2,则最终测不到SO42- |
| ② | 3%氨水 | b | ||
| ③ | 空气 | 蒸馏水 | c | |
| ④ | 3%氨水 | d |
| A.实验表明;酸性环境下,更有利于硫酸盐的形成 |
| B.反应室①中可能发生反应:SO2+2NO2+2H2O = H2SO4+2HNO2 |
| C.本研究表明:硫酸盐的形成主要与空气中的O2有关 |
| D.燃煤产生的气体盲目排放只会引起酸雨而不会加剧雾霾形成 |
18-19高三·湖南·阶段练习 查看更多[3]
(已下线)2021年高考化学押题预测卷(湖南卷)02(含考试版、答题卡、参考答案、全解全析)湖北省鄂州市泽林高中2019-2020学年高一上学期期末联考化学试题湖南省长沙市第一中学2020届高三第二次月考化学试题
更新时间:2019-10-05 19:03:33
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】水是一种常见的物质,有很多物质能与水发生反应,在不同反应中,水的作用不相同。下列反应中,水作还原剂的是
| A.2F2+2H2O = 4HF+O2 | B.3NO2+H2O = 2HNO3+NO |
| C.2Na2O2+2H2O = 4NaOH+O2↑ | D.CaO+H2O = Ca(OH)2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】部分含氮物质的分类与相应氮元素化合价关系如图所示。下列说法不正确的是


A.常温下,a的水溶液 |
| B.一定条件下,b可以转化为a或c,该过程属于氮的固定 |
| C.一定条件下,c、d、e之间存在转化关系:c→d→e |
| D.实验室用e的浓溶液与Cu反应制备d,可用排水法收集 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是( )
| A.1 mol任何物质的体积都是22.4 L |
| B.在标准状况下,某气体的体积为22.4 L,则该气体的物质的量为1 mol,所含的分子数目约为6.02×1023 |
| C.当温度高于0 ℃时,一定量任何气体的体积都大于22.4 L |
| D.当压强大于101 kPa时,1 mol任何气体的体积都小于22.4 L |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】如图1为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨。用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。下列说法正确的是
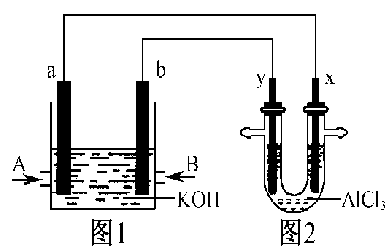

| A.A处通入的气体为CH4,电极反应式为:CH4+10OH--8e-===CO32-+7H2O |
B.图2中电解AlCl3溶液的总反应为:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.图1中电解质溶液的pH增大 |
| D.电解池中Cl-向x极移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】如图有关图示分析正确的是







| A.如图a所示,集气瓶内充満Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,焼杯中的水会进入集气瓶,并可能充满集气瓶 |
| B.如图b所示,X为铁棒,Y为铜棒,M为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入M |
| C.Pt内电极, 电解含0.10 mol M+和0.1 molN3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图c,离子氧化能力M+>N3+>H+ |
| D.图d为N2(g)和O2(g)生成NO(g)过程中的能量变化,则N-N的键能为946kJ·mol-1,其热化学方程式为N2(g)+O2(g)=2NO(g) △H=-180 kJ·mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
| A.使用催化剂,可加快反应速率,目的是提高生产效率 |
| B.使用冰箱保存食物,是利用了化学反应速率理论 |
| C.化学反应速率理论是研究怎样提高原料转化率 |
| D.化学平衡理论是研究怎样使用有限原料多出产品 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】压强为3MPa时,将NO和O3按一定体积比通入容器中,发生如下反应:
反应I:NO(g)+O3(g)⇌NO2(g)+O2(g);ΔH<0
反应II:2O3(g)⇌3O2(g);ΔH>0
O3的平衡转化率及NO、NO2的平衡体积分数随温度变化如图所示。下列说法正确的是
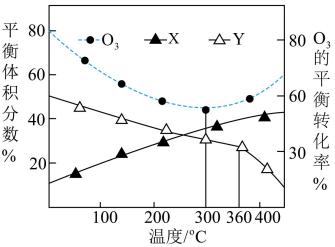
反应I:NO(g)+O3(g)⇌NO2(g)+O2(g);ΔH<0
反应II:2O3(g)⇌3O2(g);ΔH>0
O3的平衡转化率及NO、NO2的平衡体积分数随温度变化如图所示。下列说法正确的是

| A.图中X代表NO2,Y代表NO |
| B.低于300℃发生反应I,高于300℃发生反应II |
| C.其他条件不变,将压强变为4MPa,平衡时NO、NO2的体积分数不变 |
| D.高于360℃,Y的平衡体积分数减小的幅度大于X的平衡体积分数增大的幅度的原因可能是O3将Y氧化为更高价态的氧化物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列设计的实验方案能达到相应实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 探究化学反应的限度 | 取5mL0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5~6滴,充分反应,可根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应 |
| B | 探究浓度对化学反应速率的影响 | 用两支试管各取5mL0.1mol/L的KMnO4溶液,分别加入2mL0.1mol/L和0.2mol/L的H2C2O4(草酸)溶液,记录溶液褪色所需的时间 |
| C | 验证醋酸钠溶液中存在水解平衡 | 取CH3COONa溶液于试管中并加入几滴酚酞试剂,再加入醋酸铵固体其水溶液呈中性,观察溶液颜色变化 |
| D | 证明溴乙烷的消去反应有乙烯生成 | 将NaOH的乙醇溶液加入溴乙烷中加热,将产生的气体直接通入酸性KMnO4溶液中 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
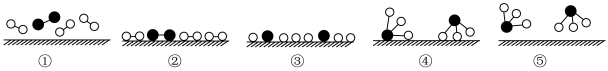
【推荐1】氨是化肥工业和基本有机化工的主要原料,工业采用N2和H2合成氨的催化过程如下图所示。已知合成氨的反应为放热反应,下列说法正确的是

| A.使用催化剂可改变反应的△H |
| B.过程③到④形成N—H吸收能量 |
| C.升高温度,合成氨反应的平衡常数减小 |
| D.催化剂可有效提高反应物的平衡转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用于净化汽车尾气的反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
 2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
2CO2(g)+N2(g),已知常温下该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是| A.该反应在常温下进行不需要催化剂 |
| B.提高尾气净化效率的最佳途径是研制高效催化剂 |
| C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| D.570K时该反应正向进行的程度很大,故使用催化剂并无实际意义 |
您最近半年使用:0次


 ,
, 的平衡转化率与压强、温度的关系如下表所示:
的平衡转化率与压强、温度的关系如下表所示: