如图有关图示分析正确的是







| A.如图a所示,集气瓶内充満Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,焼杯中的水会进入集气瓶,并可能充满集气瓶 |
| B.如图b所示,X为铁棒,Y为铜棒,M为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入M |
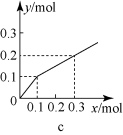
| C.Pt内电极, 电解含0.10 mol M+和0.1 molN3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图c,离子氧化能力M+>N3+>H+ |
| D.图d为N2(g)和O2(g)生成NO(g)过程中的能量变化,则N-N的键能为946kJ·mol-1,其热化学方程式为N2(g)+O2(g)=2NO(g) △H=-180 kJ·mol-1 |
更新时间:2018-06-15 12:55:28
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温下,将1.000 mol/L盐酸滴入20.00 mL 1.000 mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是


| A.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
B.a点由水电离出的c(H+)=1.0 mol/L mol/L |
C.b点:c(NH )+c(NH3·H2O)=c(Cl-) )+c(NH3·H2O)=c(Cl-) |
D.c点:c(Cl-)=c(NH ) ) |
您最近一年使用:0次
【推荐2】下列有关说法正确的是
A.常温下,向NH4Cl溶液中加入少量盐酸,溶液中 的值增大 的值增大 |
| B.一定温度下向恒容密闭容器中充入SO2和O2,当反应到达平衡时,容器中SO2、O2 、SO3的物质的量之比为2∶1∶2 |
| C.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
| D.反应N2(g)+3H2(g)⇌2NH3(g)的ΔH可通过下式估算:ΔH=反应中形成新共价键的键能之和−反应中断裂旧共价键的键能之和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】铅酸蓄电池历史悠久,至今仍在许多领域发挥着重要作用,其总反应式为: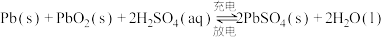 。如图是铅蓄电池的模拟装置图,下列说法正确的是
。如图是铅蓄电池的模拟装置图,下列说法正确的是
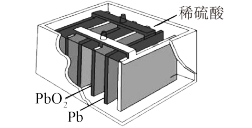
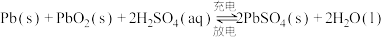 。如图是铅蓄电池的模拟装置图,下列说法正确的是
。如图是铅蓄电池的模拟装置图,下列说法正确的是
| A.该铅蓄电池属于化学电源中的一次电池,可以多次重复使用 |
B.放电时,负极铅被氧化最终生成 ,硫酸浓度没有变化 ,硫酸浓度没有变化 |
C.充电时, 与外接电源的正极相连,发生氧化反应 与外接电源的正极相连,发生氧化反应 |
D.充电时,阴极发生的电极反应式为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,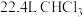 中含有的原子数为 中含有的原子数为 |
B. 溶液中,含有的阳离子数目大于 溶液中,含有的阳离子数目大于 |
C.常温下, 的醋酸钠溶液中,水电离出的 的醋酸钠溶液中,水电离出的 数为 数为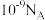 |
D.在铜的电解精炼中,当电路中通过的电子数为 时,阳极应有 时,阳极应有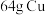 转化为 转化为 |
您最近一年使用:0次

 催化
催化 直接加氢得到二甲醚,助力碳中和催化剂
直接加氢得到二甲醚,助力碳中和催化剂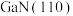 界面上的反应历程如图b,其反应为
界面上的反应历程如图b,其反应为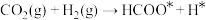 ,在
,在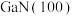 界面上发生的反应为
界面上发生的反应为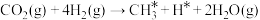 。下列说法不正确的是
。下列说法不正确的是

 中含有
中含有 键和
键和 键
键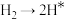 过程放热,
过程放热, 过程放热
过程放热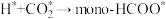
 交界面上的总反应为
交界面上的总反应为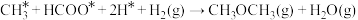
 +6H+
+6H+

