1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
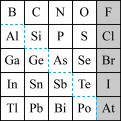
(1)元素Ga的原子结构示意图___________ ,镓(Ga)的氯化物与氨水反应的化学方程式为___________ ,
(2)Ge 的最高价氧化物对应水化物的化学式为___________ ,Bi的最高价氧化物为___________ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是___________ 元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___________ (填“>”“<”或“=”)H2SeO4。
③金属性比较:Tl___________ (填“>”“<”或“=”)Sn。
④氢化物的还原性:H2S___________ (填“>”“<”或“=”)H2O。
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___________ 。

(1)元素Ga的原子结构示意图
(2)Ge 的最高价氧化物对应水化物的化学式为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③金属性比较:Tl
④氢化物的还原性:H2S
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
更新时间:2021-05-24 09:39:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】获得2016-2017年度“影响世界华人大奖”提名的“美女科学家”颜宁教授解析出了人类葡萄糖转运蛋白GLUT家族的结构,为生命科学开启了新的篇章。目前发现的葡萄糖转运蛋白有六种,它们含有C、H、O、N、P、Na、Mg、Fe等元素,请回答下列问题:
(1)下列说法正确的是________ 。
A.葡萄糖转运蛋白中的元素全部是主族元素
B.葡萄糖转运蛋白中的元素分别位于四个不同周期
C.氢化物稳定性CH4>NH3>H2O
D.离子半径大小O2−>Na+>Mg2+
(2)铊能使葡萄糖转运蛋白失去生理活性,铊的相关信息卡片如图所示:

铊在周期表中的位置是________ 。下列推断正确的是________ 。
A.Tl原子的质量数为81 B.Tl在周期表中第13列
C.Tl元素位于金属与非金属分界线旁边 D.氧化性:Tl3+>Al3+
(3)X、Y为葡萄糖转运蛋白中含有的元素,W、Z是短周期元素,其原子半径随原子序数变化如图所示。已知X的一种核素的质量数为18,中子数为10;Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强。
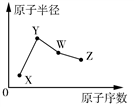
①画出X的阴离子的结构示意图:________ 。
②用电子式表示Z的氢化物的形成过程:________________ 。
③Y的金属性与Mg的金属性相比,________ (写化学式)的金属性强,请用实验证明它们金属性的相对强弱:_______________________________________________ 。
④写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学方程式:____________________ 。
⑤工业上经常用W的氧化物制取W单质的粗产品,化学方程式为______________ 。
(1)下列说法正确的是
A.葡萄糖转运蛋白中的元素全部是主族元素
B.葡萄糖转运蛋白中的元素分别位于四个不同周期
C.氢化物稳定性CH4>NH3>H2O
D.离子半径大小O2−>Na+>Mg2+
(2)铊能使葡萄糖转运蛋白失去生理活性,铊的相关信息卡片如图所示:

铊在周期表中的位置是
A.Tl原子的质量数为81 B.Tl在周期表中第13列
C.Tl元素位于金属与非金属分界线旁边 D.氧化性:Tl3+>Al3+
(3)X、Y为葡萄糖转运蛋白中含有的元素,W、Z是短周期元素,其原子半径随原子序数变化如图所示。已知X的一种核素的质量数为18,中子数为10;Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强。

①画出X的阴离子的结构示意图:
②用电子式表示Z的氢化物的形成过程:
③Y的金属性与Mg的金属性相比,
④写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学方程式:
⑤工业上经常用W的氧化物制取W单质的粗产品,化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(1)写出Be与NaOH溶液反应生成Na2BeO2和一种气体的离子方程式:______________________________________ 。
(2)Be(OH)2与Mg(OH)2可用__________ 试剂鉴别,其离子方程式为:______________________________ 。
(3)Li与Mg根据对角线规则,性质也相似,Li2CO3受热也易分解,请写出分解产物中金属氧化物的电子式_____________ ,它属于____________ 晶体。
(1)写出Be与NaOH溶液反应生成Na2BeO2和一种气体的离子方程式:
(2)Be(OH)2与Mg(OH)2可用
(3)Li与Mg根据对角线规则,性质也相似,Li2CO3受热也易分解,请写出分解产物中金属氧化物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
(1)请画出上述元素h的原子结构示意图_______ ;元素h位于元素周期表的第_____ 区。
(2)e、g两种元素的气态氢化物中更稳定的是_______ (写化学式);
(3)b2a2分子的电子式是________ ,该分子中存在的σ键与π键的个数比为_______ 。
(4)c、d两种元素中第一电离能较大的是_________ (写元素符号)。
(5)f和g两种元素形成的化合物是______ (填“离子化合物”“共价化合物”)。a2d分子是_________ 分子(填极性分子或者非极性分子)。
| a | |||||||||||||||||
| b | c | d | e | ||||||||||||||
| f | g | ||||||||||||||||
| h | |||||||||||||||||
(1)请画出上述元素h的原子结构示意图
(2)e、g两种元素的气态氢化物中更稳定的是
(3)b2a2分子的电子式是
(4)c、d两种元素中第一电离能较大的是
(5)f和g两种元素形成的化合物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是元素周期表的一部分,表中所列字母分别代表一种元素.
试回答下列问题:
(1)以上元素中,属于d区元素的是________ (填元素符号),h在周期表的位置是_________ 。
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为______________ 。
(3)元素k的基态原子电子排布式为__________ ;画出c的核外电子排布图:_____________ 。
(4)元素c的电负性______ 元素g的电负性(填“>”、“=”、“<”),元素b、c、e的第一电离能由大到小的顺序是___________________ (用元素符号表示)。
(5)工业上冶炼g元素的单质的化学方程式_______________________________ ,f、 h两种元素最高价氧化物对应的水化物反应的化学方程式是___________________ 。
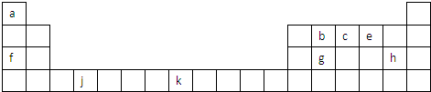
试回答下列问题:
(1)以上元素中,属于d区元素的是
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为
(3)元素k的基态原子电子排布式为
(4)元素c的电负性
(5)工业上冶炼g元素的单质的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:
(1)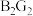 的电子式为
的电子式为___________ 。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为___________ (填化学式)。
(5)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:___________ 。
| A | |||||||||||||||||
| G | I | ||||||||||||||||
| B | E | F | H | ||||||||||||||
| C | D | J |
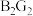 的电子式为
的电子式为(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为
(5)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:

(1)在这10种元素中,非金属性最强的是______ (填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为__________ ,元素②与⑨形成的18e﹣化合物的电子式______ ;
(3)比较元素⑦⑧形成的气态氢化物的稳定性:__ >__ (用化学式表示);
(4)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式_____ ;
(5)元素④和③形成的化合物属于______ 化合物,用电子式表示其形成过程____ 。

(1)在这10种元素中,非金属性最强的是
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为
(3)比较元素⑦⑧形成的气态氢化物的稳定性:
(4)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式
(5)元素④和③形成的化合物属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“阅读”、“质疑”、“解惑”是重要的学习方法,请回答下列问题:
(1)在元素周期表中氯元素与溴元素被置于同一主族,从原子结构分析,原因是___ ;氯元素与硫元素被置于同一周期,从原子结构分析,原因是___ 。
(2)甲同学将氯气通入硫化钠(Na2S)的溶液中,观察到产生淡黄色沉淀,反应的化学反应方程式为___ ,得出的结论是Cl-的还原性___ S2-(填“强于”或“弱于”)。
(3)甲同学通过“FeCl3和FeBr3溶液存在”这一事实推测“FeI3”溶液存在,但查阅资料后发现FeI3溶液不存在,可能的原因是___ 。
(4)甲同学将氟气通入氯化钠溶液并未出现“溶液颜色明显变化”的预测现象,可能的原因是___ 。
(1)在元素周期表中氯元素与溴元素被置于同一主族,从原子结构分析,原因是
(2)甲同学将氯气通入硫化钠(Na2S)的溶液中,观察到产生淡黄色沉淀,反应的化学反应方程式为
(3)甲同学通过“FeCl3和FeBr3溶液存在”这一事实推测“FeI3”溶液存在,但查阅资料后发现FeI3溶液不存在,可能的原因是
(4)甲同学将氟气通入氯化钠溶液并未出现“溶液颜色明显变化”的预测现象,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是___________ 、___________ 。
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用___________ 鉴别,其离子方程式是___________ 。
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为___________ 。
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是元素周期表的一部分。
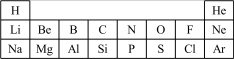
请回答下列问题。
(1)非金属性最强的元素名称 为__________ ,它位于元素周期表中的位置是__________________________ 。
(2)用化学方程式说明碳比硅的非金属性强______________________________________ 。
(3)PH3属于_____________ (填“离子”或“共价”)化合物。PH3的还原性_________ (填“>”或“<”)NH3的还原性。
(4)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的离子 方程式_______________________ 。
(5)硼酸(H3BO3)的酸性_________ (填“>” 或“<”)碳酸(H2CO3)的酸性,简要说明判断依据____ 。

请回答下列问题。
(1)非金属性最强的元素
(2)用化学方程式说明碳比硅的非金属性强
(3)PH3属于
(4)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的
(5)硼酸(H3BO3)的酸性
您最近一年使用:0次



