回答下列问题:
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是___________ 、___________ 。
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用___________ 鉴别,其离子方程式是___________ 。
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为___________ 。
(1)无机化合物甲、乙分别由三种元素组成。组成甲、乙化合物的元素原子的特征排布都可表示如下:asa、bsbbpb、csccp2c甲是一种溶解度较小的盐类化合物。由此可知甲、乙的化学式分别是
(2)根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化。氢氧化铍与氢氧化镁可用
(3)已知砷(As)元素原子的最外层电子排布是 4s24p3,砷酸钠在酸性条件下能把碘化钾氧化为单质碘,同时生成亚砷酸钠(Na3AsO3)和水,该反应的离子方程式为
更新时间:2022-10-29 21:11:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】VIA 元素的各种性质可归纳整理如下:
回答下列问题:
(1)碲(Te)的氧化物分子式是____________________ 。
(2)硒酸与碲酸酸性较强的是____________________ (填化学式)。
(3)比较键能:H—S_____ H—Se(填“>”或“<”)。
(4)氢硒酸放在空气中,可能发生反应的化学方程式为______________________________ 。
(5)下图所示为 VIA 族元素单质与 H2反应过程中体系温度变化示意图,其中 a、b、c 分别表示VIA 族中某一元素的单质,下图为相同物质的量的单质与 H2反应过程中的体系温度变化。
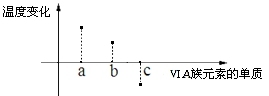
则:c 代表__________ 。(均写单质名称)
| 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点/°C | -218.4 | 113 | 271 | 450 |
| 单质沸点/°C | -183 | 444.6 | 685 | 1390 |
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
回答下列问题:
(1)碲(Te)的氧化物分子式是
(2)硒酸与碲酸酸性较强的是
(3)比较键能:H—S
(4)氢硒酸放在空气中,可能发生反应的化学方程式为
(5)下图所示为 VIA 族元素单质与 H2反应过程中体系温度变化示意图,其中 a、b、c 分别表示VIA 族中某一元素的单质,下图为相同物质的量的单质与 H2反应过程中的体系温度变化。

则:c 代表
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)卤素氢化物中最不稳定的是___________ (写化学式,放射性元素除外,下同)。碱金属中最高价氧化物对应水化物碱性最强的是___________ ,
(2)下列两个元素族,单质熔、沸点随原子序数递增而升高的是___________ (填序号)。
A.碱金属 B.卤素
(3)下列反应中,更剧烈的是___________ (填序号)。
A.钠与水反应 B.钾与水反应
(4)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、静置后,四氯化碳层显紫红色的是___________ (填序号)。
A.溴化钠溶液 B.碘化钾溶液
(2)下列两个元素族,单质熔、沸点随原子序数递增而升高的是
A.碱金属 B.卤素
(3)下列反应中,更剧烈的是
A.钠与水反应 B.钾与水反应
(4)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、静置后,四氯化碳层显紫红色的是
A.溴化钠溶液 B.碘化钾溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求完成下列问题
(1)镁原子的结构示意图_________________ 。
(2)氧化钠的电子式__________________ 。
(3)Si元素元素周期表中的位置在__________________________ 。
(4)在原子序数1~20号的元素中,最高价氧化物对应的水化物中碱性最强的是_____ (用化学式表示)
(5)元素周期表中最高价氧化物对应水化物酸性最强的是________________ (用化学式表示)
(6)短周期元素中,族序数为次外层电子数2倍的元素是_________________ 。(用元素符号表示)。
(1)镁原子的结构示意图
(2)氧化钠的电子式
(3)Si元素元素周期表中的位置在
(4)在原子序数1~20号的元素中,最高价氧化物对应的水化物中碱性最强的是
(5)元素周期表中最高价氧化物对应水化物酸性最强的是
(6)短周期元素中,族序数为次外层电子数2倍的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
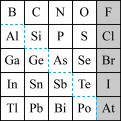
(1)元素Ga的原子结构示意图___________ ,镓(Ga)的氯化物与氨水反应的化学方程式为___________ ,
(2)Ge 的最高价氧化物对应水化物的化学式为___________ ,Bi的最高价氧化物为___________ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是___________ 元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___________ (填“>”“<”或“=”)H2SeO4。
③金属性比较:Tl___________ (填“>”“<”或“=”)Sn。
④氢化物的还原性:H2S___________ (填“>”“<”或“=”)H2O。
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___________ 。

(1)元素Ga的原子结构示意图
(2)Ge 的最高价氧化物对应水化物的化学式为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③金属性比较:Tl
④氢化物的还原性:H2S
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是元素周期表的一部分。
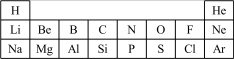
请回答下列问题。
(1)非金属性最强的元素名称 为__________ ,它位于元素周期表中的位置是__________________________ 。
(2)用化学方程式说明碳比硅的非金属性强______________________________________ 。
(3)PH3属于_____________ (填“离子”或“共价”)化合物。PH3的还原性_________ (填“>”或“<”)NH3的还原性。
(4)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的离子 方程式_______________________ 。
(5)硼酸(H3BO3)的酸性_________ (填“>” 或“<”)碳酸(H2CO3)的酸性,简要说明判断依据____ 。

请回答下列问题。
(1)非金属性最强的元素
(2)用化学方程式说明碳比硅的非金属性强
(3)PH3属于
(4)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的
(5)硼酸(H3BO3)的酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】摩擦剂是牙膏的主体成分, 是一种常见的摩擦剂.
是一种常见的摩擦剂.
(1) 在元素周期表中的位置是
在元素周期表中的位置是_____________ .
(2)根据用途推测 在水中的溶解性:
在水中的溶解性:_____________ (填“易溶”或“难溶”).
(3)制备 的方法如下:
的方法如下:

①写出反应Ⅰ的离子方程式________________________ .
②比较酸性强弱:
_____________  (填“>”或“<”).
(填“>”或“<”).
③结合原子结构解释②中酸性关系: 和S电子层数相同,
和S电子层数相同,__________________________ .
(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡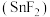 .
.
已知锡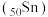 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是_____________ (填序号).
a. 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大
c. 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸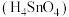 的酸性强于硅酸
的酸性强于硅酸
(5)工业上可以用木炭还原 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:_____________ ;该反应能否验证 和C的非金属性强弱?
和C的非金属性强弱?_____________ (填“能”、“不能”)
(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?_____________ (填“同意”、“不同意”);
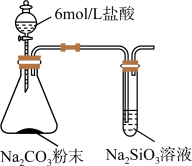
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案._____________
 是一种常见的摩擦剂.
是一种常见的摩擦剂.(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)根据用途推测
 在水中的溶解性:
在水中的溶解性:(3)制备
 的方法如下:
的方法如下:
①写出反应Ⅰ的离子方程式
②比较酸性强弱:

 (填“>”或“<”).
(填“>”或“<”).③结合原子结构解释②中酸性关系:
 和S电子层数相同,
和S电子层数相同,(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡
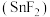 .
.已知锡
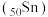 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是a.
 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大c.
 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸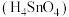 的酸性强于硅酸
的酸性强于硅酸(5)工业上可以用木炭还原
 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为: 和C的非金属性强弱?
和C的非金属性强弱?(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与
 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氢氟酸可用于半导体工业,也常用来蚀刻玻璃,其刻蚀反应原理如下:6HF + Na2SiO3 =2NaF + SiF4↑+ 3H2O完成下列填空:
(1)根据HF的________ (选填编号)大于H2O,可推断氟元素的非金属性强于氧元素。
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(2)SiF4与甲烷结构相似,SiF4是含___ 键的_____ 分子(均选填“极性”或“非极性”)。刻蚀反应中的三种元素可组成同时含离子键和共价键的化合物,该化合物的电子式为__________ 。
(3)Si原子核外电子有_____ 种不同能量的电子,其中最高能量的电子处于______ 轨道。
(4)在相同条件下,Na2SiO3、CaSiO3分别与等浓度等体积的氢氟酸反应,两个反应原理相似,但前者的反应速率明显大于后者。原因是__________________________ 。
(5)同浓度的H2SO3和HF两溶液的pH为:H2SO3_____ HF(选填“>”或“<”)。浓度均为0.01 mol/L 的H2SO3和HF的1L混合溶液中,通入0.02 mol NH3充分反应后,SO32-、HSO3-、F-、NH4+浓度从大到小的顺序为:____________________ 。
已知:H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7 HF Ki=6.8×10-4 NH3·H2O Ki=1.8×10-5
(1)根据HF的
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(2)SiF4与甲烷结构相似,SiF4是含
(3)Si原子核外电子有
(4)在相同条件下,Na2SiO3、CaSiO3分别与等浓度等体积的氢氟酸反应,两个反应原理相似,但前者的反应速率明显大于后者。原因是
(5)同浓度的H2SO3和HF两溶液的pH为:H2SO3
已知:H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7 HF Ki=6.8×10-4 NH3·H2O Ki=1.8×10-5
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】若某元素原子核外有4个电子层,最外层有2个电子。请写出满足上述条件的该元素的元素符号_____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题。
Ⅰ.用“>”或“<”填空:
(1)键长:N-N___________ N=N
(2)键能:2E(C-C)___________ E(C=C)
(3)键角:CO2___________ SO2;
(4)键的极性:C-H___________ N-H。
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO 中的N
中的N___________ 杂化,空间构型___________ ;
(2)BCl3中的B___________ 杂化,空间构型___________ ;
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含___________ 种元素,___ 种核素,___________ 种相对分子质量。
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是___________ 电子,原子轨道呈现___________ 形,它的氢化物的电子式是___________
Ⅰ.用“>”或“<”填空:
(1)键长:N-N
(2)键能:2E(C-C)
(3)键角:CO2
(4)键的极性:C-H
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO
 中的N
中的N(2)BCl3中的B
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是
您最近一年使用:0次



