回答下列问题。
Ⅰ.用“>”或“<”填空:
(1)键长:N-N___________ N=N
(2)键能:2E(C-C)___________ E(C=C)
(3)键角:CO2___________ SO2;
(4)键的极性:C-H___________ N-H。
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO 中的N
中的N___________ 杂化,空间构型___________ ;
(2)BCl3中的B___________ 杂化,空间构型___________ ;
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含___________ 种元素,___ 种核素,___________ 种相对分子质量。
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是___________ 电子,原子轨道呈现___________ 形,它的氢化物的电子式是___________
Ⅰ.用“>”或“<”填空:
(1)键长:N-N
(2)键能:2E(C-C)
(3)键角:CO2
(4)键的极性:C-H
Ⅱ.指出下列原子的杂化轨道类型及分子的空间构型。
(1)NO
 中的N
中的N(2)BCl3中的B
Ⅲ.已知有1H216O 3H218O S17O2 2H2S S16O2,其中包含
Ⅳ.元素X的原子最外层电子排布式为nsnnpn+1.试解答下列各题:
原子中能量最高的是
更新时间:2021-05-08 21:37:39
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1) A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。C和D反应可生成组成比为1∶3 的化合物E,E的立体构型为____ ,中心原子的杂化轨道类型为____ 。化合物D2A的立体构型为____ ,中心原子的价层电子对数为 ____ 。
(2)X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族元素;Z和U位于第ⅦA族;X和Z可形成化合物XZ4;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质在空气中能够自燃。利用价层电子对互斥理论判断TU3的立体构型是___ 。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为___ ,其中氧原子的杂化方式为___ 。
(2)X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族元素;Z和U位于第ⅦA族;X和Z可形成化合物XZ4;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质在空气中能够自燃。利用价层电子对互斥理论判断TU3的立体构型是
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】黑火药是中国古代四大发明之一,它的爆炸反应为:
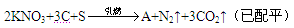
(1)生成物中除了氮气与二氧化碳外,还有一种物质A生成,则A的电子式为____________ ,A属于________ 晶体。
(2)黑火药中位于元素周期表短周期的元素有_________ 种。其中一种元素的单质可用于制药,其氧化物可用于漂白织物和防腐剂,该元素在周期表中的位置是___________________ ,该元素的原子核外有______ 种不同运动状态的电子。
(3)黑火药中所含元素的原子半径从大到小的顺序是________________ (用元素符号表示);
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有___________ 。
A.同条件同浓度溶液pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.分解温度:CH4>H2S
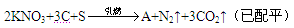
(1)生成物中除了氮气与二氧化碳外,还有一种物质A生成,则A的电子式为
(2)黑火药中位于元素周期表短周期的元素有
(3)黑火药中所含元素的原子半径从大到小的顺序是
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有
A.同条件同浓度溶液pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.分解温度:CH4>H2S
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在1400~1450℃的氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:
Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:
(1)上述反应所涉及的元素,原子半径由大到小的顺序是______ 。其中一种元素的原子核外s电子数与p电子数相等,写出它的最外层电子排布的轨道表示式______ 。比较碳、硅两种元素的非金属性强弱,可以通过比较______ (填:化合物性质的差异)来判断
(2)上述反应混合物中的极性分子是______ ,写出非极性分子的电子式______ 。从晶体类型的角度分析用氮化硅制造发动机中耐热部件的原因是______
(3)下列措施可以提高二氧化硅转化率的是______ (选填编号)
a.增加二氧化硅用量b.升高反应温度
c.增大气体压强 d.向反应容器中多充入氮气
(4)下列描述中能说明反应已达平衡的是______ (选填编号)
a.c(CO)=3c(N2)
b.v (CO)=3v(N2)
c.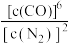 保持不变
保持不变
d.气体的压强保持不变
(5)测得平衡时固体质量减少了11.2g,则用氮气表示的平均反应速率为______
 Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:
Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:(1)上述反应所涉及的元素,原子半径由大到小的顺序是
(2)上述反应混合物中的极性分子是
(3)下列措施可以提高二氧化硅转化率的是
a.增加二氧化硅用量b.升高反应温度
c.增大气体压强 d.向反应容器中多充入氮气
(4)下列描述中能说明反应已达平衡的是
a.c(CO)=3c(N2)
b.v (CO)=3v(N2)
c.
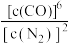 保持不变
保持不变d.气体的压强保持不变
(5)测得平衡时固体质量减少了11.2g,则用氮气表示的平均反应速率为
您最近一年使用:0次
【推荐1】在水溶液中:YO3n-+3S2-+6H+=Y-+3S +3H2O
(1)YO3n-中Y元素的化合价是:_______
(2)Y元素原子的最外层电子数是:_____
(3)比较S2-和Y-的还原性:____
(1)YO3n-中Y元素的化合价是:
(2)Y元素原子的最外层电子数是:
(3)比较S2-和Y-的还原性:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:2NaOCN+3NaClO→Na2CO3+CO2↑+3NaCl+N2↑
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外价电子数是______ 个;
O2—、Na+、Cl—中半径最小的是_____________ 。
(2)NaCN晶体中含有的化学键类型为_____________________________ 。
(3)第二段过程中,产物属于双原子分子的结构式是___________ ,该物质一般要比其他共价化合物如:NH3、H2S等都要稳定,其原因为:___________________ ;写出该物质的一种用途:____________________ 。
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:2NaOCN+3NaClO→Na2CO3+CO2↑+3NaCl+N2↑
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外价电子数是
O2—、Na+、Cl—中半径最小的是
(2)NaCN晶体中含有的化学键类型为
(3)第二段过程中,产物属于双原子分子的结构式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)S单质的常见形式为 ,其环状结构如图所示,S原子采用的轨道杂化方式是
,其环状结构如图所示,S原子采用的轨道杂化方式是_______ 。
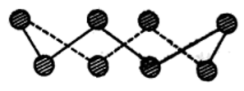
(2)现有H、N、O、S、Cu几种元素,回答下列问题。
①氢元素和N、O、S、Cu形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_______ ;分子中既含有极性共价键又含有非极性共价键的化合物是_______ (填化学式,写出两种)。
②这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_______ (填化学式,下同);酸根呈三角锥形的酸是_______ 。
 ,其环状结构如图所示,S原子采用的轨道杂化方式是
,其环状结构如图所示,S原子采用的轨道杂化方式是
(2)现有H、N、O、S、Cu几种元素,回答下列问题。
①氢元素和N、O、S、Cu形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为
②这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氨硼烷 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。 分子中,
分子中, 化学键称为
化学键称为_______ 键,其电子对由_______ 提供。氨硼烷在催化剂作用下水解释放氢气: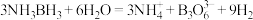 。
。 的结构为
的结构为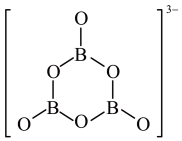 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。 分子中,
分子中, 化学键称为
化学键称为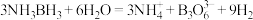 。
。 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由
您最近一年使用:0次





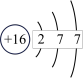
 的空间构型为
的空间构型为