黑火药是中国古代四大发明之一,它的爆炸反应为:
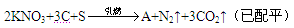
(1)生成物中除了氮气与二氧化碳外,还有一种物质A生成,则A的电子式为____________ ,A属于________ 晶体。
(2)黑火药中位于元素周期表短周期的元素有_________ 种。其中一种元素的单质可用于制药,其氧化物可用于漂白织物和防腐剂,该元素在周期表中的位置是___________________ ,该元素的原子核外有______ 种不同运动状态的电子。
(3)黑火药中所含元素的原子半径从大到小的顺序是________________ (用元素符号表示);
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有___________ 。
A.同条件同浓度溶液pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.分解温度:CH4>H2S
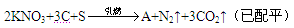
(1)生成物中除了氮气与二氧化碳外,还有一种物质A生成,则A的电子式为
(2)黑火药中位于元素周期表短周期的元素有
(3)黑火药中所含元素的原子半径从大到小的顺序是
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有
A.同条件同浓度溶液pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
D.分解温度:CH4>H2S
12-13高三上·上海闵行·期末 查看更多[2]
更新时间:2012-01-09 17:18:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe2+的核外电子排布式为_________________ 。
(2)NH3是一种很好的配体,NH3的沸点______ (填“高于”“等于”或“低于”)AsH3。
(3)科学家通过X射线测得胆矾结构示意图可简单表示如下,图中虚线表示的作用力为________________ 。

(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于________ (填标号)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)As 的卤化物的熔点如下:
表中卤化物熔点差异的原因是________________ 。
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是_________ ,Fe3+的配位数为_________ 。

(1)Fe2+的核外电子排布式为
(2)NH3是一种很好的配体,NH3的沸点
(3)科学家通过X射线测得胆矾结构示意图可简单表示如下,图中虚线表示的作用力为

(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)As 的卤化物的熔点如下:
| AsCl3 | AsBr3 | AsI3 | |
| 熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是

您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐2】Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si S | O2- Na+ | NaCl Si | H2SO4 HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_______ 。

(2)Se原子序数为_______ ,其核外M层电子的排布式为_______ 。
(3)O、S、Se原子的第一电离能由大到小的顺序为_______ 。
(4)比较酸性:H2SeO4_______ H2SeO3(填“>”、“<”或“=”),理由是:_______ 。
(5)气态SeO3分子的立体构型为_______ ,  离子的VSEPR模型为
离子的VSEPR模型为_______ 。
(6)H2Se、H2S、H2O的稳定性由强到弱的顺序是_______ ,原因是_______ (用共价键理论解释)。H2Se、H2S、H2O的沸点由高到低的顺序是_______ ,原因是_______ 。
(7)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是_______ 。
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(2)Se原子序数为
(3)O、S、Se原子的第一电离能由大到小的顺序为
(4)比较酸性:H2SeO4
(5)气态SeO3分子的立体构型为
 离子的VSEPR模型为
离子的VSEPR模型为(6)H2Se、H2S、H2O的稳定性由强到弱的顺序是
(7)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)化学与生活、生产息息相关。
① 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;
③ 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;
⑤CO可用于冶炼金属; ⑥ 可用于制硫酸;
可用于制硫酸;
⑦ 可用于制硝酸
可用于制硝酸
上述物质中,属于酸性氧化物的是______________________ (填序号)。
(2)硝酸是用途广泛的重要化工原料。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为___________ 。
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是___________ (填序号)。
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。 的沸点
的沸点___________  的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。
(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
(6)实验室中 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式_________________________ 。
(7)氰气[ ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素___________ (写元素符号)显负价。
(1)化学与生活、生产息息相关。
①
 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;③
 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;⑤CO可用于冶炼金属; ⑥
 可用于制硫酸;
可用于制硫酸;⑦
 可用于制硝酸
可用于制硝酸上述物质中,属于酸性氧化物的是
(2)硝酸是用途广泛的重要化工原料。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。
 的沸点
的沸点 的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
| A.“类钫”单质具有强氧化性 | B.“类钫”单质能与冷水剧烈反应 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 | D.“类钫”在化合物中显+1价 |
(6)实验室中
 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式(7)氰气[
 ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,请回答:
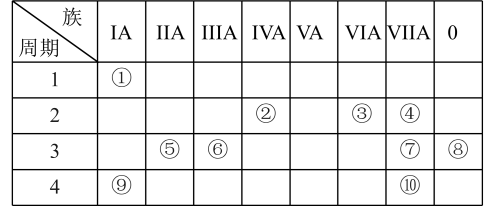
(1)元素⑦的原子结构示意图为___________ ;元素⑩的名称为___________ 。
(2)在这些元素中,化学性质最活泼的金属元素是___________ (填元素符号,下同),最不活泼的元素是___________ ;原子半径最小的元素是___________ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同);具有两性的是___________ 。

(1)元素⑦的原子结构示意图为
(2)在这些元素中,化学性质最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 ________ ;
(2)表中能形成两性氢氧化物的元素是________ (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式:_________ ;
(3)③⑦⑩三种元素的阴离子还原性顺序为:___________________ ;⑦的水溶液呈__________ 色;
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是_______ (填化学式) ;
(5)③元素与⑩元素两者核电荷数之差是____________ ;
(6)设计实验方案:比较⑦与⑥单质氧化性的强弱,请将方案填入下表。
| 周期 主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)表中能形成两性氢氧化物的元素是
(3)③⑦⑩三种元素的阴离子还原性顺序为:
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是
(5)③元素与⑩元素两者核电荷数之差是
(6)设计实验方案:比较⑦与⑥单质氧化性的强弱,请将方案填入下表。
| 实验步骤 | 实验现象与结论 |
| |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,回答下列问题:
(1)写出下列元素符号:①________ ⑥_______ ⑦______
(2)在这些元素中,最活泼的金属元素是________ ,最活泼的非金属元素是_______ 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ ,碱性最强的是_____ ,呈两性的是________ 。
(4)在这些元素中,原子半径最大的是________ 。
族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| ⒉ | ① | ② | ||||||
| ⒊ | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| ⒋ | ⑩ | ⑾ |
(1)写出下列元素符号:①
(2)在这些元素中,最活泼的金属元素是
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)在这些元素中,原子半径最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F均为短周期主族元素,且原子序数依次增大。短周期元素中C的原子半径最大,B、E同族,E的最外层电子数是电子层数的2倍,A的最高价氧化物水化物为H2AO3,D是地壳中含量最高的金属元素。
(1)A的元素符号是_______ ,C2B2的电子式为_______ 。
(2)B、C、D、F的离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)E和F相比,非金属性强的是_______ (用元素符号表示),下列事实能证明这一结论的是_______ (用符号填空)。
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为_______ (填化学式)。
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为_________________________ 。
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为_______ , pH=10的乙溶液中由水电离产生的c(OH-)=_______ mol·L-1。
(1)A的元素符号是
(2)B、C、D、F的离子半径由大到小的顺序是
(3)E和F相比,非金属性强的是
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.自然界的硫循环对动植物和人类的生存意义重大。
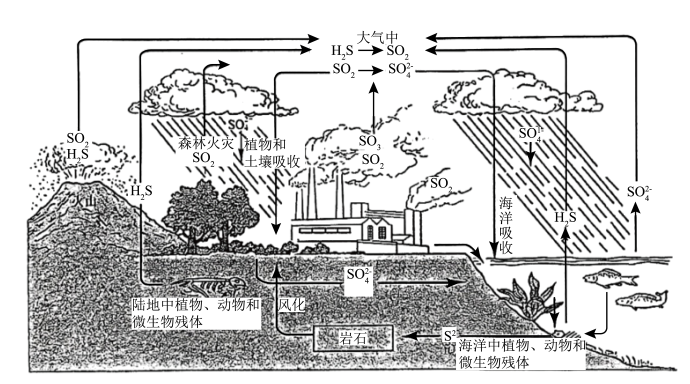
(1)生物体内多种蛋白质含有硫元素,硫与同主族的氧元素相比,非金属性S_____ O(选填“>”、“<”或“=”),写出两种能够比较说明O和S非金属性强弱的化学事实或化学反应方程式_______ 、_____ 。
(2)已知 与硫元素属于同一主族,原子序数比硫大18,写出
与硫元素属于同一主族,原子序数比硫大18,写出 在元素周期表的位置
在元素周期表的位置_______ ,写出 原子的原子结构示意图
原子的原子结构示意图_______ 。
(3)O、S和 都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。
都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。
(4)硫元素在第三周期,第三周期元素的原子所形成的简单离子中:还原性最弱的阴离子是_______ ;对第三周期简单阳离子的离子半径由大到小进行排列_______ 。
II.活火山的火山口往往有硫磺矿物富集,是人类获得硫磺的主要来源之一,人们利用硫磺可以制备例如浓硫酸等许多有用的含硫化合物。
(5)下列不能由硫单质和其他单质化合生成的物质是_______。
(6)硫磺和过氧化钠都是淡黄色固体,如何鉴别某固体物质为硫磺或过氧化钠:____ 。硫单质有多种结构,例如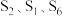 和
和 等,它们互称
等,它们互称_______ ,已知 中S原子最外层满足8电子稳定结构,且
中S原子最外层满足8电子稳定结构,且 结构中仅有硫硫单键,计算
结构中仅有硫硫单键,计算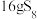 固体中共价键的数目为
固体中共价键的数目为_______ 。
III.火山喷发产生的气体中含有 ,经过一系列化学反应最终能转变为硫磺。
,经过一系列化学反应最终能转变为硫磺。
(7)写出 的结构式
的结构式_______ , 是一种具有强还原性的二元弱酸,写出
是一种具有强还原性的二元弱酸,写出 在水溶液中的电离方程式
在水溶液中的电离方程式_______ 、_______ 。
(8) 从火山口喷出后在空气中转变化
从火山口喷出后在空气中转变化 ,写出有关化学反应方程式
,写出有关化学反应方程式__ ,之后生成的 与剩余
与剩余 继续反应形成硫磺,
继续反应形成硫磺, 与
与 反应产物中氧化产物与还原产物的比例为
反应产物中氧化产物与还原产物的比例为_______ 。
IV. 是海洋中硫元素的主要存在形式之一。
是海洋中硫元素的主要存在形式之一。
(9)海水中硫酸根离子含量大约为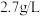 ,会干扰海水中
,会干扰海水中 的检验,写出检验海水中
的检验,写出检验海水中 的实验方法
的实验方法_______ 。
(10)粗盐提纯时,除去粗盐中的硫酸根离子,经常向溶液中加入_______ (填写试剂化学式)。该物质的固体熔点_______ (填写“大于”或“小于”) 的熔点。
的熔点。
V.人们合成的许多硫的化合物具有奇妙的性质
(11)人类合成了一系列的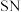 二元化合物,其中线性的
二元化合物,其中线性的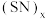 是具有类似黄铜的金属光泽和导电性,其结构片段为:
是具有类似黄铜的金属光泽和导电性,其结构片段为: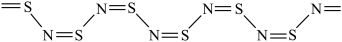 ,以下说法正确的是_______。
,以下说法正确的是_______。
(12) 与酸反应时生成
与酸反应时生成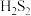 ,
,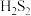 与
与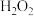 相似,易分解。实验室用过量稀硫酸与
相似,易分解。实验室用过量稀硫酸与 颗粒混合,不可能生成的物质是_______。
颗粒混合,不可能生成的物质是_______。
(13) 在酸性环境中的氧化性比
在酸性环境中的氧化性比 还要强,实验室可以用无色的酸性
还要强,实验室可以用无色的酸性 溶液来检验
溶液来检验 (溶液几乎无色),原理如下所示:
(溶液几乎无色),原理如下所示:
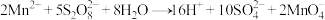
 的结构如图所示:
的结构如图所示:
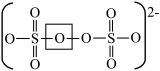
①已知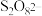 中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态
中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态_______ ,并标明上述反应的电子转移方向与数目_______ 。
②确认溶液中是否含 的现象是:
的现象是:_______ 。

(1)生物体内多种蛋白质含有硫元素,硫与同主族的氧元素相比,非金属性S
(2)已知
 与硫元素属于同一主族,原子序数比硫大18,写出
与硫元素属于同一主族,原子序数比硫大18,写出 在元素周期表的位置
在元素周期表的位置 原子的原子结构示意图
原子的原子结构示意图(3)O、S和
 都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。
都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。A.O的原子半径>S的原子半径 的原子半径 的原子半径 | B.最外层电子数都相同 |
| C.核外电子层数都相同 | D.最外层电子数都不相同 |
II.活火山的火山口往往有硫磺矿物富集,是人类获得硫磺的主要来源之一,人们利用硫磺可以制备例如浓硫酸等许多有用的含硫化合物。
(5)下列不能由硫单质和其他单质化合生成的物质是_______。
A. | B. | C. | D. |
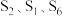 和
和 等,它们互称
等,它们互称 中S原子最外层满足8电子稳定结构,且
中S原子最外层满足8电子稳定结构,且 结构中仅有硫硫单键,计算
结构中仅有硫硫单键,计算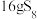 固体中共价键的数目为
固体中共价键的数目为III.火山喷发产生的气体中含有
 ,经过一系列化学反应最终能转变为硫磺。
,经过一系列化学反应最终能转变为硫磺。(7)写出
 的结构式
的结构式 是一种具有强还原性的二元弱酸,写出
是一种具有强还原性的二元弱酸,写出 在水溶液中的电离方程式
在水溶液中的电离方程式(8)
 从火山口喷出后在空气中转变化
从火山口喷出后在空气中转变化 ,写出有关化学反应方程式
,写出有关化学反应方程式 与剩余
与剩余 继续反应形成硫磺,
继续反应形成硫磺, 与
与 反应产物中氧化产物与还原产物的比例为
反应产物中氧化产物与还原产物的比例为IV.
 是海洋中硫元素的主要存在形式之一。
是海洋中硫元素的主要存在形式之一。(9)海水中硫酸根离子含量大约为
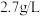 ,会干扰海水中
,会干扰海水中 的检验,写出检验海水中
的检验,写出检验海水中 的实验方法
的实验方法(10)粗盐提纯时,除去粗盐中的硫酸根离子,经常向溶液中加入
 的熔点。
的熔点。V.人们合成的许多硫的化合物具有奇妙的性质
(11)人类合成了一系列的
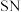 二元化合物,其中线性的
二元化合物,其中线性的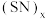 是具有类似黄铜的金属光泽和导电性,其结构片段为:
是具有类似黄铜的金属光泽和导电性,其结构片段为: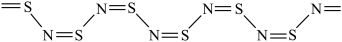 ,以下说法正确的是_______。
,以下说法正确的是_______。| A.是共价化合物 | B.酸性: ,所以非金属性 ,所以非金属性 |
| C.为离子化合物 | D.所有原子最外层都是8电子 |
 与酸反应时生成
与酸反应时生成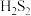 ,
,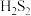 与
与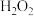 相似,易分解。实验室用过量稀硫酸与
相似,易分解。实验室用过量稀硫酸与 颗粒混合,不可能生成的物质是_______。
颗粒混合,不可能生成的物质是_______。A. | B.S | C. | D. |
 在酸性环境中的氧化性比
在酸性环境中的氧化性比 还要强,实验室可以用无色的酸性
还要强,实验室可以用无色的酸性 溶液来检验
溶液来检验 (溶液几乎无色),原理如下所示:
(溶液几乎无色),原理如下所示: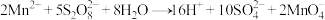
 的结构如图所示:
的结构如图所示:
①已知
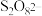 中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态
中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态②确认溶液中是否含
 的现象是:
的现象是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】大型客机燃油用四乙基铅[Pb(CH2CH3)4])做抗震添加剂,但皮肤长期接触四乙基铅对身体健康有害,可用硫基乙胺(HSCH2CH2NH2)和KMnO4清除四乙基铅。
(1)碳原子核外电子的空间运动状态有______ 种,基态锰原子的外围电子排布式为___ ,该原子能量最高的电子的电子云轮廓图形状为________ 。
(2)N、C和Mn电负性由大到小的顺序为____________ 。
(3)HSCH2CH2NH2中C的杂化方式为_____ ,其中NH2-空间构型为____ ;N和P的价电子相同,但磷酸的组成为H3PO4,而硝酸的组成不是H3NO4,其原因是_______ 。
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于_____ 晶体。已知Pb(CH2CH3)4晶体的堆积方式如下。
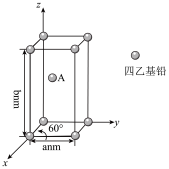
Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是___ ,A分子的坐标参数为_____ ;设阿伏加 德罗常数为NA/mol,Pb(CH2CH3)4]的摩尔质量为Mg/mol,则Pb(CH2CH3)4]晶体的密度是_____ g/cm3 (列出计算式即可)。
(1)碳原子核外电子的空间运动状态有
(2)N、C和Mn电负性由大到小的顺序为
(3)HSCH2CH2NH2中C的杂化方式为
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于

Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁元素和碳元素形成的单质及化合物在生产、生活中有广泛的用途,
请回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为_________________ ;其最外层电子的电子云形状为___________ 。
(2)(NH4)2Fe(SO4)2 • 6H2O俗称摩尔盐。其阴离子的VSEPR模型名称为____________________ 。
写出一种与NH4+互为等电子体的分子的电子式:________________________________ 。
(3)Fe(CO)5可用作催化剂、汽油抗暴剂等.其分子中σ键和π键的数目之比为______________ 。CO的沸点高于N2的原因是_________________________ 。
(4)碳元素可形成多种单质。
①石墨烯是从石墨中剥离出来的由单层碳原子构成的平面结构新型碳材料。其中碳原子的杂化方式为______________________ 。
料,其中碳原子的杂化方式为 ,
②金刚石的晶胞如图所示。若晶胞参数为a pm,阿伏伽德罗常数的值为NA,则该晶胞中原子的体积占晶胞体积的百分率为________________ ;1cm3晶体的平均质量为___________ (列出计算式即可)。
请回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为
(2)(NH4)2Fe(SO4)2 • 6H2O俗称摩尔盐。其阴离子的VSEPR模型名称为
写出一种与NH4+互为等电子体的分子的电子式:
(3)Fe(CO)5可用作催化剂、汽油抗暴剂等.其分子中σ键和π键的数目之比为
(4)碳元素可形成多种单质。
①石墨烯是从石墨中剥离出来的由单层碳原子构成的平面结构新型碳材料。其中碳原子的杂化方式为
料,其中碳原子的杂化方式为 ,
②金刚石的晶胞如图所示。若晶胞参数为a pm,阿伏伽德罗常数的值为NA,则该晶胞中原子的体积占晶胞体积的百分率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
(1)B元素在周期表中的位置是____ 区 ,写出A离子的电子排布式_______________
(2)写出C单质与水反应的离子方程式___________________________________
(3)A、B、C、 D四种元素的第一电离能由大到小的顺序______________________
(4)A、B两元素非金属性较强的是(写元素符号)________ 。写出证明这一结论的一个实验事实 _________________________________________________________________
| 元素 | A | B | C | D |
| 性质 结构 信息 | 室温下单质呈粉末状固体,加热易熔化。单质在纯氧中燃烧,发出明亮的蓝紫色火焰。 | 单质常温、常压下是气体,能溶于水。原子的M层有1个未成对的p电子。 | 单质质软、银白色固体、导电性强。单质在空气中燃烧发出黄色的火焰。 | 原子最外电子层上s电子数等于p电子数,等于电子层数。 |
(1)B元素在周期表中的位置是
(2)写出C单质与水反应的离子方程式
(3)A、B、C、 D四种元素的第一电离能由大到小的顺序
(4)A、B两元素非金属性较强的是(写元素符号)
您最近一年使用:0次



