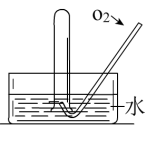
如图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由___________ 逐渐变为___________ 色,试管内的液面会逐渐________ ,当反应停止后向试管中缓慢通入氧气,气体颜色又由_______ 色逐渐变为______ 色,之后又变为_______ 色,试管内的液面会______ ,用化学方程式表示试管中发生的化学反应___________ 。

更新时间:2021-06-06 16:26:53
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】氮氧化物污染的防治
①使用___________ 能源。
②安装汽车尾气净化装置,反应方程式为:___________ 。
①使用
②安装汽车尾气净化装置,反应方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请根据物质在生产、生活中的应用填空:
(1)常温下盛装浓硝酸可使用的容器是_______ (填“铁罐”或“铜罐”)。
(2)酸雨是指pH_______ (填“>”“<”或“=”)5.6的降水。
(3)大型中央空调的制冷剂可用液氨,原因是_______ 。
(4)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是_______ 。
(1)常温下盛装浓硝酸可使用的容器是
(2)酸雨是指pH
(3)大型中央空调的制冷剂可用液氨,原因是
(4)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】I.如图所示:在B水槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B水槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL。
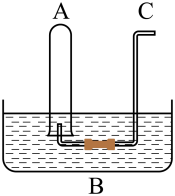
(1)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是___________ 。
(2)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为___________ mol/L(设溶液的体积仍为500 mL,答案用分数表示)。
Ⅱ.向 溶液中通入
溶液中通入 后,将溶液分置于两支试管中。向一份溶液中通入
后,将溶液分置于两支试管中。向一份溶液中通入 ,出现白色沉淀A;另一份通入少量
,出现白色沉淀A;另一份通入少量 ,产生白色沉淀B.试回答下列问题:
,产生白色沉淀B.试回答下列问题:
(3)沉淀A的化学式为___________ ,该沉淀能否溶于稀盐酸?___________ (填“能”或“不能”)。
(4)写出通入少量 ,生成沉淀B的离子方程式:
,生成沉淀B的离子方程式:___________ ,生成2.33 g沉淀B,理论上需要消耗标准状况下的
___________  。
。
(5)若将 溶液换成
溶液换成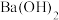 溶液,少量
溶液,少量 通入
通入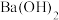 溶液中的离子方程式为
溶液中的离子方程式为___________ 。
Ⅲ.完成下列问题
(6)2.0 g铜镁合金完全溶解于100 mL密度为1.4 g/mL质量分数为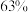 的浓硝酸溶液中,得到NO2和N2O4(NO2和
的浓硝酸溶液中,得到NO2和N2O4(NO2和 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体1792 mL (标况
的混合气体1792 mL (标况 ,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为
,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为___________ ,加入NaOH溶液的体积为___________ mL。
(7)某分子筛类催化剂(H+交换沸石)催化NH3脱除NO、NO2的反应机理如图所示。
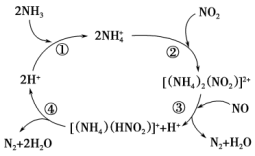
按如图反应机理,NH3脱除NO、NO2总反应的化学方程式是___________ 。
(8)室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不支持燃烧。则a、b、c的等量关系是___________ 。
(9)下列二组混合气体体积比为①NO2∶O2=1∶1;②NH3∶O2=2∶1,将分别盛满上述各种气体的试管倒置于盛有水的水槽中,最后两试管内溶液浓度之比为___________ (忽略溶质扩散)。
(10)将充满NO2和O2混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的 处停止了,则原混合气体中NO2和O2的体积之比是
处停止了,则原混合气体中NO2和O2的体积之比是___________ 。

(1)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是
(2)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为
Ⅱ.向
 溶液中通入
溶液中通入 后,将溶液分置于两支试管中。向一份溶液中通入
后,将溶液分置于两支试管中。向一份溶液中通入 ,出现白色沉淀A;另一份通入少量
,出现白色沉淀A;另一份通入少量 ,产生白色沉淀B.试回答下列问题:
,产生白色沉淀B.试回答下列问题:(3)沉淀A的化学式为
(4)写出通入少量
 ,生成沉淀B的离子方程式:
,生成沉淀B的离子方程式:
 。
。(5)若将
 溶液换成
溶液换成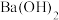 溶液,少量
溶液,少量 通入
通入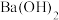 溶液中的离子方程式为
溶液中的离子方程式为Ⅲ.完成下列问题
(6)2.0 g铜镁合金完全溶解于100 mL密度为1.4 g/mL质量分数为
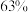 的浓硝酸溶液中,得到NO2和N2O4(NO2和
的浓硝酸溶液中,得到NO2和N2O4(NO2和 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体1792 mL (标况
的混合气体1792 mL (标况 ,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为
,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为(7)某分子筛类催化剂(H+交换沸石)催化NH3脱除NO、NO2的反应机理如图所示。

按如图反应机理,NH3脱除NO、NO2总反应的化学方程式是
(8)室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不支持燃烧。则a、b、c的等量关系是
(9)下列二组混合气体体积比为①NO2∶O2=1∶1;②NH3∶O2=2∶1,将分别盛满上述各种气体的试管倒置于盛有水的水槽中,最后两试管内溶液浓度之比为
(10)将充满NO2和O2混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的
 处停止了,则原混合气体中NO2和O2的体积之比是
处停止了,则原混合气体中NO2和O2的体积之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对含有氮氧化物的废气进行处理。
(1)NH3催化还原氮氧化物技术是目前应用最广泛的烟气氮氧化物脱除技术。其反应原理为NH3+NO2→N2+H2O(未配平)。
①该反应中的还原剂为___ (填化学式)。
②现有NO2与NO气体混合物7.6g,与足量氨气在一定条件下充分反应,消耗氨气的体积为4.48L(已折算为标准状况下的体积)。则混合气体中NO的体积分数为__ 。
③若某工厂排出的废气中NO2含量为0.336%(体积分数),处理1000m3(已折算为标准状况下的体积)这种废气,最少需要的氨气的质量为__ g。
(2)工业上可用NaOH溶液吸收废气中的氮氧化物,反应的化学方程式如下:
Ⅰ.NO2+NO+2NaOH=2NaNO2+H2O;
Ⅱ.2NO2+2NaOH=NaNO2+NaNO3+H2O。
在反应Ⅰ中,氧化剂是__ (填化学式)。在反应Ⅱ中,每生成1molNaNO3,转移电子的物质的量是__ mol。
(3)实验室中用Cu与浓硝酸反应有NO2生成。
①用双线桥法表示出该反应的电子转移方向和数目:___ 。
②12.8gCu与足量该浓硝酸反应能使___ molHNO3被还原。
③浓硝酸在反应中显示出来的性质是__ (填标号)。
a.还原性 b.酸性 c.氧化性 d.挥发性
(1)NH3催化还原氮氧化物技术是目前应用最广泛的烟气氮氧化物脱除技术。其反应原理为NH3+NO2→N2+H2O(未配平)。
①该反应中的还原剂为
②现有NO2与NO气体混合物7.6g,与足量氨气在一定条件下充分反应,消耗氨气的体积为4.48L(已折算为标准状况下的体积)。则混合气体中NO的体积分数为
③若某工厂排出的废气中NO2含量为0.336%(体积分数),处理1000m3(已折算为标准状况下的体积)这种废气,最少需要的氨气的质量为
(2)工业上可用NaOH溶液吸收废气中的氮氧化物,反应的化学方程式如下:
Ⅰ.NO2+NO+2NaOH=2NaNO2+H2O;
Ⅱ.2NO2+2NaOH=NaNO2+NaNO3+H2O。
在反应Ⅰ中,氧化剂是
(3)实验室中用Cu与浓硝酸反应有NO2生成。
①用双线桥法表示出该反应的电子转移方向和数目:
②12.8gCu与足量该浓硝酸反应能使
③浓硝酸在反应中显示出来的性质是
a.还原性 b.酸性 c.氧化性 d.挥发性
您最近一年使用:0次

 4NO+6H2O
4NO+6H2O

