某蓄电池的反应为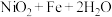

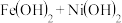
(1)放电时,正极的电极反应式为_______ ,电路中转移电子 时,生成氧化产物
时,生成氧化产物_______ g;充电时,发生氧化反应的物质是_______ ,阳极附近溶液pH_______
(2)为防止远洋轮船的钢铁船体在海水中发生腐蚀,通常在船体上镶嵌Zn块,或与该蓄电池的_______  填“正”或“负”
填“正”或“负” 极相连。
极相连。
(3)以该蓄电池作电源,实验小组同学用如图所示的装置在实验室模拟铝制品表面“钝化” 在表面形成氧化物保护膜
在表面形成氧化物保护膜 。“钝化”时阳极的电极反应为
。“钝化”时阳极的电极反应为_______ ,但有同学在实验过程中发现溶液逐渐变浑浊,并有气泡产生,其原因是_______  用电极反应式表示
用电极反应式表示

(4)精炼铜过程中,电解质溶液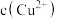 逐渐减小,
逐渐减小,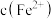 、
、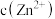 增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:
增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:

已知:
加入 的目的是
的目的是_______ ,加入CuO调节 可除去的离子是
可除去的离子是_______ ,其原因是_______  用平衡移动原理说明
用平衡移动原理说明
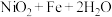

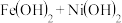
(1)放电时,正极的电极反应式为
 时,生成氧化产物
时,生成氧化产物(2)为防止远洋轮船的钢铁船体在海水中发生腐蚀,通常在船体上镶嵌Zn块,或与该蓄电池的
 填“正”或“负”
填“正”或“负” 极相连。
极相连。(3)以该蓄电池作电源,实验小组同学用如图所示的装置在实验室模拟铝制品表面“钝化”
 在表面形成氧化物保护膜
在表面形成氧化物保护膜 。“钝化”时阳极的电极反应为
。“钝化”时阳极的电极反应为 用电极反应式表示
用电极反应式表示

(4)精炼铜过程中,电解质溶液
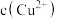 逐渐减小,
逐渐减小,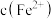 、
、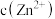 增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:
增大,会影响进一步电解精炼铜。甲同学设计如图除杂方案:
已知:
| 沉淀物 |  |  |  |  |
| 开始沉淀时的pH |  |  | 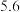 |  |
| 完全沉淀时的pH | 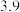 |  |  |  |
加入
 的目的是
的目的是 可除去的离子是
可除去的离子是 用平衡移动原理说明
用平衡移动原理说明
更新时间:2021-06-17 10:08:24
|
相似题推荐
【推荐1】电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:若X、Y都是惰性电极,a是饱和NaCl溶液,

(1)实验开始时,同时在两边各滴入几滴酚酞试液,则
①在X极附近观察到的现象是______ 。
②Y电极上的电极反应式是______ ,检验该电极反应产物的方法是______ 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的电极反应式是______ ,
②Y电极的材料是______ ,
③假若电路中有0.04mol电子通过时,阴极增重____ 克。
(3)生产中常用类似上述装置的原理来保护放置在海水中的金属器件,你认为金属器件应与___ 位置相同(填“X”或“Y”),我们把这种方法叫做 ___ 保护法。

(1)实验开始时,同时在两边各滴入几滴酚酞试液,则
①在X极附近观察到的现象是
②Y电极上的电极反应式是
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的电极反应式是
②Y电极的材料是
③假若电路中有0.04mol电子通过时,阴极增重
(3)生产中常用类似上述装置的原理来保护放置在海水中的金属器件,你认为金属器件应与
您最近一年使用:0次
【推荐2】回答下列问题:
(1)有一种燃料电池,所用燃料为 和空气,电解质为熔融的
和空气,电解质为熔融的 。回答下列问题
。回答下列问题
① 移向
移向_______ 极。
②正极反应式为_______ 。
③电池中 的物质的量将逐渐
的物质的量将逐渐_______ (填增大、减少、不变)。
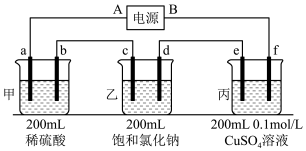
(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则
①电源A极是_______ 极。
②c极上的电极反应式:_______ 。
③甲、乙两池共可收集到_______ mol气体。
(1)有一种燃料电池,所用燃料为
 和空气,电解质为熔融的
和空气,电解质为熔融的 。回答下列问题
。回答下列问题①
 移向
移向②正极反应式为
③电池中
 的物质的量将逐渐
的物质的量将逐渐(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则

①电源A极是
②c极上的电极反应式:
③甲、乙两池共可收集到
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3 H2(g) CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+ H2(g) CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:

【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l) H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在__ 极,该电极反应式是______________ 。
CO2(g)+3 H2(g)
 CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 ICO2(g)+ H2(g)
 CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:

【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)
 H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1请回答(不考虑温度对ΔH的影响):
研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图表示一个电解池,装有电解液a、X、Y是两块电极板,通过导线与直流电源相连,请回答以下问题:
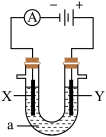
(1)若X、Y是惰性石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,在X极附近观察到的现象是______________________________ ;Y电极上的电极反应式是 ___________________ ,电解NaCl溶液的离子方程式是________________________________ 。
(2)若要在铜制品上镀Ag,则电解质溶液a可为___________________ ,Y电极反应式为_________________________________ 。
(3)若上图装置中的电源为甲醇—空气—KOH溶液的燃料电池,则电池负极的电极反应式_________________ ,电池工作过程中,正极附近的pH将______ (填“增大、减小或不变”)。

(1)若X、Y是惰性石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,在X极附近观察到的现象是
(2)若要在铜制品上镀Ag,则电解质溶液a可为
(3)若上图装置中的电源为甲醇—空气—KOH溶液的燃料电池,则电池负极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列方程式正确且能设计成原电池的是________ 。
A.KOH+HCl=KCl+H2O
B.Cu+Fe3+=Fe2++Cu2+
C.Na2O+H2O=2NaOH
D.Fe+H2SO4=FeSO4+H2
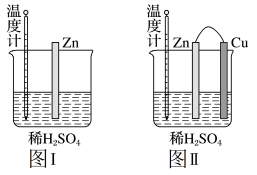
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(图Ⅰ、图Ⅱ中除连接的铜棒不同外,其他均相同)。有关实验现象,下列说法正确的是___________ 。
A.图Ⅰ中温度计的示数高于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速度比Ⅰ快
(3)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80,工作一段时间后,取出二者洗净,干燥后称重,总质量为54g,则产生氢气的体积_____ mL(标准状况)
(4)将铝片和镁片放入氢氧化钠溶液中,负极的电极反应式为:______________
(1)根据构成原电池的本质判断,下列方程式正确且能设计成原电池的是
A.KOH+HCl=KCl+H2O
B.Cu+Fe3+=Fe2++Cu2+
C.Na2O+H2O=2NaOH
D.Fe+H2SO4=FeSO4+H2
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(图Ⅰ、图Ⅱ中除连接的铜棒不同外,其他均相同)。有关实验现象,下列说法正确的是

A.图Ⅰ中温度计的示数高于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速度比Ⅰ快
(3)将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80,工作一段时间后,取出二者洗净,干燥后称重,总质量为54g,则产生氢气的体积
(4)将铝片和镁片放入氢氧化钠溶液中,负极的电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组的同学用以下装置研究电化学的问题。

(1)甲装置是由铜、锌和稀硫酸组成的原电池,其中正极材料是___ ,电池的总反应式用离子方程式表示为___ 。当导线中有1mol电子通过时,理论上两极的变化是___ (填序号)。
A.锌片溶解了32.5g B.锌片增重32.5g
C.铜片上析出lgH2 D.铜片上析1molH2
(2)若乙装置中X、Y都是惰性电极,a是滴有酚酞试液的饱和NaCl溶液。

乙
则:X极上的电极反应式为___ ,在X极附近观察到的现象是___ ;Y极上的电极反应式为___ ,检验该电极反应产物的方法是___ 。
(3)若要通过乙装置用电解方法精炼粗铜,电解质溶液a选用CuSO4溶液,则X电极的材料是___ ,X极的电极反应式为___ 。

(1)甲装置是由铜、锌和稀硫酸组成的原电池,其中正极材料是
A.锌片溶解了32.5g B.锌片增重32.5g
C.铜片上析出lgH2 D.铜片上析1molH2
(2)若乙装置中X、Y都是惰性电极,a是滴有酚酞试液的饱和NaCl溶液。

乙
则:X极上的电极反应式为
(3)若要通过乙装置用电解方法精炼粗铜,电解质溶液a选用CuSO4溶液,则X电极的材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a; X、Y 是两块电极板(X、Y都是惰性电极),A、B 是出口,通过导线与直流电源相连。请回答以下问题:

(1)若a是CuCl2溶液,则:
①X 的电极名称是___________ ,电极反应式是_________________________ 。
②在B 出口放一块湿润的KI-淀粉试纸会变为__________ 色。
(2)若a饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X 极上的电极反应式是______________ 。在X极附近观察到的现象是_____________ 。
②该电解池总反应式是___________________________________ 。
(3)若a是400mL2mol/LCuSO4溶液,一段时间阴极增重1.28g (该极无气体放出),电解后溶液体积不变,则溶液的pH 为__________ ,阳极可收集标况下气体__________ mL。

(1)若a是CuCl2溶液,则:
①X 的电极名称是
②在B 出口放一块湿润的KI-淀粉试纸会变为
(2)若a饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X 极上的电极反应式是
②该电解池总反应式是
(3)若a是400mL2mol/LCuSO4溶液,一段时间阴极增重1.28g (该极无气体放出),电解后溶液体积不变,则溶液的pH 为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列填空:硼氧化钠(NaBH4)是合成中常用的还原剂。采用NaBO2为主要原料制备NaBH4(B元素化合价为+3)的反应为:NaBO2+SiO2+Na+H2 NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
完成下列填空:
(1)上述反应中,原子最外层有两个未成对电子的元素是_____ (填元素符号)。SiO2熔点高的原因是_____ 。
(2)上述反应中H2与Na的物质的量之比为_____ 。
(3)硅酸钠水溶液产生硅酸(H2SiO3),硬化粘结,且有碱性,其原因是_____ (用离子方程式表示)。铸造工艺中可用氯化铵作为水玻璃的硬化剂。试用平衡原理加以解释_____ 。
(4)NaBH4可使许多金属离子还原成金属单质。例如它从含金离子(Au3+)的废液中提取Au.配平该反应的离子方程式:_____ Au3++_____ BH4﹣+_____ OH-→_____ Au+_____ BO2﹣+_____ H2O。
(5)最新研究发现以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,则每消耗1L6mol/L H2O2溶液,理论上流过电路中的电子数为_____ 。
 NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)完成下列填空:
(1)上述反应中,原子最外层有两个未成对电子的元素是
(2)上述反应中H2与Na的物质的量之比为
(3)硅酸钠水溶液产生硅酸(H2SiO3),硬化粘结,且有碱性,其原因是
(4)NaBH4可使许多金属离子还原成金属单质。例如它从含金离子(Au3+)的废液中提取Au.配平该反应的离子方程式:
(5)最新研究发现以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,则每消耗1L6mol/L H2O2溶液,理论上流过电路中的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键 时,观察到电流表的指针发生了偏转。请回答下列问题:
时,观察到电流表的指针发生了偏转。请回答下列问题:

(1)乙池为___________ (填“原电池”“电解池”“电镀池”), 电极的电极反应式为:
电极的电极反应式为:___________ 。
(2)丙池中 电极为
电极为___________ (填“正极”、“负极”、“阴极”或“阳极”),写出电解时总反应的离子方程式___________ 。
(3)当乙池中 极质量变化
极质量变化 时,甲池中
时,甲池中 电极理论上消耗
电极理论上消耗 的体积为
的体积为___________  (标准状况)。
(标准状况)。
(4)一段时间后,断开电键 。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。
。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。
(5)若丙池通电一段时间后,向所得的溶液中加入 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和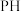 (不考虑
(不考虑 的溶解),则电解过程中转移的电子
的溶解),则电解过程中转移的电子___________  。
。
 时,观察到电流表的指针发生了偏转。请回答下列问题:
时,观察到电流表的指针发生了偏转。请回答下列问题:
(1)乙池为
 电极的电极反应式为:
电极的电极反应式为:(2)丙池中
 电极为
电极为(3)当乙池中
 极质量变化
极质量变化 时,甲池中
时,甲池中 电极理论上消耗
电极理论上消耗 的体积为
的体积为 (标准状况)。
(标准状况)。(4)一段时间后,断开电键
 。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。
。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。A. | B. | C. | D. |
 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和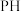 (不考虑
(不考虑 的溶解),则电解过程中转移的电子
的溶解),则电解过程中转移的电子 。
。
您最近一年使用:0次



