完成有关化学方程式:
(1)NO与O2 反应___________ 。
(2)NO2与水反应___________ 。
(3)Cu与稀硝酸反应___________ 。
(1)NO与O2 反应
(2)NO2与水反应
(3)Cu与稀硝酸反应
更新时间:2021-06-23 11:39:25
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】1.氮的氧化物
(1)氮的氧化物
简介:氮元素有_______ 五种正价态,对应有六种氧化物
(2)NO和 的重要性质和制法(横线部分书写化学方程式)
的重要性质和制法(横线部分书写化学方程式)
①性质:_______ (易被氧气氧化,无色气体转化为红棕色);
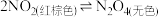 (平衡体系);
(平衡体系);
_______ (工业制硝酸);
_______ (尾气吸收);
 有较强的氧化性,能使湿润的KI淀粉试纸
有较强的氧化性,能使湿润的KI淀粉试纸_______ 。
②制法:
NO: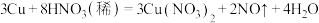 (必须
(必须_______ 法收集NO);
 :
: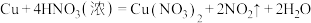 (必须
(必须_______ 法收集 )
)
(3)氮的氧化物溶于水的计算
① 或
或 与
与 (非
(非 )的混合气体溶于水可依据
)的混合气体溶于水可依据 利用气体体积变化差值进行计算。
利用气体体积变化差值进行计算。
② 和O2的混合气体溶于水时,由
和O2的混合气体溶于水时,由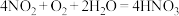 进行计算,当体积比
进行计算,当体积比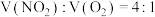 时,恰好反应;
时,恰好反应; 时,
时, 过量,剩余NO;
过量,剩余NO; 时,
时, 过量,剩余
过量,剩余 。
。
③NO和 同时通入水中时,由
同时通入水中时,由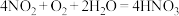 进行计算,原理同②。
进行计算,原理同②。
④NO、 、
、 的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
(1)氮的氧化物
简介:氮元素有
| 种类 | 色态 | 化学性质 |
 | 无色气体 | 较不活泼 |
| NO | 活泼,不溶于水 | |
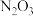 (亚硝酸酐) (亚硝酸酐) | 蓝色液体(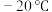 ) ) | 常温极易分解为NO, |
 | 较活泼,与水反应 | |
 | 无色气体 | 较活泼,受热易分解 |
 (硝酸酸酐) (硝酸酸酐) | 无色固体 | 气态时不稳定,易分解 |
 的重要性质和制法(横线部分书写化学方程式)
的重要性质和制法(横线部分书写化学方程式)①性质:
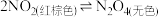 (平衡体系);
(平衡体系); 有较强的氧化性,能使湿润的KI淀粉试纸
有较强的氧化性,能使湿润的KI淀粉试纸②制法:
NO:
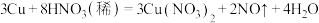 (必须
(必须 :
: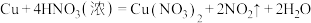 (必须
(必须 )
)(3)氮的氧化物溶于水的计算
①
 或
或 与
与 (非
(非 )的混合气体溶于水可依据
)的混合气体溶于水可依据 利用气体体积变化差值进行计算。
利用气体体积变化差值进行计算。②
 和O2的混合气体溶于水时,由
和O2的混合气体溶于水时,由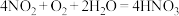 进行计算,当体积比
进行计算,当体积比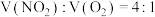 时,恰好反应;
时,恰好反应; 时,
时, 过量,剩余NO;
过量,剩余NO; 时,
时, 过量,剩余
过量,剩余 。
。③NO和
 同时通入水中时,由
同时通入水中时,由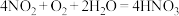 进行计算,原理同②。
进行计算,原理同②。④NO、
 、
、 的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氮及其化合物是中学化学的基础知识,请你回答下列含氮化合物的有关问题。
(1)汽车尾气中含有氮氧化物,严重污染大气。NO和NO2是常见的氮氧化物,这两种氮氧化物中,呈红棕色的是_______ ;(填写化学式)
(2)一氧化氮在常温下很容易与空气中的氧气化合,生成二氧化氮。该反应的化学方程式为:______ ;
(3)实验室常用NH3做“喷泉实验”,该实验说明NH3的溶解性是______ 溶于水(填“极易”或“极难”)。
(1)汽车尾气中含有氮氧化物,严重污染大气。NO和NO2是常见的氮氧化物,这两种氮氧化物中,呈红棕色的是
(2)一氧化氮在常温下很容易与空气中的氧气化合,生成二氧化氮。该反应的化学方程式为:
(3)实验室常用NH3做“喷泉实验”,该实验说明NH3的溶解性是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】判断正误
1.氮气在通常情况下不燃烧,也不支持燃烧,不能供呼吸。(_______)
2.液氮可用于医学和高科技领域,制造低温环境。(_______)
3.高温高压催化剂条件下与氢气反应时,氮气作还原剂。(_______)
4.固氮反应一定属于氧化还原反应。(_______)
5.高温或通电的条件下,氮气能与氧气化合生成一氧化氮。(_______)
6.N2与O2在放电条件下直接化合成NO2。(_______)
7.NO2溶于水时,NO2是氧化剂,水是还原剂。(_______)
8.NO不溶于水,所以可用排水法收集。(_______)
9.NO是一种有刺激性气味的红棕色气体。(_______)
10.常温常压下,含等质量氧元素的NO和CO的体积相等。(_______)
11.NO2不能通过化合反应获得。(_______)
12.NO2能与水反应生成硝酸,故NO2为酸性氧化物。(_______)
13.除去O2中混有的NO2,可将混合气体通过水,将NO2溶解。(_______)
14.NO2与溴蒸气的鉴别可用NaOH溶液,溶于NaOH溶液得无色溶液的是NO2,得橙色溶液的为溴蒸气。(_______)
15.CO、NO、NO2都是大气污染气体,在空气中都稳定存在。(_______)
1.氮气在通常情况下不燃烧,也不支持燃烧,不能供呼吸。(_______)
2.液氮可用于医学和高科技领域,制造低温环境。(_______)
3.高温高压催化剂条件下与氢气反应时,氮气作还原剂。(_______)
4.固氮反应一定属于氧化还原反应。(_______)
5.高温或通电的条件下,氮气能与氧气化合生成一氧化氮。(_______)
6.N2与O2在放电条件下直接化合成NO2。(_______)
7.NO2溶于水时,NO2是氧化剂,水是还原剂。(_______)
8.NO不溶于水,所以可用排水法收集。(_______)
9.NO是一种有刺激性气味的红棕色气体。(_______)
10.常温常压下,含等质量氧元素的NO和CO的体积相等。(_______)
11.NO2不能通过化合反应获得。(_______)
12.NO2能与水反应生成硝酸,故NO2为酸性氧化物。(_______)
13.除去O2中混有的NO2,可将混合气体通过水,将NO2溶解。(_______)
14.NO2与溴蒸气的鉴别可用NaOH溶液,溶于NaOH溶液得无色溶液的是NO2,得橙色溶液的为溴蒸气。(_______)
15.CO、NO、NO2都是大气污染气体,在空气中都稳定存在。(_______)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列化学方程式。
(1)二氧化氮溶于水:_______ 。
(2)浓硫酸与铜的反应:_______ 。
(3)氨的催化氧化:_______ 。
(4)甲烷与氯气的一氯取代:_______ 。
(5)乙烯的加聚反应:_______ 。
(1)二氧化氮溶于水:
(2)浓硫酸与铜的反应:
(3)氨的催化氧化:
(4)甲烷与氯气的一氯取代:
(5)乙烯的加聚反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】酸雨的形成
NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:______ 。此反应的氧化剂是______ ,氧化产物是______ ,1molNO2反应转移电子______ mol。
NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】请根据物质在生产中的应用填空:
(1)自来水厂对水消毒,常使用的物质是__________ (填“液氯”或“明矾”);
(2)制造光导纤维的基本原料是__________ (填“硅”或“二氧化硅”);
(3)铁在冷的浓硫酸或浓硝酸中,表面被氧化生成致密氧化物膜而保护内层金属。常温下盛装浓硫酸或浓硝酸可使用的容器是__________ (填“铁罐”或“铜罐”)。
(4)二氧化氮(NO2)是一种红棕色的有毒气体,二氧化氮与水反应生成硝酸和_________ ;
(5)乙烯和苯是重要有机化合物,在工业上,可以用__________ 的产量衡量一个国家的石油化工发展水平;苯滴入酸性高锰酸钾溶液中,酸性高锰酸钾溶液__________ (填“褪色”或“不褪色”);
(1)自来水厂对水消毒,常使用的物质是
(2)制造光导纤维的基本原料是
(3)铁在冷的浓硫酸或浓硝酸中,表面被氧化生成致密氧化物膜而保护内层金属。常温下盛装浓硫酸或浓硝酸可使用的容器是
(4)二氧化氮(NO2)是一种红棕色的有毒气体,二氧化氮与水反应生成硝酸和
(5)乙烯和苯是重要有机化合物,在工业上,可以用
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下列离子方程式不正确的是_______ 。
A. 通入酸性
通入酸性 溶液中:
溶液中: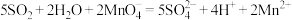
B.锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag
C.向稀Fe(NO3)2溶液中加入稀盐酸:Fe2++2H++NO =Fe3++NO↑+H2O
=Fe3++NO↑+H2O
D.向FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl-
E.向稀硝酸中加入铜片:Cu+2H++NO =Cu2++NO↑+H2O
=Cu2++NO↑+H2O
A.
 通入酸性
通入酸性 溶液中:
溶液中: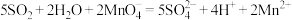
B.锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag
C.向稀Fe(NO3)2溶液中加入稀盐酸:Fe2++2H++NO
 =Fe3++NO↑+H2O
=Fe3++NO↑+H2OD.向FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl-
E.向稀硝酸中加入铜片:Cu+2H++NO
 =Cu2++NO↑+H2O
=Cu2++NO↑+H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】请按要求回答下列问题:
(1)乙醇的结构式______ ;聚异戊二烯的结构简式______ 。
(2)写出铜与浓硝酸反应的离子方程式______ 。
(3) 是一种
是一种______ (填“酸性”、“碱性”或“两性”)氧化物。实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞。请结合化学方程式解释其中原因:______ 。
(1)乙醇的结构式
(2)写出铜与浓硝酸反应的离子方程式
(3)
 是一种
是一种
您最近一年使用:0次

 、
、 、
、 、
、 中的一种。现进行下列实验:
中的一种。现进行下列实验: 无明显变化:
无明显变化: 无明显变化;
无明显变化; 生成溶液及沉淀物E:
生成溶液及沉淀物E: 生成溶液F及沉淀:少量E溶于过量F中,生成溶液并放出气体。
生成溶液F及沉淀:少量E溶于过量F中,生成溶液并放出气体。 的电离方程式
的电离方程式

