已知短周期元素X、Y、Z在周期表中的位置如图:

按要求回答下列问题:
(1)若Y的-2价阴离子结构示意图为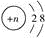 ,则
,则
①Y元素在周期表中位于第___ 周期第___ 族。
②Y与X形成的化合物X2Y2中含有的化学键是___ ,其电子式为___ 。
③用电子式的形式表示X与Z形成化合物的过程:__ 。
(2)若Y元素原子核外最外层电子数是次外层电子数的2倍,则Y元素形成的氢化物的分子空间构型为___ ,其结构式为___ ,最高价氧化物的分子空间构型为___ ,其电子式为__ 。

按要求回答下列问题:
(1)若Y的-2价阴离子结构示意图为
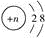 ,则
,则①Y元素在周期表中位于第
②Y与X形成的化合物X2Y2中含有的化学键是
③用电子式的形式表示X与Z形成化合物的过程:
(2)若Y元素原子核外最外层电子数是次外层电子数的2倍,则Y元素形成的氢化物的分子空间构型为
更新时间:2021-06-23 08:54:33
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素,用化学用语回答下列问题:
(1)⑤在元素周期表中的位置是__________ 。
(2)①的最高价氧化物的结构式为___________ 。
(3)②③单质在加热条件下形成的物质中含有的化学键类型是__________ 。
(4)用电子式表示④⑦元素物质的形成过程__________ 。
(5)②、④、⑥离子半径由大到小的顺序为____________ 。
(6)②⑦组成的物质是新的自来水消毒剂,可以用来除去水中超标的锰离子,生成黑色沉淀,当消耗13.50g②⑦组成的物质时,共转移了1mol电子,则反应的离子方程式为____________ 。
① | ② | |||||||
③ | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)①的最高价氧化物的结构式为
(3)②③单质在加热条件下形成的物质中含有的化学键类型是
(4)用电子式表示④⑦元素物质的形成过程
(5)②、④、⑥离子半径由大到小的顺序为
(6)②⑦组成的物质是新的自来水消毒剂,可以用来除去水中超标的锰离子,生成黑色沉淀,当消耗13.50g②⑦组成的物质时,共转移了1mol电子,则反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】如表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
请根据要求用元素符号或化学式回答下列问题:
(1)表中所列元素中,原子最外层有2个电子的元素为___ 。
(2)画出d元素原子的结构示意图___ ,其气态氢化物溶于水显___ 性。(填“酸”或“碱”)
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱___ >___ 。
(4)表中j元素的电子排布式___ 。
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是___ (填写化合物的化学式,下同),具有两性的是___ 。
| a | b | ||||||||||||||||
| c | d | e | f | ||||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o |
(1)表中所列元素中,原子最外层有2个电子的元素为
(2)画出d元素原子的结构示意图
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱
(4)表中j元素的电子排布式
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】如图是现行元素周期表的一部分,请回答:
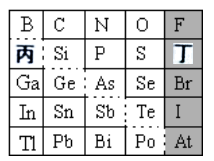
(1)元素Se在周期表中的位置为___________ 。
(2)下列说法正确的是___________ 。
A.丙位于周期表中从左到右数第13列
B.Bi的最高价氧化物的化学式为Bi2O5
C.丁所形成的含氧酸是强酸
D.C、N、O三种元素的最高正价等于其所在族的族序数
(3)①阴影部分元素所形成的氢化物中热稳定性最高的是___________ (填化学式)。请从原子结构的角度解释其原因:___________ 。
②可在图中分界线(虚线部分)附近寻找___________ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.新品种农药
(4)Pb能形成多种氧化物,如碱性氧化物PbO,酸性氧化物PbO2,还有类似于Fe3O4中铁元素价态特征(有两种价态)的Pb3O4,Pb3O4能与硝酸发生非氧化还原反应生成一种盐和一种铅的氧化物,写出该反应的化学方程式___________ 。

(1)元素Se在周期表中的位置为
(2)下列说法正确的是
A.丙位于周期表中从左到右数第13列
B.Bi的最高价氧化物的化学式为Bi2O5
C.丁所形成的含氧酸是强酸
D.C、N、O三种元素的最高正价等于其所在族的族序数
(3)①阴影部分元素所形成的氢化物中热稳定性最高的是
②可在图中分界线(虚线部分)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料 D.新品种农药
(4)Pb能形成多种氧化物,如碱性氧化物PbO,酸性氧化物PbO2,还有类似于Fe3O4中铁元素价态特征(有两种价态)的Pb3O4,Pb3O4能与硝酸发生非氧化还原反应生成一种盐和一种铅的氧化物,写出该反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】有A、B、C、D四种元素,它们的核电荷数依次增大,已知:
①A原子最外层电子数是次外层电子数的两倍,D原子M层上的电子比K层多5个。
②B的阴离子与跟氖原子的电子层结构相同,0℃、101.3KPa时B可形成B2气体,经测定0.2mol B2气体为6.4g.
③C与B构成的CB2中,C的质量分数为50%,在C原子核中,质子数与中子数相同。
回答:
(1)写出A元素的名称是______ 、B的元素符号是____ .
(2)写出下列微粒的结构示意图或电子式:
①A的原子结构示意图_________ ;②B的阴离子的电子式_________ ;
③C的离子的结构示意图__________ ;④D的阴离子的电子式__________ 。
①A原子最外层电子数是次外层电子数的两倍,D原子M层上的电子比K层多5个。
②B的阴离子与跟氖原子的电子层结构相同,0℃、101.3KPa时B可形成B2气体,经测定0.2mol B2气体为6.4g.
③C与B构成的CB2中,C的质量分数为50%,在C原子核中,质子数与中子数相同。
回答:
(1)写出A元素的名称是
(2)写出下列微粒的结构示意图或电子式:
①A的原子结构示意图
③C的离子的结构示意图
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:
(1)元素⑩在周期表中的位置是___________ ,⑦的原子结构示意图为___________ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为___________ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是___________ (用名称表示),最高价氧化物对应水化物中,酸性最强的是___________ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式___________ 。
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
只存在共价键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在共价键的是___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑩ |
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
只存在共价键的是
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知有A、B、C、D、E五种短周期元素元素,其原子序数依次增大。F是常见的金属,在潮湿的空气中被腐蚀形成红棕色固体。A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正价与最低负价的代数和为6,D是同周期中离子半径最小的元素。
(1)五种元素中,金属性最强的元素在周期表的位置是________写出D元素的原子结构示意图________
(2)B元素的气态氢化物与其最高价氧化物对应的水化物化合,生成物的水溶液呈___性,原因________(离子方程式表示)上述化合物浓溶液滴加到Mg(OH)2悬浊液中,沉淀逐渐消失最后澄清,请解释澄清的原因______________________________________________
(3)含F的二价离子的酸性溶液,在空气中易被氧化变质,该过程的离子反应为:____________________
检验该二价离子没有被完全氧化的方法为:_______________________________
(4).E元素的最高价氧化物对应的水化物与D元素的最高价氧化物对应的水化物反应的化学方程式为____________________________________________________
(1)五种元素中,金属性最强的元素在周期表的位置是________写出D元素的原子结构示意图________
(2)B元素的气态氢化物与其最高价氧化物对应的水化物化合,生成物的水溶液呈___性,原因________(离子方程式表示)上述化合物浓溶液滴加到Mg(OH)2悬浊液中,沉淀逐渐消失最后澄清,请解释澄清的原因______________________________________________
(3)含F的二价离子的酸性溶液,在空气中易被氧化变质,该过程的离子反应为:____________________
检验该二价离子没有被完全氧化的方法为:_______________________________
(4).E元素的最高价氧化物对应的水化物与D元素的最高价氧化物对应的水化物反应的化学方程式为____________________________________________________
您最近半年使用:0次



