如表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
请根据要求用元素符号或化学式回答下列问题:
(1)表中所列元素中,原子最外层有2个电子的元素为___ 。
(2)画出d元素原子的结构示意图___ ,其气态氢化物溶于水显___ 性。(填“酸”或“碱”)
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱___ >___ 。
(4)表中j元素的电子排布式___ 。
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是___ (填写化合物的化学式,下同),具有两性的是___ 。
| a | b | ||||||||||||||||
| c | d | e | f | ||||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o |
(1)表中所列元素中,原子最外层有2个电子的元素为
(2)画出d元素原子的结构示意图
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱
(4)表中j元素的电子排布式
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是
更新时间:2021-05-20 13:12:32
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素, 请根据要求回答问题:
(1)画出②的原子结构示意图_______ 。
(2)①的最高价氧化物的电子式_______ 。
(3)③和⑥分别形成的氢化物中,最稳定的是_______ (填化学式)。
(4)写出⑤的单质与④的最高价氧化物对应的水化物反应的化学方程式_______ 。
族 周期 | IA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | Ar | |||||
(2)①的最高价氧化物的电子式
(3)③和⑥分别形成的氢化物中,最稳定的是
(4)写出⑤的单质与④的最高价氧化物对应的水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:___________ (填标号);化学性质最不活泼的元素是___________ (填元素符号)。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序___________ (填化学式)。
(4)用电子式表示J与C形成化合物的过程:___________ 。
(5)请写出B的最高价氧化物对应的水化物与E发生反应的化学方程式:___________ 。

(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序
(4)用电子式表示J与C形成化合物的过程:
(5)请写出B的最高价氧化物对应的水化物与E发生反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下图是元素周期表的一部分,根据①~⑨在周期表中的位置按题目要求回答:
(1)在元素①~⑨中,金属性最强的元素是___________ (填元素符号)。
(2)画出元素④的原子结构示意图___________ 。
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,甲物质的电子式为___________ ,其化学键类型为___________ 共价键(填“极性”或“非极性”)。
(4)元素③⑤对应的最高价氧化物的水化物,它们相互之间能发生反应的离子方程式为___________ 。
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程___________ 。
(6)②与⑥分别形成的氢化物中,稳定性较高的是___________ (填化学式),⑥和⑦的最高价氧化物的水化物酸性___________ 
___________ (填化学式)。
| 族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ | ||||||
(2)画出元素④的原子结构示意图
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,甲物质的电子式为
(4)元素③⑤对应的最高价氧化物的水化物,它们相互之间能发生反应的离子方程式为
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程
(6)②与⑥分别形成的氢化物中,稳定性较高的是

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,表中所列字母分别代表一种元素.

(1)常温下,其单质呈液态的元素是____ (填字母代号),它与e形成的化合物电子式为:_____ (用元素符号表示)
b元素形成的单质所属晶体类型可能是____ (填序号)
①分子晶体 ②原子晶体 ③金属晶体 ④离子晶体 ⑤过渡型晶体
(2)元素c、d、g的氢化物的沸点由高到低的顺序为______ (用化学式表示)

(1)常温下,其单质呈液态的元素是
b元素形成的单质所属晶体类型可能是
①分子晶体 ②原子晶体 ③金属晶体 ④离子晶体 ⑤过渡型晶体
(2)元素c、d、g的氢化物的沸点由高到低的顺序为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,推出图中标记的11种元素,回答下列问题:
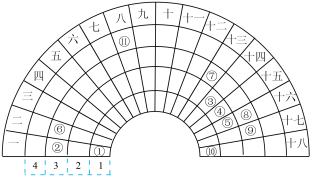
(1)⑤的简单阴离子的结构示意图为_______ ,⑪的原子序数为___________ 。
(2)④的简单氢化物的电子式为__________________ 。
(3)在11种元素中,单质的化学性质最不活泼的是__________ (填化学式)。
(4)⑧、⑨两种元素形成的最高价氧化物的水化物中,酸性较强的是_______ (填化学式)。
(5)加热时,③的单质能和⑧的最高价氧化物的水化物的浓溶液发生反应,化学方程式为___________ 。
(6)⑦在元素周期表中的位置是_____________ 。

(1)⑤的简单阴离子的结构示意图为
(2)④的简单氢化物的电子式为
(3)在11种元素中,单质的化学性质最不活泼的是
(4)⑧、⑨两种元素形成的最高价氧化物的水化物中,酸性较强的是
(5)加热时,③的单质能和⑧的最高价氧化物的水化物的浓溶液发生反应,化学方程式为
(6)⑦在元素周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语 回答下列问题。
(1)元素①的原子结构示意图为________ 。
(2)元素③和⑤可形成化合物,用电子式表示其形成过程______ 。
(3)元素②、③形成离子的半径_____ >______ 。
(4) 元素③、④形成的最高价氧化物水化物的碱性__ >____ 。
(5)元素⑥的单质与元素③⑨组成的化合物的水溶液反应的离子方程式为___ 。请从原子结构的角度解释该反应能发生的原因:____ 。
(6)某同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成①、⑦、⑧的非金属性强弱比较的实验研究;从以下所给物质中选出实验所需的物质:a.稀HNO3 b.稀盐酸 c.碳酸钙 d.Na2SiO3溶液 e.SiO2。

试剂A为________ ;(填字母,下同)试剂B为________ ;试剂C为________ 。
写出该过程中的化学方程式________ 、________ 。该装置存在一个缺陷是________ 。
族 周期 | IA | 0 | |||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
2 | ⑦ | ① | ② | ||||||
3 | ③ | ④ | ⑧ | ⑤ | ⑥ | ||||
4 | ⑨ | ||||||||
(2)元素③和⑤可形成化合物,用电子式表示其形成过程
(3)元素②、③形成离子的半径
(4) 元素③、④形成的最高价氧化物水化物的碱性
(5)元素⑥的单质与元素③⑨组成的化合物的水溶液反应的离子方程式为
(6)某同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成①、⑦、⑧的非金属性强弱比较的实验研究;从以下所给物质中选出实验所需的物质:a.稀HNO3 b.稀盐酸 c.碳酸钙 d.Na2SiO3溶液 e.SiO2。

试剂A为
写出该过程中的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表示为
,其实验过程可表示为
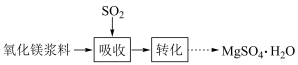
(1)在搅拌下向氧化镁浆料中匀速缓慢通入 气体,生成
气体,生成 ,反应为
,反应为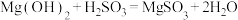 ,其平衡常数K与
,其平衡常数K与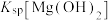 、
、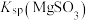 、
、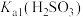 、
、 、
、 的代数关系式为
的代数关系式为
__________ 。
(2)①水浴加热氧化镁浆料,不一定能提高氧化镁浆料吸收 效率,说明原因
效率,说明原因__________ 。
②写出一种能提高氧化镁浆料吸收 效率的操作
效率的操作__________ 。
(3)在负载钴的分子筛催化剂作用下 被
被 氧化为
氧化为 。已知
。已知 的溶解度为
的溶解度为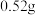 (19℃),若
(19℃),若 饱和溶液的密度以
饱和溶液的密度以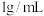 计。
计。
①计算19℃时,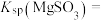
__________ 。
②写出 氧化溶液中
氧化溶液中 的离子方程式为
的离子方程式为__________ 。
③金属钴在周期表中的位置是__________ 。钴原子价电子排布式为__________ 。
(4)在其他条件相同时,浆料中 被
被 氧化的速率随pH的变化如图所示。在
氧化的速率随pH的变化如图所示。在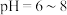 范围内,pH增大,浆料中
范围内,pH增大,浆料中 的氧化速率增大,其主要原因是
的氧化速率增大,其主要原因是__________ 。
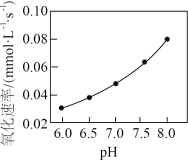
 ,其实验过程可表示为
,其实验过程可表示为
(1)在搅拌下向氧化镁浆料中匀速缓慢通入
 气体,生成
气体,生成 ,反应为
,反应为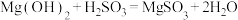 ,其平衡常数K与
,其平衡常数K与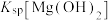 、
、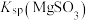 、
、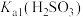 、
、 、
、 的代数关系式为
的代数关系式为
(2)①水浴加热氧化镁浆料,不一定能提高氧化镁浆料吸收
 效率,说明原因
效率,说明原因②写出一种能提高氧化镁浆料吸收
 效率的操作
效率的操作(3)在负载钴的分子筛催化剂作用下
 被
被 氧化为
氧化为 。已知
。已知 的溶解度为
的溶解度为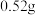 (19℃),若
(19℃),若 饱和溶液的密度以
饱和溶液的密度以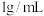 计。
计。①计算19℃时,
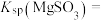
②写出
 氧化溶液中
氧化溶液中 的离子方程式为
的离子方程式为③金属钴在周期表中的位置是
(4)在其他条件相同时,浆料中
 被
被 氧化的速率随pH的变化如图所示。在
氧化的速率随pH的变化如图所示。在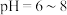 范围内,pH增大,浆料中
范围内,pH增大,浆料中 的氧化速率增大,其主要原因是
的氧化速率增大,其主要原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】配合物在许多尖端领域如激光材料、超导材料、抗癌药物、催化剂、自组装超分子等方面有广泛的应用。回答下列问题:
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。碳原子的核外电子排布式为___________ 。CO的结构式为C≡O,则Ni(CO)4分子中σ键与π键个数之比为___________ 。
(2)胆矾溶于水后可得蓝色的水合铜离子,其中 的配位数是
的配位数是___________ 。胆矾晶体的结构如下图所示,其存在的化学键有___________ (填字母)。

A.离子键 B.极性键 C.范德华力 D.氢键 E.配位键
(3)金属Ni可以与Mg、C形成一种新型超导体,它的临界温度为8K,由C、Mg、Ni形成的某物质的晶胞为正六面体,结构如图所示。
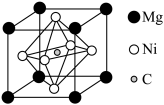
①该物质的化学式为___________ 。
②每个Mg原子距离最近的Ni原子的个数是___________ 。
③若用NA表示阿伏伽德罗常数的值,如果晶体的密度为ρg/cm3,则该晶胞的体积为___________ nm3(用含ρ、NA的代数式表示)。
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。碳原子的核外电子排布式为
(2)胆矾溶于水后可得蓝色的水合铜离子,其中
 的配位数是
的配位数是
A.离子键 B.极性键 C.范德华力 D.氢键 E.配位键
(3)金属Ni可以与Mg、C形成一种新型超导体,它的临界温度为8K,由C、Mg、Ni形成的某物质的晶胞为正六面体,结构如图所示。

①该物质的化学式为
②每个Mg原子距离最近的Ni原子的个数是
③若用NA表示阿伏伽德罗常数的值,如果晶体的密度为ρg/cm3,则该晶胞的体积为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】氮化钛广泛用于耐高温、耐磨损及航空航天等领域。一种氮化钛的制备反应为:6TiCl4+8NH3 = 6TiN+24HCl+N2 ,回答下列问题:
(1)钛在元素周期表中的位置为_____________ ,基态Ti原子价层电子的轨道表达式为________ 。
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为____________ ;NH4+的空间构型为___________ ;NO2+中氮原子的杂化形式为_______ ,其中σ键与π键的数目比为_________ 。
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为___________ ,该晶体中微粒之间的作用力为___________ 。
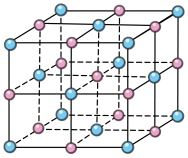
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为_______ ;该氮化钛的密度为5.4 g/cm3,则其晶胞参数a=___________ pm(用NA表示阿伏加德常数的数值,只列算式)。
(1)钛在元素周期表中的位置为
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为

您最近一年使用:0次



